初中化学人教版九年级下册第九单元 溶液综合与测试学案设计
展开【学习目标】
1.掌握溶液、溶质、溶剂、饱和溶液、不饱和溶液、溶解度、溶质的质量分数等概念。
2.掌握溶解过程中的放热和吸热现象;掌握溶解度曲线的意义及应用。
3.掌握溶质质量分数的有关计算;初步学会配制一定溶质质量分数的溶液。
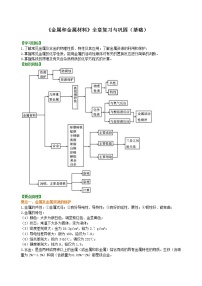
【知识网络】
【要点梳理】
要点一、溶液、饱和溶液、不饱和溶液
1.溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。被溶解的物质叫做溶质;能溶解其他物质的物质叫溶剂。
2.溶液的特征:均一性、稳定性。
3.饱和溶液与不饱和溶液:
【要点诠释】
浓溶液、稀溶液与饱和溶液、不饱和溶液的区别与联系:
要点二、溶解过程中的吸热和放热现象、乳浊液和乳化现象
1.溶解时的热现象:浓硫酸、氢氧化钠等物质溶于水,溶液温度升高;硝酸铵等物质溶于水时,溶液温度降低;氯化钠等物质溶于水,溶液温度不变。
2.乳浊液:小液滴分散到液体里形成的混合物,叫乳浊液。如:把植物油和水混合振荡后得到的浑浊的液体,就是乳浊液。该混合物不稳定,静置分层。
3.乳化现象:是指加入乳化剂后,乳浊液(植物油和水的混合物)不再分层而能稳定存在,使植物油分散成无数细小的液滴能随水流走。衣服餐具上的油污可以用加入洗涤剂的水洗掉就是这个道理。
【要点诠释】
汽油和洗洁精都能洗去油污但原理不同,汽油洗油污是油污溶解在汽油中形成溶液,而洗洁精洗油污是发生了乳化现象,不能形成溶液。
要点三、溶解度、溶解度曲线
1.固体的溶解度:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
2.固体物质的溶解度与溶解性的关系:
【要点诠释】
1.温度对固体溶解度的影响规律:
(1)大多数物质的溶解度随温度升高而增大(如KNO3);
(2)少数物质的溶解度受温度影响不大(如NaCl);
(3)极少数物质的溶解度随温度升高而减小(如Ca(OH)2)。
2.气体的溶解度随压强的增大而增大,随温度的升高而减小。
要点四、溶质的质量分数、配制一定溶质质量分数的溶液
1.溶质的质量分数:是溶质质量与溶液质量之比。
(1)溶质的质量分数=溶质质量/溶液质量 ×100%
(2)饱和溶液中溶质的质量分数=溶解度÷(100g+溶解度)×100%
2.配制溶液的主要步骤:计算、称量(量取)、溶解。
【要点诠释】
溶解度与溶质的质量分数的比较:
要点五、溶液的稀释、浓缩
1.关于溶液稀释的计算:
(1)溶液稀释前后,溶质的质量不变。
(2)若设浓溶液质量为A g,溶质的质量分数为a%,加水稀释成溶质的质量分数为b%的稀溶液B g,则
A g×a%=Bg×b%(其中B=A+m水)
2.关于溶液浓缩(无溶质析出)的计算:
(1)向原溶液中添加溶质:溶液增加溶质前后,溶剂的质量不变。增加溶质后,溶液中溶质的质量=原溶液中溶质的质量+增加的溶质的质量,而溶液的质量=原溶液的质量+增加的溶质的质量。若设原溶液质量为A g,溶质的质量分数为a%,加溶质Bg后变成溶质的质量分数为b%的溶液,则
Ag×a%+Bg=(A g+Bg)×b%。
(2)将原溶液蒸发掉部分溶剂:溶液蒸发溶剂前后,溶质的质量不变。若设原溶液质量为A g,溶质的质量分数为a%,蒸发Bg水后变成溶质的质量分数为b%的溶液,则
Ag×a%=(Ag一Bg)×b%。
(3)与浓溶液混合:混合后溶液的总质量等于两混合溶液的质量之和,混合后溶液中溶质质量等于两混合溶液的溶质质量之和。若设原溶液质量为 A g,溶质的质量分数为a%,浓溶液质量为B g,溶质的质量分数为b%,两溶液混合后得到溶质的质量分数为c%的溶液,则
Ag×a%+B g× b%=(Ag+Bg)×c%。
【要点诠释】
1.关于溶液稀释的计算一定要抓住:溶液稀释前后,溶质的质量不变。然后根据所给信息列方程求解。
2.关于溶液浓缩(无溶质析出)的计算,要根据浓缩的具体类型来具体分析找出等量关系来解决。
【典型例题】
类型一、考查溶液、饱和溶液、不饱和溶液、溶解度、溶质的质量分数等概念及溶解度曲线
1.(2016•苍梧县一模)溶液在加水稀释后,下列各量不发生变化的是( )
【思路点拨】根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答。
【答案】A
【解析】A、溶液在加水稀释后,溶质质量不变,选项正确。
B、溶液在加水稀释后,溶质质量不变,溶剂质量增加,溶液质量增加,选项错误。
C、溶液在加水稀释后,溶质质量不变,溶剂质量增加,溶液体积增加,选项错误。
D、溶液在加水稀释后,溶质质量不变,溶剂质量增加,溶质的质量分数减小,选项错误。
【总结升华】本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在。
2.下列说法正确的是( )
A.在一定条件下饱和溶液可以变成不饱和溶液
B.饱和溶液肯定是较浓的溶液
C.饱和溶液肯定要比不饱和溶液的质量分数要大些
D.在一定的溶剂中不能再溶解某种溶质的溶液叫饱和溶液
【答案】A
【解析】改变温度或加水均可使某饱和溶液变成不饱和溶液,A正确;某些物质在某温度时的溶解度很小,所以它形成饱和溶液后,溶质质量分数仍很小,B不正确;C也不正确,因为:①没有指明是不是同一种溶质,②没有指明是不是在同一温度下;D不正确,没有指明温度。
【总结升华】掌握溶液、溶质、溶剂、饱和溶液、不饱和溶液等概念是解题的关键。
3.右图是甲、乙、丙、丁四种物质的溶解度曲线。温度为t1℃时,
将等质量甲、乙、丙、丁四种物质分别加到100g水中,充分搅拌后只
得到一种饱和溶液,该饱和溶液中的溶质是( )
A.甲 B.乙 C.丙 D.丁
【答案】C
【解析】一定温度下,一定量水中加入等质量的不同溶质,溶解度最小的最先达到饱和。观察几种物质的溶解度曲线,t1℃时丙的溶解度最小,其最容易达到饱和。
【总结升华】本题要根据溶解度曲线,判断出几种物质在t1℃时的溶解度大小,然后进行判断。
举一反三:
【变式】(2014•北京中考)下列物质放入水中,能形成溶液的是( )
A.面粉 B.牛奶 C.食盐 D.植物油
【答案】C
【解析】面粉不溶于水,与水混合形成的是悬浊液,不是溶液,故A错误;牛奶与水混合形成的是乳浊液,不是溶液,故B错误;食盐易溶于水,形成均一、稳定的混合物,属于溶液,故C正确;植物油不溶于水,与水混合形成的是乳浊液,故D错误。
类型二、考查溶解过程中的吸热、放热现象及乳化现象
4. (2014•山东中考)下列固体物质溶于水后,能使液体温度明显降低的是( )
A、氯化钠 B、硝酸铵 C、生石灰 D、氢氧化钠
【思路点拨】物质在溶解时经常伴随有吸热或放热现象,如氢氧化钠固体、浓硫酸溶于水放出大量的热,溶液温度升高;硝酸铵固体溶于水吸热,溶液温度降低。解题时根据常见物质溶于水的吸热或放热现象、溶液温度的变化情况进行分析解答即可。
【答案】B
【解析】生石灰、氢氧化钠溶于水,溶液温度升高;硝酸铵溶于水,溶液温度降低;食盐溶于水,溶液温度无明显变化。
【总结升华】在物质溶解形成溶液的过程中,所发生的溶质的分子(或离子)向溶剂中扩散的过程吸收热量,而溶质的分子(或离子)与水分子作用生成水合分子(或水合离子)的过程放出热量。当:扩散吸热>水合放热——溶液温度降低;扩散吸热=水合放热——溶液温度不变;扩散吸热<水合放热——溶液温度升高。
举一反三:
【变式】各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是( )
A.用汽油除去衣服上的油污 B.用餐具洗洁精清洗餐具上的油污
C.用水洗去盘子中的水果渣 D.用醋洗去水壶的水垢
【答案】B
类型三、考查溶液的配制、稀释、溶质质量分数及有关计算
5.要配制100g 溶质质量分数为10%的氯化钠溶液,下列操作中正确的是( )
A.将10g氯化钠固体直接放在天平的托盘上称量
B.量取90ml水时,俯视读数
C.为加快固体溶解,用温度计搅拌溶液
D.将配好的溶液倒入细口瓶中,盖紧瓶塞,并贴上标签
【答案】D
【解析】氯化钠要放在纸上称量;量取液体读数时,视线要和凹液面的最低处保持水平;温度计不能当玻璃棒用。
【总结升华】要掌握溶液的配制步骤和常见化学仪器操作要点。
6.病人在医院接受静脉注射或滴注时,常用到生理盐水即氯化钠注射液。下图是某药业公司生产的氯化钠注射液包装标签上的部分文字。
请回答:
(1)该注射液里的溶质是_____________________;该注射液的溶质质量分数是(该注射液的密度为1g/mL)___________。
(2)常温下,一瓶合格的氯化钠注射液密封放置一段时间后, (填“会”或“不会”)出现浑浊现象。
【答案】(1)氯化钠(或NaCl) 0.9%
(2)不会
【解析】被溶解的物质叫做溶质。看商标可知氯化钠注射液里的溶质是氯化钠。溶质的质量分数为溶质质量和溶液质量之比,100mL溶液的质量为100g,含溶质质量是0.9g,因此可求出溶质质量分数为0.9%。
【总结升华】氯化钠溶液是均一、稳定的混合物,故在常温、密封放置情况下,不会出现浑浊现象。
举一反三:
【变式1】要将100g溶质质量分数为20%的硝酸钾溶液稀释成溶质质量分数为10%的硝酸钾溶液,需加入水的质量为( )
A.50g B.90g C.100g D.200g
【答案】C
【变式2】用氯化钠固体配制50g质量分数为5%氯化钠溶液,下列仪器中需要用到的是( )
A、②④⑥⑦ B、①④⑤⑥ C、①③⑤⑦ D、①③④⑥
【答案】B
饱和溶液
不饱和溶液
概念
在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫这种溶质的饱和溶液
在一定温度下,在一定量的溶剂里,能再溶解某种溶质的溶液,叫这种溶质的不饱和溶液
相互转化
(饱和溶液是针对某种溶质而言,对其它溶质不一定是饱和溶液)
饱和与不饱和溶液
浓溶液与稀溶液
区别
涵义不同
溶液是否饱和取决于溶质在一定温度、一定量的溶剂里,是否达到最大溶解限度
溶液的浓与稀取决于溶质在一定量溶液里含量的多与少
温度影响
受温度影响,须指明温度
一般不受温度影响
联系
1.溶液的饱和与不饱和与溶液的浓与稀没有必然的联系
2.饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液;反之亦然
3.对同一种溶质,在一定温度时,饱和溶液比不饱和溶液的溶质的质量分数大
溶解性
溶解度
意义
一种物质溶解在另一种物质里的能力
一定温度下,100g溶剂中最多溶解溶质的质量
影响因素
溶质、溶剂的性质
溶质、溶剂的性质,温度、压强等
表示方法
定性:易溶、可溶、微溶、难溶
定量:溶解度
溶解度曲线、溶解度表
联系
溶解度是溶解性的定量表示方法
溶解度(S)
溶质的质量分数(W%)
概念
一定温度时,100g溶剂中最多溶解溶质的质量
任意溶液中,溶质质量与溶液质量之比
表示意义
某物质溶解能力的大小
任一溶液的浓度大小
条件
一定温度
温度不一定相同
状态
饱和溶液
饱和或不饱和溶液
单位
g
无单位
联系
饱和溶液中溶质的质量分数=溶解度/(溶解度+100克)×100%
A.溶质质量
B.溶液质量
C.溶液体积
D.溶质的质量分数
氯化钠注射液
【规格】 100mL含氯化钠0.9g
【注意】 使用前发现溶液中有絮状物、瓶身细微破裂
等均不可使用
【贮藏】 密封保存
…… …… …
①
②
③
④
⑤
⑥
⑦
初中第三单元 物质构成的奥秘综合与测试导学案及答案: 这是一份初中第三单元 物质构成的奥秘综合与测试导学案及答案,共5页。学案主要包含了学习目标,知识网络,要点梳理,要点诠释,典型例题,思路点拨,总结升华等内容,欢迎下载使用。
人教版九年级上册本单元综合和测试导学案: 这是一份人教版九年级上册本单元综合和测试导学案,共7页。学案主要包含了学习目标,知识网络,要点梳理,要点诠释,典型例题,思路点拨,总结升华,答案与解析等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 化学元素与人体健康导学案: 这是一份初中化学人教版九年级下册课题2 化学元素与人体健康导学案,共7页。学案主要包含了学习目标,知识网络,要点梳理,要点诠释,典型例题,思路点拨,总结升华,提出问题等内容,欢迎下载使用。