




- 1.1+物质的分类及转化【综合训练】-2022-2023学年高一化学考点分层解读与综合训练(人教版2019必修第一册) 试卷 26 次下载
- 1.2+离子反应【分层解读】-2022-2023学年高一化学考点分层解读与综合训练(人教版2019必修第一册) 试卷 20 次下载
- 1.3+氧化还原反应【分层解读】-2022-2023学年高一化学考点分层解读与综合训练(人教版2019必修第一册) 试卷 23 次下载
- 1.3+氧化还原反应【综合训练】-2022-2023学年高一化学考点分层解读与综合训练(人教版2019必修第一册) 试卷 22 次下载
- 2.1+钠及其化合物【分层解读】-2022-2023学年高一化学考点分层解读与综合训练(人教版2019必修第一册) 试卷 22 次下载
化学人教版 (2019)第二节 离子反应优秀复习练习题
展开一、单选题(共14小题,每小题只有一个选项符合题意)
1.下列各组物质,前者属于电解质,后者属于非电解质的是
A.NaCl晶体、BaSO4B.液态的醋酸、酒精
C.铜、二氧化硫D.熔融的KNO3、硫酸溶液
2.向下列物质中滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是
A.BaCl2B.Ba(OH)2C.Na2CO3D.KOH
3.海盐经溶解、过滤后仍含有可溶性杂质Ca2+、Mg2+、SO,为了得到纯净的NaCl,下列试剂(均过量)的滴加顺序及操作顺序不合理的是
A.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤→稀盐酸→蒸发结晶
B.Ba(OH)2溶液→Na2CO3溶液→过滤→稀盐酸→蒸发结晶
C.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤→稀盐酸→蒸发结晶
D.BaCl2溶液→Na2CO3溶液→NaOH溶液→过滤→稀盐酸→蒸发结晶
4.下列各组离子在指定溶液中能大量共存的是
①无色溶液中:、、
②能使酚酞试剂变红的溶液中:、、
③加入Mg能放出的溶液中:、、
④无色、透明溶液中:、、
A.①②B.③④C.②④D.①④
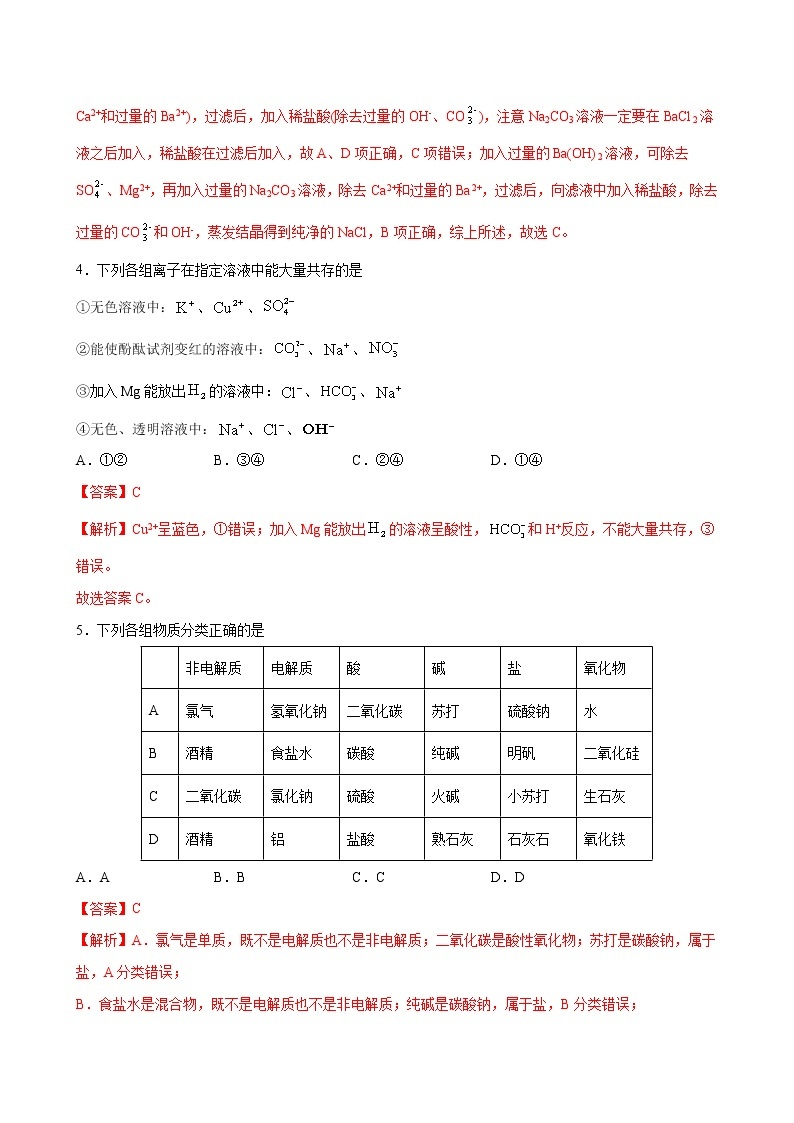
5.下列各组物质分类正确的是
6.下列反应①和②可以用同一离子方程式表示的是( )
A.①稀盐酸+碳酸钠溶液;②稀盐酸+碳酸氢钠溶液
B.①氢氧化钠溶液+稀盐酸;②氢氧化钡溶液+稀硫酸
C.①氯化钡溶液+稀硫酸;②氢氧化钡溶液+硫酸钠溶液
D.①稀盐酸+碳酸钙粉末;②稀硫酸+碳酸钠溶液
7.在碱性溶液中能大量共存且溶液为无色透明的离子组是
A.、、、B.、、、
C.、、、D.、、、
8.已知:。某无色溶液中可能含有、、、、、、,且所有离子的物质的量浓度相等。向该溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
A.肯定不含B.可能含有C.肯定含有D.肯定含有
9.重金属离子具有毒性。实验室中有甲、乙两种重金属离子的废液,甲废液经化验呈碱性,主要为有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低。则乙废液中可能含有的离子是
A.Cu2+和SOB.Cu2+和ClC.K+和SOD.Ag+和NO
10.下列离子方程式书写正确的是
A.碳酸钠溶液与盐酸反应:
B.氨水中加盐酸:
C.硫酸铜溶液中放入铁片:
D.碳酸钙溶于硝酸:
11.在两份相同的溶液中,分别滴入物质的量浓度相等的、溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析不正确的是
A.①代表滴加溶液的变化曲线
B.b点,溶液中大量存在的离子是、
C.c点,两溶液中含有相同量的
D.a、d两点对应的溶液均显中性
12.某溶液中含有、、、、Na+、Ag+中的若干种,为确定该溶液的离子组成,进行如下实验∶
①取少量该溶液,向其中滴加 BaCl2溶液,产生白色沉淀
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体;白色沉淀部分溶解
③取②中上层清液继续滴加 BaCl2溶液至无沉淀时,再滴加 AgNO3溶液,产生白色沉淀根据上述实验,以下推测不正确的是
A.一定有B.一定有C.不能确定是否存在D.不能确定是否存在
13.某固体可能含有NH、Cu2+、Na+、Cl-、CO、SO中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生0.672L NH3(标准状况)。(已知:NH+ OH-=NH3+H2O)
下列说法正确的是
A.该固体中一定含有NH、CO、SO、Na+B.该固体中一定没有Cu2+、Cl-、Na+
C.该固体中只含有NH、CO、SO、Cl-D.根据以上实验,无法确定该固体中有Na+
14.甲、乙、丙、丁分别是溶液、溶液、溶液、盐酸中的一种,两两反应后产生的实验现象如下:甲+乙→沉淀,甲+丙→沉淀,乙+丙→沉淀,丙+丁→沉淀,乙+丁→无色无味气体。则甲、乙、丙、丁依次是( )
A.溶液、溶液、溶液、盐酸
B.溶液、溶液、盐酸、溶液
C.溶液、盐酸、溶液,溶液
D.溶液、盐酸、溶液、溶液
二、非选择题(共6小题)
15.有一包白色粉末状混合物,可能含有Na2CO3、NaCl、CaCO3、CuSO4、Na2SO4、MgCl2中的某几种,现进行如下实验:
①将混合物溶于水,得到无色透明溶液。
②取少量上述溶液两份,其中一份加入BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀不溶解,向另一份中加入NaOH溶液,也产生白色沉淀。
根据上述实验现象回答:
(1)原混合物中肯定没有___________。
(2)原混合物中肯定有___________。
(3)不能确定是否含有___________。
16.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________,有关的离子方程式为______________________。
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明液中肯定有_____________, 有关的离子方程式为____________________。
(4)原溶液可能大量存在的阴离子是下列的____________。
A.C1- B.NO C.CO D.OH-
17.现有S2-,SO,NH,Al3+,HPO,Na+,SO,AlO,Fe3+,HCO,Cl-,请按要求填空:
(1)在水溶液中,水解后溶液呈碱性的离子是___。
(2)在水溶液中,水解后溶液呈酸性的离子是___。
(3)既能在酸性较强的溶液中大量存在,又能在碱性较强的溶液中大量存在的离子有___。
(4)既不能在酸性较强的溶液中大量存在,又不能在碱性较强的溶液中大量存在的离子有___。
18.现有下列9种物质:①Na2CO3固体,②CO2固体,③Ca(OH)2固体,④NH4HCO3固体,⑤葡萄糖,⑥Al,⑦食盐水,⑧CH3COOH,⑨熔融氯化钾。
请回答下列问题:
(1)上述物质中属于电解质的是___________(填序号),属于非电解质的是___________ (填序号),能导电的是___________(填序号)。
(2)上述物质中①可用作洗涤剂,其原因是___________ ,写出其电离方程式:___________ 。
(3)下图为一定量③的饱和溶液中通人②气体后,溶液的导电能力与二氧化碳体积之间的关系曲线,由图___________。(填“能”或“不能”)确定B处生成的除水外的物质是电解质。在AB段曲线某一处,若通人的CO2的体积为3.36L(标准状况)时,写出反应的化学方程式:___________ ,得到沉淀的质量为___________g。
19.某溶液无色、澄清,对该溶液初步分析后发现其中可能含有、Na+、、H+、、中的若干种,然后又做了如下实验。
①用 pH 试纸测定溶液的酸碱性,结果 pH 试纸显红色。
②取2 mL溶液,加入 BaCl2溶液和稀盐酸,生成了白色沉淀。
③将②中所得的混合物充分静置后,取上层澄清的液体,加入 AgNO3溶液和稀硫酸,生成了白色沉淀。
(1)由上述实验可知,溶液中一定存在的离子是___________(填离子符号,下同),一定不存在的离子是___________。
(2)在上述实验操作中,有错误的步骤是(填序号)___________。正确的操作是(要作较详细的说明)___________。
(3)按(2)中改正实验操作后,仍生成白色沉淀,则还不能确定该溶液中是否存在的离子是___________。
20.对物质进行分类是学习化学的一种重要方法,科学合理的分类对于提高学习效率、解决问题都有着重要的意义。请回答下列问题。
有以下13种物质:①石墨 ②过氧化钠 ③蔗糖 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钠溶液⑧纯醋酸 ⑨氯化氢 ⑩硫酸铝⑪稀硫酸⑫氯化银⑬硫酸氢钠
(1)属于电解质的是___________(填序号,下同);属于非电解质的是___________;既不是电解质,也不是非电解质,但能导电的是___________ 。
(2)写出下列物质在水溶液中的电离方程式:
⑥___________;
⑩___________。
非电解质
电解质
酸
碱
盐
氧化物
A
氯气
氢氧化钠
二氧化碳
苏打
硫酸钠
水
B
酒精
食盐水
碳酸
纯碱
明矾
二氧化硅
C
二氧化碳
氯化钠
硫酸
火碱
小苏打
生石灰
D
酒精
铝
盐酸
熟石灰
石灰石
氧化铁
高中化学人教版 (2019)必修 第一册第四章 物质结构 元素周期律第三节 化学键优秀课时作业: 这是一份高中化学人教版 (2019)必修 第一册第四章 物质结构 元素周期律第三节 化学键优秀课时作业,文件包含43化学键综合训练2022-2023年化学必修第一册考点综合训练人教版2019解析版docx、43化学键综合训练2022-2023年化学必修第一册考点综合训练人教版2019原卷版docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
人教版 (2019)必修 第一册第四章 物质结构 元素周期律第三节 化学键精品练习: 这是一份人教版 (2019)必修 第一册第四章 物质结构 元素周期律第三节 化学键精品练习,文件包含43化学键分层解读2022-2023年化学必修第一册考点分层解读人教版2019解析版docx、43化学键分层解读2022-2023年化学必修第一册考点分层解读人教版2019原卷版docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 金属材料精品综合训练题: 这是一份高中化学人教版 (2019)必修 第一册第二节 金属材料精品综合训练题,文件包含课题32金属材料综合训练-2022-2023学年高一化学考点分层解读与综合训练人教版2019必修第一册解析版docx、课题32金属材料综合训练-2022-2023学年高一化学考点分层解读与综合训练人教版2019必修第一册原卷版docx等2份试卷配套教学资源,其中试卷共17页, 欢迎下载使用。













