- 2.2.1 氯及其化合物(第1课时)-2021-2022学年高一化学同步配套教案(人教版2019必修第一册) 教案 15 次下载
- 2.3.1 物质的量(第1课时)-2021-2022学年高一化学同步配套教案(人教版2019必修第一册) 教案 11 次下载
- 2.3.3 物质的量(第3课时)-2021-2022学年高一化学同步配套教案(人教版2019必修第一册) 教案 12 次下载
- 3.1 铁及其化合物-2021-2022学年高一化学同步配套教案(人教版2019必修第一册) 教案 14 次下载
- 3.2 金属材料-2021-2022学年高一化学同步配套教案(人教版2019必修第一册) 教案 10 次下载
人教版 (2019)必修 第一册第三节 物质的量第2课时教案及反思
展开
课题 | 第二章 海水中的重要元素——钠和氯 第三节 物质的量 第2课时 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教学目标 | 知识与技能 | 1、进一步巩固物质的量的概念及其与质量、摩尔质量、物质的量、物质的粒子数之间的相互关系 2、知道气体摩尔体积的概念,学会有关气体摩尔体积的简单计算逻辑思维能力 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
过程与方法 | 1、初步学会分析处理数据、推理演绎、归纳总结的科学学习方法 2、体验发现问题、分析问题、解决问题的探究性学习过程 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
情感态度 与价值观 | 通过理解并运用概念,培养严谨的科学态度,激发严谨务实、循序渐进、探索真理的科学态度,培养科学归纳的思维能力、空间想像能力和运用事物规律分析解决问题的 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教学 重点 | 气体摩尔体积的概念及其简单计算 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教学 难点 | 气体摩尔体积的概念及其简单计算 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教 学 设 想 | 教材分析 | 人教版高中化学必修1、第一章第二节“化学计量在实验中的应用”主要内容为“物质的量及其单位—摩尔”概念的建立;物质的量与物质微粒数量,阿佛加德罗常数之间的关系;物质的量与物质的质量,物质的摩尔质量之间关系;气体摩尔体积概念以及气体摩尔体积、气体体积、物质的量之间的关系;物质的量浓度概念以及相关计算 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
学情分析 | 学生在此之前已经学习过分子、原子、离子等微观粒子,对这些粒子有了基本的了解; 同时学生对宏观世界的物质质量、物质体积等内涵也有所了解;学生的这两项基本知识有利于建构微观和宏观之间的联系,有利于学生这节内容的学习。同时由于上节内容的讲解,学生对化学实验有了更进一步的认识,利于本节课学习过程中的实验探究。 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教法设计 |
“教无定法,贵在得法”。为了使学生顺利掌握教材,解决重难点,我采用了设问、类比、实验等综合性启发式教学方法去启迪学生思维,以力求落实“在体验中成长,在探究中发展”教学目标,同时,我还利用了板书、课件、观看实验视频的手段,增大课容量,增加学生的学习兴趣,调动学生的学习积极性。
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
教学环节 | 教 学 内 容
| 设计 意图 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 教师活动 | 学生活动 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
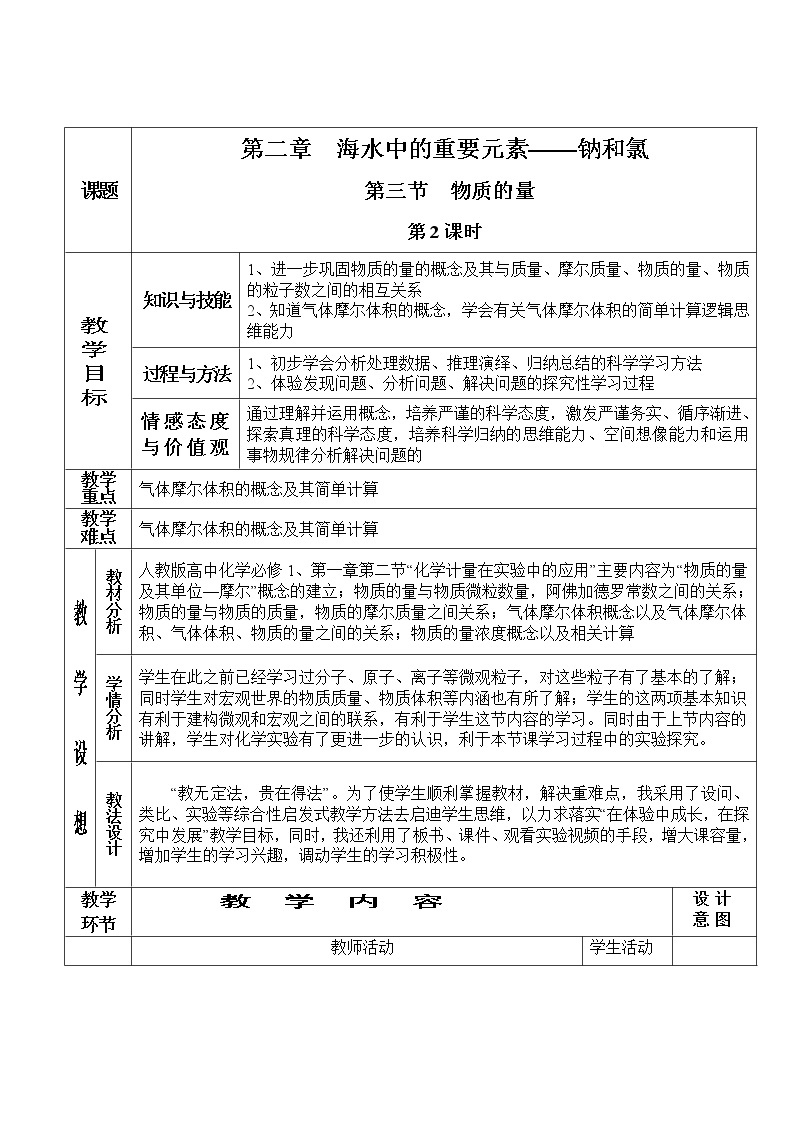
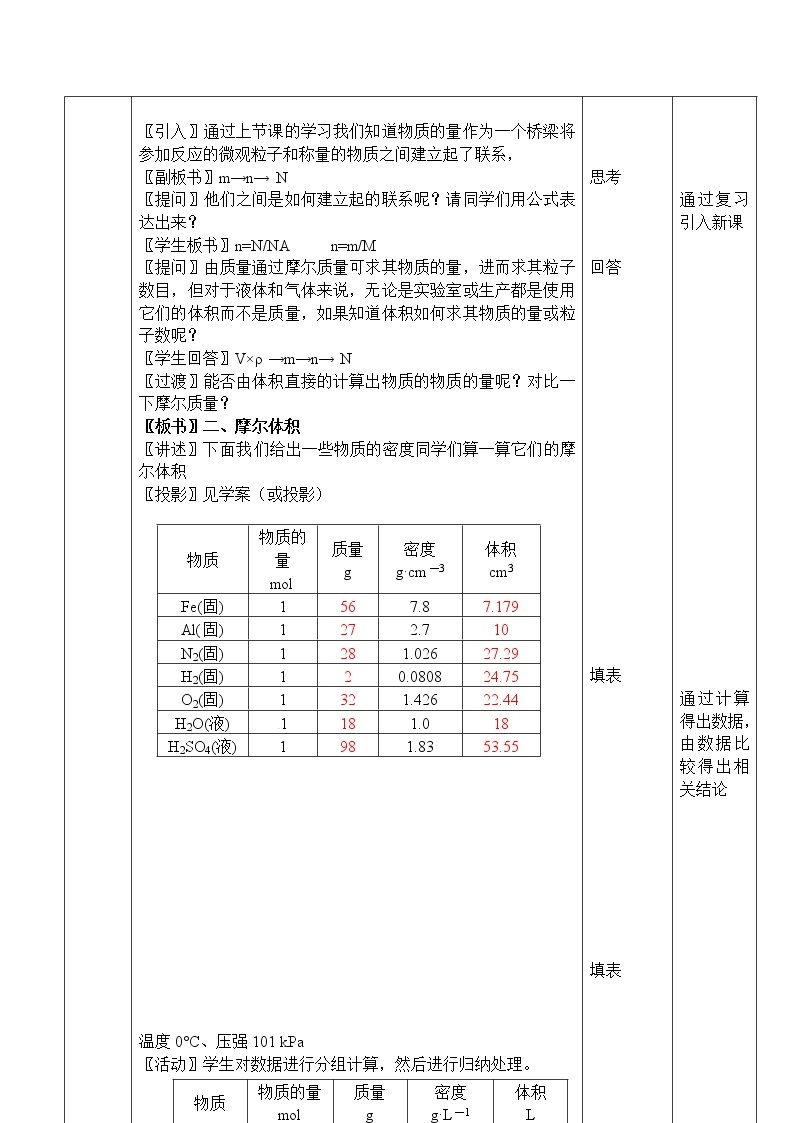
〖引入〗通过上节课的学习我们知道物质的量作为一个桥梁将参加反应的微观粒子和称量的物质之间建立起了联系, 〖副板书〗m→n→ N 〖提问〗他们之间是如何建立起的联系呢?请同学们用公式表达出来? 〖学生板书〗n=N/NA n=m/M 〖提问〗由质量通过摩尔质量可求其物质的量,进而求其粒子数目,但对于液体和气体来说,无论是实验室或生产都是使用它们的体积而不是质量,如果知道体积如何求其物质的量或粒子数呢? 〖学生回答〗V×ρ →m→n→ N 〖过渡〗能否由体积直接的计算出物质的物质的量呢?对比一下摩尔质量? 〖板书〗二、摩尔体积 〖讲述〗下面我们给出一些物质的密度同学们算一算它们的摩尔体积 〖投影〗见学案(或投影)
温度0°C、压强101 kPa
〖活动〗学生对数据进行分组计算,然后进行归纳处理。 〖小结〗数据处理的方法:先将数据有序排列,再将数据进行对比异同,观察规律。 |
思考
回答
填表
填表
|
通过复习引入新课
通过计算得出数据,由数据比较得出相关结论
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
〖学生总结〗在相同的条件下,1mol的液体和固体它们的体积不相同,而1mol的气体在相同的条件下条件下他们的体积都近视相等。在温度0°C、压强101 kPa它们的体积约为22.4升 〖讲述〗由于1mol不同的固态或液态物质的体积是不相同的。所以研究固体和液体的摩尔体积没有意义。而1mol不同的气体的体积相差不大,都接近22.4L。因此研究气体的摩尔体积有一定的意义。 〖板书〗气体 〖提问〗气体摩尔体积受哪些外在条件的影响呢? 〖板书〗1、影响因素:T P 〖讲解〗 气体的体积受温度、压强的影响很大,因此,说到气体的体积时,必须指明外界条件,否则就没有意义。如果将单位物质的量的气体所占的体积称为气体摩尔体积,用Vm表示,单位为L/mol,那么在一定温度和压强下,Vm是个常数,如果条件变化了,则Vm亦随之改变。如在0℃、101 kPa时,Vm=22.4 L/mol;在25℃、101 kPa时,Vm=24.8 L/mol。 〖板书〗2、0℃、101 kPa时,Vm=22.4 L/mol 〖思考〗根据摩尔质量的定义请同学们归纳一下气体摩尔体积的公式: 〖板书〗3、V= n•Vm 〖过渡〗刚才我们讨论了气体,现在我们讨论一下液体。 〖讲述〗在生产和科学实验中,我们经常使用溶液,为了表明溶液中溶质和溶剂之间量的关系,需要使用表示溶液组成的物理量,我们学过的表示溶液组成的物理量有哪些? 〖回答〗质量分数、溶解度、饱和溶液、不饱和溶液等。 〖过渡〗我们在初中学习过溶液中溶质的质量分数,应用这种表示溶液浓度的方法,可以计算一定质量的溶液中所含溶质的质量。但是,很多化学反应都在溶液中进行,对于溶液我们通常不称其质量,而是量它的体积。同时,在化学反应中,各物质之间的物质的量的关系要比他们之间的质量关系简单明了的多。 〖举例〗 NaOH + HCl = NaCl + H2O 质量关系40g 36.5g 58.5g 18g 物质的量关系1 mol 1mol 1 mol 1mol 〖讲述〗对于溶液,量取体积要比称量质量更易操作。能不能通过量取一定体积的溶液就知道其中含有多少摩尔溶质呢?我们在这节课学习一种常用的表示溶液组成的物理量--------物质的量浓度 |
小结
认真听讲
识记
回顾初中学所知识 |
通过问题引出要研究的知识,逐步深入,有利于学生更好的理解和掌握知识
利用初中所学表示溶液组成的物理量——质量分数导出物质的量浓度 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
〖板书〗三、物质的量在化学实验中的作用 〖板书〗1、物质的量浓度 A、定义:单位体积溶液中所含溶质B的物质的量,又叫B的物质的量浓度,符号cB , 〖提问〗根据物质的量浓度的定义,物质的量浓度的公式应怎样表达呢? 〖板书〗B、cB=nB/V ,单位通常是用mol/L表示。 〖阅读〗P14相关内容 〖强调〗1、溶液体积为1升,而不是溶剂体积是1升; 2、溶质是用物质的量表示,而不是用摩尔质量表示。 例题:1、配置500ml 0.1 mol/l NaOH需要NaOH的质量是多少? 解:n(NaOH)= c(NaOH)·V[NaOH(aq)] = 0.1mo/l×0.5L = 0.05mol m(NaOH)== n(NaOH)·M(NaOH) ==0.05 mol×40g/mol =2g
|
学习新知
计算
|
根据所学理论知进行解题,达到知识的理解与掌和握
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
作业设计 |
导学案相应习题 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
板
书
设
计 |
一、气体摩尔体积 1、定义:单位物质的量的气体所占的体积 2、表示符号:Vm 3、公式: 4、单位:L/mol 或L ·mol-1 5、特定条件下的气体摩尔体积:标准状况下,Vm = 22.4L/mol 二、物质的量浓度 1、定义:用单位体积溶液中所含溶质B的物质的量来表示溶液组成的物理量 2、表示符号:cB 3、公式: 4、单位: mol/L 或mol·L -1
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表第2课时教学设计: 这是一份高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表第2课时教学设计,共8页。教案主要包含了复习提问,组织讨论,指导实验,实验小结,启发设问,提供信息,引导归纳,给出信息等内容,欢迎下载使用。
2020-2021学年第三节 化学键第2课时教案: 这是一份2020-2021学年第三节 化学键第2课时教案,共9页。
高中化学人教版 (2019)必修 第一册第三节 化学键第1课时教学设计及反思: 这是一份高中化学人教版 (2019)必修 第一册第三节 化学键第1课时教学设计及反思,共6页。教案主要包含了引入新课,新课教学,离子化合物等内容,欢迎下载使用。