





人教版 (2019)必修 第一册第三节 物质的量多媒体教学课件ppt
展开1.你知道古代曹冲称象的故事吗?曹冲在称象时的主导思想是什么?
2.已知托盘天平的最小刻度为0.1克,你能用它称量一粒大米的质量吗?你的主导思想又是什么?
微观: 1个碳原子 1个氧分子 1个二氧化碳分子
宏观: 12克炭 32克氧气 44克二氧化碳
任务一:感受宏观辨识与微观探析
从宏观上看,发生化学反应的物质之间是按照一定的质量关系进行的,物质是可称量的。从微观上看,化学反应是微观粒子按一定的数目关系进行的,而微观粒子是难以称量的。那么,对化学反应进行定量研究时,能否将可称量的物质与难以称量的微观粒子之间联系起来呢?为此,国际上采用了一个新的物理量一物质的量
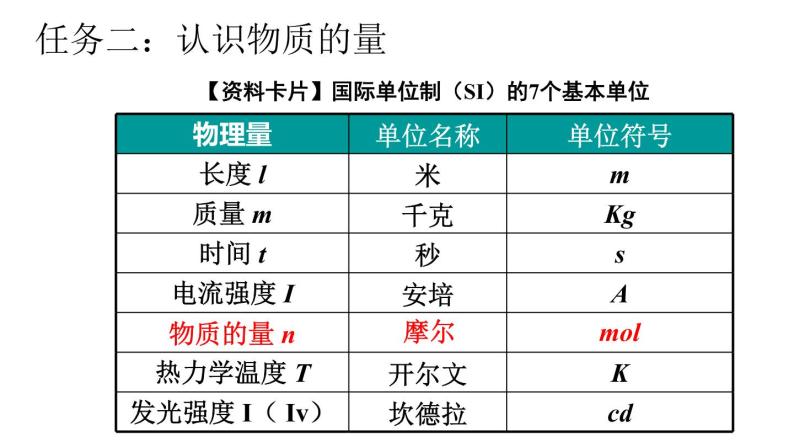
【资料卡片】国际单位制(SI)的7个基本单位
用0.012 kg 12C所含的碳原子数作为1ml的标准。
1ml的标准是什么?(既1ml某种微粒集合体表示的粒子数目的依据是什么?)
千克是质量的单位,规定: 1000立方厘米的纯水在4℃时的质量为1千克
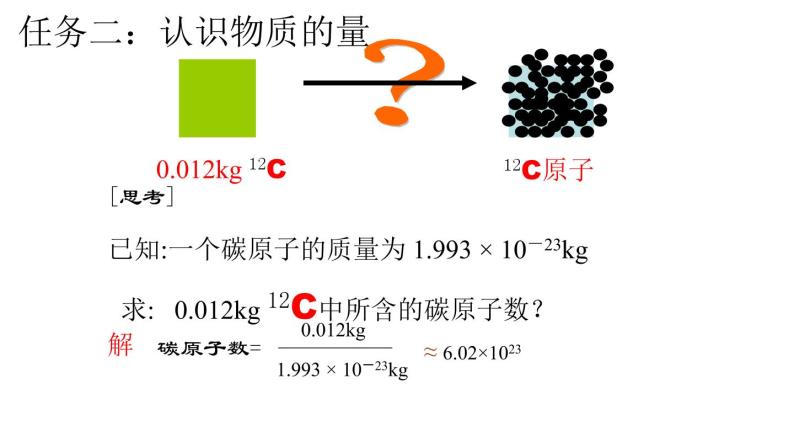
已知:一个碳原子的质量为 1.993 × 10-23kg 求: 0.012kg 12C中所含的碳原子数?
1.993 × 10-23kg
≈ 6.02×1023
生平简介 意大利物理学家。1776年8月9日生于都灵市一个律师家庭,1856年7月9日卒于都灵市。1792年进都灵大学法律系学习,取得法学博士学位后,曾开业当律师。1800年弃法从理,十分勤奋,1820年被聘任都灵大学理科教授。自 18年被选为都灵科学院院士后,还担任过意大利教育委员和度量衡学会会长.
表示含有一定数目粒子的集合体的物理量
(2)单位: 摩尔(ml)
(3)标准: 阿伏伽德罗常数(NA),约6.02×1023
【注意】NA是一个精确值(=0.012Kg 12C中所含的碳原子数) NA≈6.02×1023ml-1 (近似值)
微观粒子(分子、原子、离子、原子团、电子、中子、质子等)
① “物质的量” 是一个专有名词,不能分割
②物质的量和摩尔只能描述微观粒子,不能描述宏观物质
③用ml表示物质时,必须指明微粒的具体种类,一般用化学式表示
物质的量的理解——“四化”
①摩尔是七个基本物理量之一 ( )②1ml氢约含6.02×1023个氢原子 ( )③摩尔是物质的数量单位 ( )④NA就是6.02×1023ml-1 ( )⑤1mlH的数目约为6.02×1023 个 ( )⑥1ml大米的数目约为6.02×1023 个 ( )
【小试牛刀】判断下列说法是否正确?
1 ml任何粒子的粒子数
约6.02×1023 ml-1
3.物质的量n、阿伏加德罗常数NA、微粒数目N之间的关系
物质的量n(ml) 微粒数目N(个)
【再来一刀】(1)1ml H2所含氢气分子的个数约为 个。(2)2ml H2O约含 个氢原子。(3)1ml SO42—可表示有 NA 个SO42—;所带的电荷数为 NA,约为 个。 (4)2ml CO2中含有 ml C和 ml O,含有 个CO2分子。(5) ml H2O中含有的氧原子数与1.5ml CO2中含有的氧原子数相同
1.204×1024
【再来一刀】通过下图可进一步认识水的组成,请完成图中空格。
学习任务三:证据推理与模型认知
结论:1 ml任何物质的质量,若以克为单位,在数值上与该物质的相对原子质量,或相对分子质量相等。
单位物质的量(1ml)的物质所具有的质量,符号M,单位:g/ml、或g·ml-1
3.M 数值=相对原子(分子)质量
4.相对质量、1ml粒子的质量、摩尔质量三者的关系:
推算1ml的下列各种粒子的质量
1ml Fe 1ml O21ml Na 1ml Na+1ml NH4+ 1ml SO42-
相对原子质量相对分子质量
相同
数值相同,单位不同,意义不同
相对原子质量:Fe:56 O:16 H:1①铁的摩尔质量是 __,即1ml铁的质量是___ ; 28g铁中含有 __ml铁原子。② 水的相对分子质量是___,摩尔质量是______;2ml的水是 克;90g水是 ml
1、24.5克硫酸的物质的量是 ml;
2、1.5ml 硫酸的质量是 ,其中含有 ml O ,其质量是 克;
3、0.01 ml 某物质的质量是1.08克,此物质的摩尔质量为 ;
4、71克Na2SO4中含Na+ ml, 含SO42- 个.
宏观: 12克炭 32克氧气 44克二氧化碳
1ml 1ml 1ml
1NA 1NA 1NA
1.下列对于“摩尔”的理解正确的是( ) A.摩尔是国际科学界建议采用的一种物理量 B.摩尔是物质的量的单位,简称摩,符号为ml C.摩尔可以把物质的宏观数量与微观粒子的数量 联系起来 D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
2.下列说法正确的是( ) A.摩尔质量就等于物质的质量 B.摩尔质量就是物质相对分子质量的6.02×1023倍 C.HNO3的摩尔质量是63g D.硫酸和磷酸的摩尔质量相等
3.0.5mlNa2SO4中所含的Na+数目约为( ) A.3.01×1023 B.6.02×1023 C.0.5 D.14.下列气体中所含分子数目最多的是( ) A .1gH2 B.11gCO2 D.17g NH3
化学必修 第一册第三节 物质的量教课内容课件ppt: 这是一份化学必修 第一册第三节 物质的量教课内容课件ppt,共26页。PPT课件主要包含了物质的量,交流与讨论,感受阿伏加德罗常数,mol的质量,归纳总结等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 物质的量课文ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量课文ppt课件,共17页。PPT课件主要包含了课前回顾,物质的量,相互转化,符号Vm,单位Lmol,阿伏加德罗定律,推论2,推论3,①③④,练习巩固等内容,欢迎下载使用。
化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教案配套ppt课件: 这是一份化学必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教案配套ppt课件,共24页。PPT课件主要包含了物质的量浓度,容量瓶简介等内容,欢迎下载使用。













