沪教版九年级上册第3节 物质的组成第3课时教案
展开第3节 物质组成的化学式
第3课时
一、教学目标
1.掌握某物质的相对分子质量、各元素的质量比及某元素的质量分数的计算方法。
2.能看懂某些商品标签或说明书上标识的物质成分和含量。
二、教学重难点
重点:元素的质量比和某元素质量分数的计算。
难点:元素质量分数的计算。
三、教学准备
多媒体课件。
四、教学过程
教学环节 | 教师活动 | 学生活动 | 设计意图 |
环节一 创设情境 引入新课 | 【展示】展示图片。 【讲述】农业人员在研究氮肥的肥效时首先必须知道所施氮肥的含氮量;化工生产中某些产品质量的分析,也要设法测出其中某种元素的含量。在这些实践活动中,人们常常根据物质化学式来确定组成物质元素之间的质量关系。 【提问】化学式能告诉我们这些信息吗? |
倾听
思考
| 用农业生产中的实例引入课程,让学生理解化学与生产、生活的关系,感受学习化学相关计算的重要性。 |
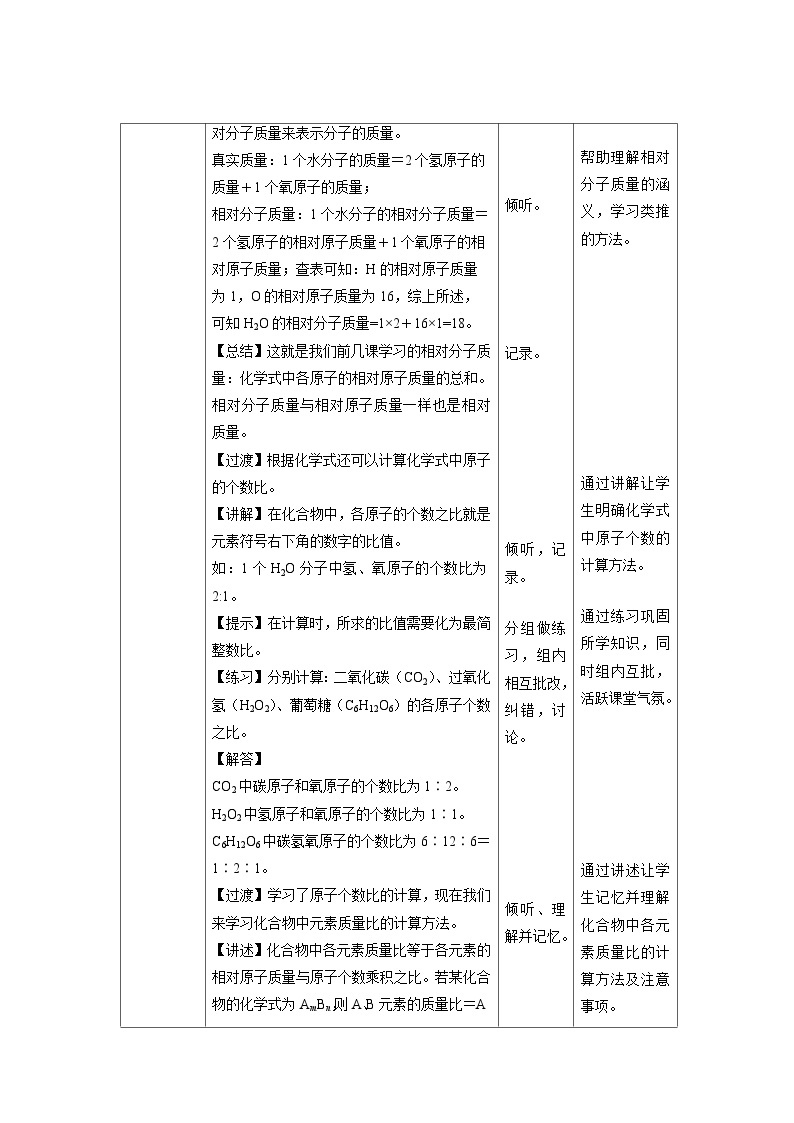
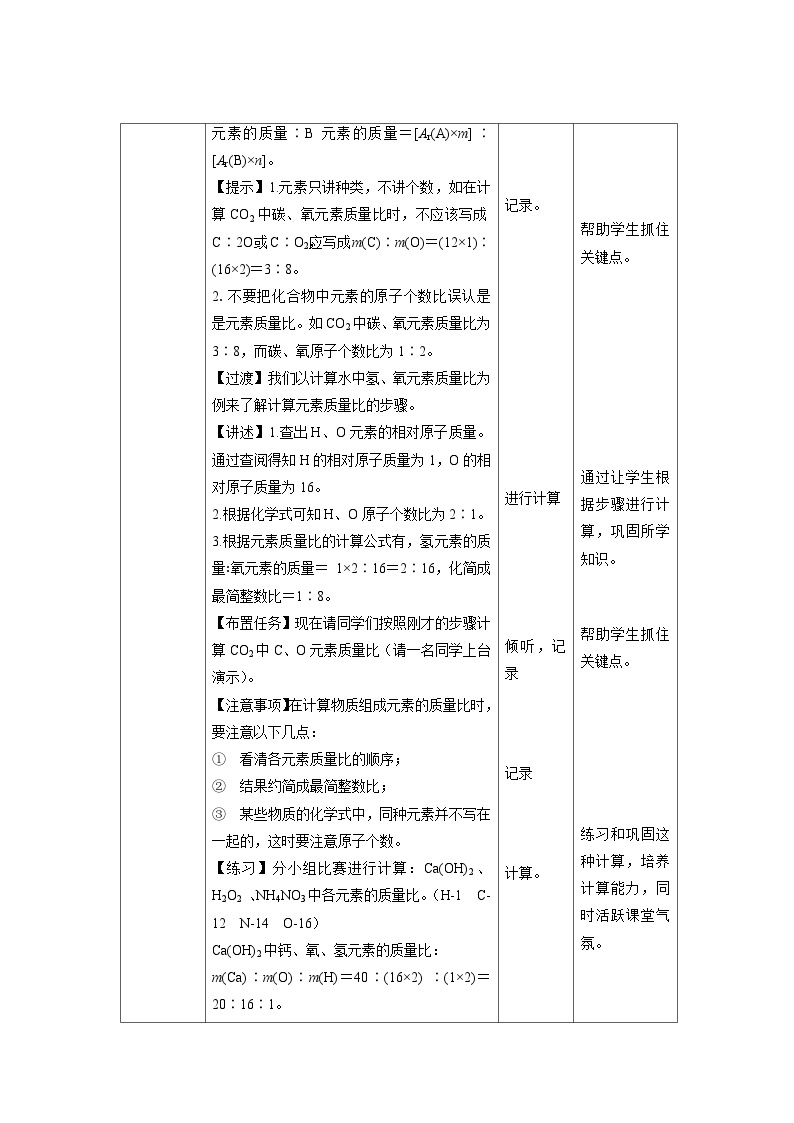
环节二 新课讲解 | 一、计算某物质中元素的质量比 【过渡】在学习新知识之前,我们以水为例先来复习一下相对分子质量的计算。 【讲述】通过水的化学式“H2O”我们知道,水是由氢元素和氧元素组成的,且一个水分子中,含有2个氢原子和1个氧原子,那么你能根据化学式计算出水分子的质量吗?化学式能告诉我们有关组成元素之间的质量关系的信息吗? 【讲解】在化学上,人们用相对原子质量来表示原子的质量,依次类推,人们采用了相对分子质量来表示分子的质量。 真实质量:1个水分子的质量=2个氢原子的质量+1个氧原子的质量; 相对分子质量:1个水分子的相对分子质量=2个氢原子的相对原子质量+1个氧原子的相对原子质量;查表可知:H的相对原子质量为1,O的相对原子质量为16,综上所述,可知H2O的相对分子质量=1×2+16×1=18。 【总结】这就是我们前几课学习的相对分子质量:化学式中各原子的相对原子质量的总和。相对分子质量与相对原子质量一样也是相对质量。 【过渡】根据化学式还可以计算化学式中原子的个数比。 【讲解】在化合物中,各原子的个数之比就是元素符号右下角的数字的比值。 如:1个H2O分子中氢、氧原子的个数比为2:1。 【提示】在计算时,所求的比值需要化为最简整数比。 【练习】分别计算:二氧化碳(CO2)、过氧化氢(H2O2)、葡萄糖(C6H12O6)的各原子个数之比。 【解答】 CO2中碳原子和氧原子的个数比为1∶2。 H2O2中氢原子和氧原子的个数比为1∶1。 C6H12O6中碳、氢、氧原子的个数比为6∶12∶6=1∶2∶1。 【过渡】学习了原子个数比的计算,现在我们来学习化合物中元素质量比的计算方法。 【讲述】化合物中各元素质量比等于各元素的相对原子质量与原子个数乘积之比。若某化合物的化学式为AmBn,则A、B元素的质量比=A元素的质量∶B元素的质量=[Ar(A)×m]∶ [Ar(B)×n]。 【提示】1.元素只讲种类,不讲个数,如在计算CO2中碳、氧元素质量比时,不应该写成C∶2O或C∶O2,应写成m(C)∶m(O)=(12×1)∶(16×2)=3∶8。 2.不要把化合物中元素的原子个数比误认是是元素质量比。如CO2中碳、氧元素质量比为3∶8,而碳、氧原子个数比为1∶2。 【过渡】我们以计算水中氢、氧元素质量比为例来了解计算元素质量比的步骤。 【讲述】1.查出H、O元素的相对原子质量。通过查阅得知H的相对原子质量为1,O的相对原子质量为16。 2.根据化学式可知H、O原子个数比为2∶1。 3.根据元素质量比的计算公式有,氢元素的质量∶氧元素的质量= 1×2∶16=2∶16,化简成最简整数比=1∶8。 【布置任务】现在请同学们按照刚才的步骤计算CO2中C、O元素质量比(请一名同学上台演示)。 【注意事项】在计算物质组成元素的质量比时,要注意以下几点: ① 看清各元素质量比的顺序; ② 结果约简成最简整数比; ③ 某些物质的化学式中,同种元素并不写在一起的,这时要注意原子个数。 【练习】分小组比赛进行计算:Ca(OH)2、H2O2 、NH4NO3中各元素的质量比。(H-1 C-12 N-14 O-16) Ca(OH)2中钙、氧、氢元素的质量比: m(Ca)∶m(O)∶m(H)=40∶(16×2) ∶(1×2)=20∶16∶1。 H2O2中氢、氧元素的质量比: m(O)∶m(H) =(1×2)∶(16×2)=1∶16 NH4NO3中氮、氢、氧元素的质量比 m(N)∶m(H)∶m(O)=(14×2) ∶(1×4)∶(16×3) =7∶1∶12。 |
倾听。
思考。
倾听。
倾听。
记录。
倾听,记录。
分组做练习,组内相互批改,纠错,讨论。
倾听、理解并记忆。
记录。
进行计算
倾听,记录
记录
计算。
| 通过复习相对分子质量的计算,为后续计算元素质量比打下基础。
帮助理解相对分子质量的涵义,学习类推的方法。
通过讲解让学生明确化学式中原子个数的计算方法。
通过练习巩固所学知识,同时组内互批,活跃课堂气氛。
通过讲述让学生记忆并理解化合物中各元素质量比的计算方法及注意事项。
帮助学生抓住关键点。
通过让学生根据步骤进行计算,巩固所学知识。
帮助学生抓住关键点。
练习和巩固这种计算,培养计算能力,同时活跃课堂气氛。
|
二、计算物质中某元素的质量分数 【过渡】根据化学式不但可以求出元素质量比,还能求出物质中的元素质量分数。 【讲解】某元素的质量分数(ω),就是该元素的质量与组成物质的元素总质量之比乘以百分之百,可根据化学式计算。 即: 如:计算Fe2O3中铁元素的质量分数。 步骤1.查出Fe、O的相对原子质量。 步骤2:Fe2O3中的相对分子质量=56×2+16×3 =160。 步骤3:Fe2O3中的铁的质量分数 【过渡】百闻不如一见,百见不如一练。下面请同学们完成PPT上的练习。 【展示】展示PPT中的练习。 【总结】通过计算,我们得出的结果是36 水中氢元素的质量是4 g,氧元素的质量是32 g。 【过渡】在课程的刚开始,我们提到了农业人员在研究氮肥的肥效时首先必须知道所施氮肥的含氮量;化工生产中某些产品质量的分析,也要设法测出其中某种元素的含量。同理,通过元素含量计算,我们也能推断化肥样品是纯净物还是混合物。 【布置任务】请同学们完成下面这个题,分析该化肥样品是纯净物还是混合物? 农业人员在研究氮肥的肥效时首先必须知道所施氮肥的含氮量;化工生产中某些产品质量的分析,也要设法测出其中某种元素的含量。在这些实践活动中,人们常常根据物质化学式来确定组成物质元素之间的质量关系。(可请一名同学到黑板) 【总结】通过计算我们发现该样品为混合物。 【过渡】除了可以根据化学式计算某物质中的元素质量分数,还可以计算一定质量的物质中某元素的质量。 【讲述】一定量某物质中某元素的质量=物质质量×该元素的质量分数。例如下面这道习题: 已知硝酸铵中氮元素的质量分数为35%,60 gNH4NO3中含有的氮的质量。 氮元素的质量= NH4NO3的质量×氮元素的质量分数= 60 g×35%= 21 g。 【布置任务】生活中处处有化学,药品、食品等商品的标签或说明书上常常用质量分数来表示物质的成分或纯度,请同学们根据收集来的说明书对药品、食品的有关情况做记录。 |
倾听、理解并记忆元素质量分数的计算公式。
倾听、理解并记忆。
计算,并得出结论。
倾听、理解并记忆。
完成任务。
|
通过讲述让学生明确元素质量分数的计算公式。
通过讲解让学生明确某元素质量分数的计算公式。
通过让学生计算,既可巩固化学式相关计算知识,又可向学生渗透化学与生产、生活之间紧密相关。
通过讲述让学生记忆并理解一定量某物质中某元素质量的计算方法。
培养学生学以致用的能力。
| |
拓展延伸 | PPT展示我国科学家屠呦呦的故事。 | 阅读 | 通过展示我国科学家屠呦呦发现青蒿素的事迹,激发学生爱国主义情怀。 |
随堂作业 | PPT展示。 | 做题 | 通过习题巩固本节所学知识 |
环节四 课堂小结 | 展示PPT21页。 | 倾听并理解。 | 帮助学生梳理本节知识,便于学生记忆。 |
五、板书设计
第3节 物质的组成
第3课时
一、计算化合物中各元素质量比
二、计算化合物中某元素的质量分数
1.质量分数
2.根据化学式计算化合物中某元素的质量分数
3.有关化学式计算的其他公式
初中化学沪教版九年级上册第3节 物质的组成第2课时教案设计: 这是一份初中化学沪教版九年级上册第3节 物质的组成第2课时教案设计,共6页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。
沪教版九年级上册第3节 物质的组成第1课时教案及反思: 这是一份沪教版九年级上册第3节 物质的组成第1课时教案及反思,共7页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。
初中化学沪教版九年级上册第1节 构成物质的基本微粒第3课时教案设计: 这是一份初中化学沪教版九年级上册第1节 构成物质的基本微粒第3课时教案设计,共8页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。