



高中化学人教版 (2019)必修 第一册第二节 元素周期律优质课课件ppt
展开练习2、下列说法不能作为比较卤族元素非金属强弱的依据的是( )A、F2、Cl2、Br2、I2跟氢气反应的激烈程度逐渐减弱B、HF、HCl、HBr、HI的热稳定性依次减弱C、F-、Cl-、Br -、I-的还原性依次增强D、HF、HCl、HBr、HI水溶液的酸性依次增强
练习3、不能说明氯的非金属强于溴的非金属的事实是( )A、HClO4的酸性强于HBrO4B、HBr的分解温度低于HCl的分解温度C、BrCl中氯的为-1价D、FeBr2溶液中滴加少量的氯水,溶液变黄
练习4、下列叙述中正确的是( ) A.随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现 B.随着元素原子序数的递增,同周期从左到右原子半径从小到大 (稀有气体元素除外)发生周期性的变化 C.随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价 从-7到-1重复出现 D.元素原子核外电子排布的周期性变化是导致原子半径、元素的主要 化合价变化的主要原因
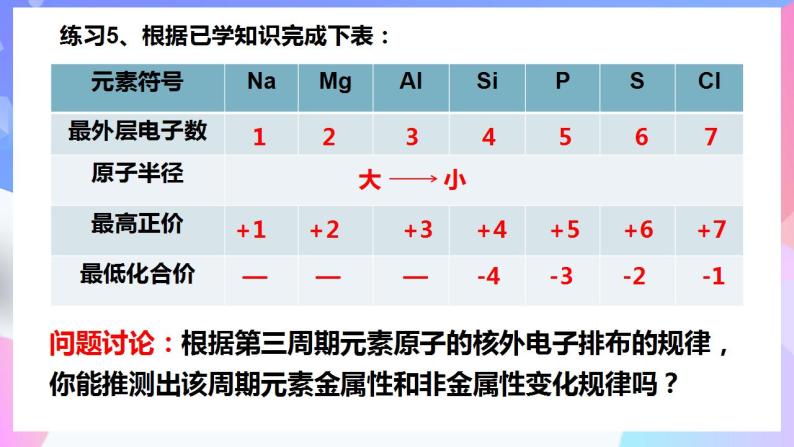
练习5、根据已学知识完成下表:
1 2 3 4 5 6 7
+1 +2 +3 +4 +5 +6 +7
— — — -4 -3 -2 -1
问题讨论:根据第三周期元素原子的核外电子排布的规律,你能推测出该周期元素金属性和非金属性变化规律吗?
人教版 高中化学必修一 第一册
第四章 物质结构 元素周期律
第二节 元素周期律 (第二课时)
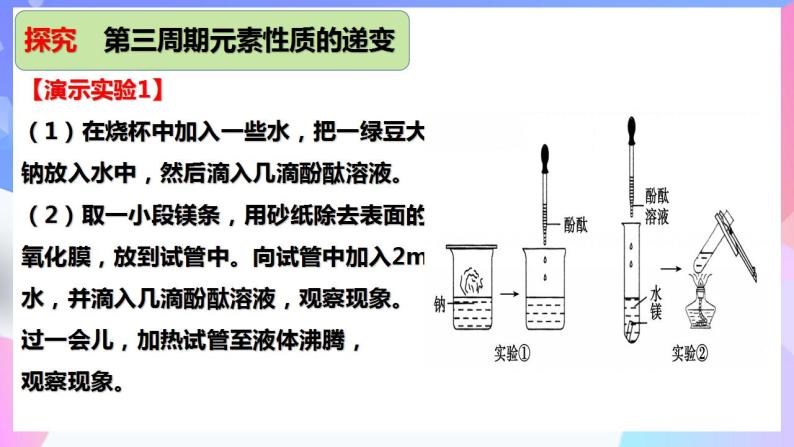
探究 第三周期元素性质的递变
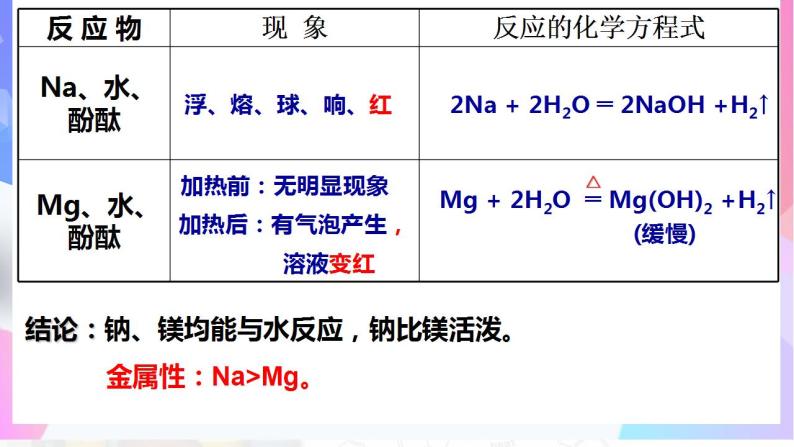
加热前:无明显现象加热后:有气泡产生, 溶液变红
2Na + 2H2O ═ 2NaOH +H2↑
结论:钠、镁均能与水反应,钠比镁活泼。 金属性:Na>Mg。
【演示实验2】 取一段镁条,用砂纸除去表面的氧化膜,卷成螺旋状,插入盛有食盐水的试管中。再将试管倒插盛有食盐水的烧杯中,观察现象。
现象:镁条表面不断有气泡产生。
【演示实验3】 取一段镁条和一小片铝片,用砂纸除去表面的氧化膜,分别与等体积、等浓度的盐酸反应,观察现象。
现象:镁与盐酸反应产生氢气的速率比铝快
结论:金属性 镁>铝
【演示实验4】(1)向试管中加入2ml1ml/LAlCl3溶液,然后滴加氨水,直到不再产生白色絮状Al(OH)3沉淀为止。将Al(OH)3沉淀分装在两支试管中,向一支试管中滴加2ml/L盐酸,向另一支试管中滴加2ml/LNaOH溶液。边加边振荡,观察现象。
【演示实验4】(2)用2ml 1ml/LMgCl2溶液代替AlCl3溶液做上述实验,观察现象,并进行比较。
【信息获取】钠、镁、铝的最高价氧化物对应的水化物的碱性
两性氢氧化物:既能与酸反应生成盐和水,又能与碱反应生成盐和水的氢氧化物。Al(OH)3+3H+ = Al 3++3H2O Al(OH)3+OH- = AlO2-+2H2O这说明铝虽是金属,但已表现出非金属性。
NaOH>Mg(OH)2>Al(OH)3
金属性:Na>Mg>Al
H2SiO3
【信息获取】Si 、P、S 、Cl 的最高价氧化物对应的水化物的酸性及与氢气反应的情况如下表:
1、第三周期元素金属性、非金属性的递变规律:
Na Mg Al Si P S Cl
金属性逐渐 ,非金属性逐渐 。
对其他周期主族元素进行同样的研究,一般情况下也会得到类似的结论。
原子失电子的能力逐渐_ ___,得电子的能力逐渐__
从左到右,核电荷数依次 原子半径逐渐_____
元素的金属性逐渐_____,元素的非金属性逐渐_____。
2、用结构观点解释同周期主族元素的变化规律
(1)内容:元素的性质随着原子序数的递增而呈周期性的变化。
(2)实质:元素性质的周期性变化是元素原子的核外电子排布 的周期性变化的必然结果。
练习1、下列能说明氯元素的非金属性比硫元素的强的有几项( )①HCl比H2S稳定 ②HClO的氧化性比H2SO4强 ③沸点:H2S>HCl ④S2Cl2中Cl元素为-1价 ⑤Cl原子最外层有7个电子,S原子最外层有6个电子⑥Cl2与Fe反应生成FeCl3,S与Fe生成FeS ⑦HCl的酸性比H2S的酸性强⑧Cl2能与H2S反应生成S A. 7项 B. 6项 C. 5项 D. 4项
人教版 高中化学必修一第一册 第四章 第二节
练习2、运用元素周期律分析,下列推断中错误的是( ) A. 已知Ra是第七周期第IIA族元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强B. 已知As是第四周期第VA元素,故AsH3的稳定性比NH3的稳定性弱C. 已知Cs是第六周期第ΙA族元素,原子半径比Na的原子半径大,故Cs与 水反应比Na与水反应剧烈 D. 已知Cl的非金属性比S强,故HClO2的酸性比H2SO4的强
练习3、X、Y两元素是同周期的非金属主族元素,如果X原子半径比Y的大,下面说法正确的是 ( )A.最高价氧化物对应水化物的酸性,X的比Y的强B.X的非金属性比Y的强C.X的阴离子比Y的阴离子还原性强D.X的气态氢化物比Y的稳定
练习4、X、Y、Z三种元素的电子层数相同,它们的最高价氧化物分别为酸性氧化物、碱性氧化物和两性氧化物,则三种元素的原子序数的大小顺序是 ( )A.X>Y>ZB.Y>Z>X C.X>Z>YD.Z>X>Y
高中化学人教版 (2019)必修 第一册第二节 元素周期律优秀ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 元素周期律优秀ppt课件,共33页。PPT课件主要包含了内容索引,学习目标,活动方案,Si<P<S<Cl,GaAs,课堂反馈,Mg+2H2O,第三周期第ⅠA族等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二节 元素周期律评优课复习课件ppt: 这是一份人教版 (2019)必修 第一册第二节 元素周期律评优课复习课件ppt,共19页。PPT课件主要包含了原子结构,元素周期表,元素周期律,化学键,第五周期ⅦA族等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 元素周期律授课课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第二节 元素周期律授课课件ppt,共34页。PPT课件主要包含了知识回顾,原子结构分析,核电荷数,性质分析,周期性,原子半径,微粒半径大小,与冷水反应剧烈,中强碱,两性氢氧化物等内容,欢迎下载使用。













