




- 6.1.1 化学反应与热能(精品课件)) 课件 27 次下载
- 6.1.2 化学反应与电能(精品课件) 课件 25 次下载
- 6.2.1 化学反应速率(精品课件) 课件 28 次下载
- 6.2.2 探究影响化学反应速率的因素(精品课件) 课件 29 次下载
- 6.2.3 化学反应的限度(精品课件) 课件 27 次下载
高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化教课ppt课件
展开①自发进行的氧化还原反应,设置在两个不同的区域
②合适的电极材料和电解质
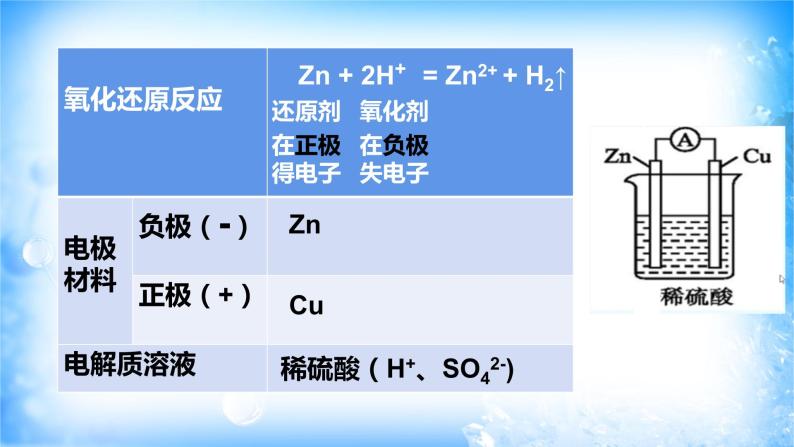
Zn + 2H+ = Zn2+ + H2↑
稀硫酸(H+、SO42-)
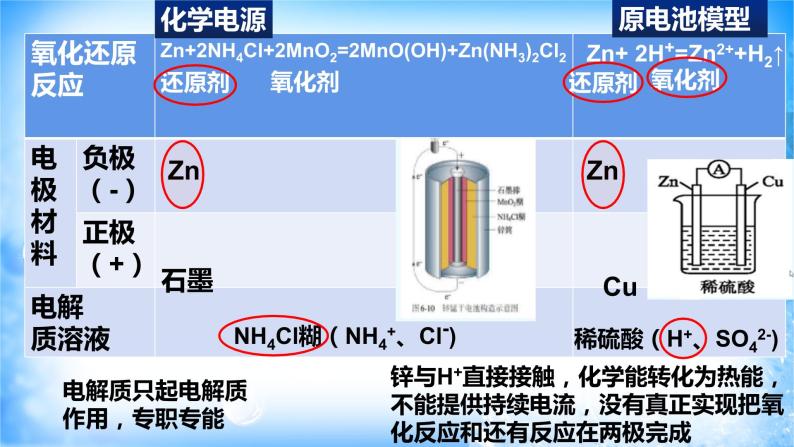
Zn+2NH4Cl+2MnO2=2MnO(OH)+Zn(NH3)2Cl2
NH4Cl糊(NH4+、Cl-)
Zn+ 2H+=Zn2++H2↑
比较两种电池,负极材料和电解质溶液所起的作用有何异同?
锌与H+直接接触,化学能转化为热能,不能提供持续电流,没有真正实现把氧化反应和还有反应在两极完成
电解质只起电解质作用,专职专能
2H2 + O2 = H2O
多孔可以增大接触面积,铂起催化剂作用
写出H2SO4为电解质溶液的氢氧燃料电池的总反应式和电极反应式
写出KOH为电解质溶液的氢氧燃料电池的总反应式和电极反应式
总反应: 2H2+ O2 =2H2O
O2 + 4e- + 4H+ =2H2O
O2 +4e- +2H2O =4OH-
H2 -2e- =2H+
2H2 -4e- =4H+
H2 -2e- +2OH- =2H2O
2H2 -4e- +4OH- =4H2O
CH4 +10OH- -8e- = CO32-+7H2O
CH4 + 2O2 +2OH- =3H2O+ CO32-
2O2+8e-+4H2O = 8OH-
写出甲烷燃料电池(CH4-O2-KOH溶液)的电极反应式
书写燃料电池电极反应式注意事项
2.负极失电子所得氧化产物和正极得电子所得还原产物,与溶液的酸碱性有关(如+4价的C在酸性溶液中以CO2形式存在,在碱性溶液中以CO32-形式存在);
1.将两极反应的电子得失数配平后,相加得到总反应,总反应减去一极反应即得到另一极反应;
3.水溶液中不存在O2-:在酸性溶液中它与H+结合成H2O、在碱性或中性溶液中它与水结合成OH-;
负极: Pb - 2e- +SO42- = PbSO4↓
正极:PbO2+4H++ SO42- +2e-=PbSO4↓+2H2O
总反应:PbO2+ Pb+2H2SO4=2PbSO4↓+2H2O
负极:Li - e- = Li+
常用于电脑笔记本、手机、照相机、 心脏起博器、火箭、导弹等的动力电源。
正极:MnO2 + e- = MnO2-
总反应式:Li + MnO2 = LiMnO2
锂亚硫酰氯电池(Li-SOCl2):8Li+3SOCl2=6LiCl+Li2SO3+2S
负极: 。
正极: 。
8Li-8e-=8Li+
3SOCl2+8e- = 6Cl- +2S+SO32-
优点:质轻、比能量高、高工作效率、高稳定电压、工作温度宽、高使用寿命,广泛应用于军事和航空领域。
锂电池(非水有机溶剂电解液)
1. 1991年,我国首创铝-空气-海水电池,用作海上标志灯。以海水为电解液,靠空气中的氧使铝不断氧化而产生电流。已知电池总反应式:4A1+3O2+6H2O=4A1(OH)3,写出负极和正极的电极反应式
负极:4A1-12e- = 4A13+
正极:3O2+6H2O+12e- =12OH-
2.据媒体报道:以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢为燃料,空气为氧化剂,铂做催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )
①正极反应为:O2 + 4H+ + 4e- = 2H2O ②负极反应为:2H2-4e- = 4H+③总的化学反应为:2H2 + O2 == 2H2O④氢离子通过电解质向正极移动 (A)①②③ (B)②③④ (C)①②④ (D)①②③④
3、银锌电池广泛用作电子仪器的电源,它的充电和放电过程可以表示为:在此电池放电时,负极上发生反应的物质是( )A、Ag B、Zn(OH)2C、Ag2O D、Zn
2Ag+Zn(OH)2 Ag2O +Zn+H2O
必修 第二册第一节 化学反应与能量变化备课课件ppt: 这是一份必修 第二册第一节 化学反应与能量变化备课课件ppt,共27页。PPT课件主要包含了电池是谁发现的,无处不在的电池,学习目标,第4课时化学电源等内容,欢迎下载使用。
人教版 (2019)必修 第二册第一节 化学反应与能量变化图片ppt课件: 这是一份人教版 (2019)必修 第二册第一节 化学反应与能量变化图片ppt课件,共24页。PPT课件主要包含了学习目标,设计原电池等内容,欢迎下载使用。
苏教版 (2019)必修 第二册第三单元 化学能与电能的转化获奖课件ppt: 这是一份苏教版 (2019)必修 第二册第三单元 化学能与电能的转化获奖课件ppt,共44页。PPT课件主要包含了学习目标,知识体系,继续使用,原电池,燃料燃烧,知识梳理,石墨棒,氧化银,二氧化铅,氢氧化钾等内容,欢迎下载使用。














