






- 5.2.1 氮气、氮的氧化物(精品课件) 课件 31 次下载
- 5.3.1 硅及其化合物(精品课件) 课件 27 次下载
- 6.1.2 化学反应与电能(精品课件) 课件 25 次下载
- 6.1.3 化学电源(精品课件) 课件 26 次下载
- 6.2.1 化学反应速率(精品课件) 课件 28 次下载
人教版 (2019)必修 第二册第一节 化学反应与能量变化教案配套ppt课件
展开第一课时 化学反应与热能
现代社会中,人类的一切活动(从衣食住行到文化娱乐,从社会生产到科学研究等)都离不开能量,而许多能量的利用与化学反应中的能量变化密切相关。从煤、石油和天然气等提供的热能,到各种化学电池提供的电能,都是通过化学反应获得的
第一节 化学反应与能量变化
天然气的主要成分为甲烷(CH4),燃烧时产生蓝色火焰,产物主要是水及二氧化碳。
化学反应中除了物质变化还伴随着能量变化
能量变化:热能、光能、电能……
“暖宝宝”中含有铁粉、活性炭、水、氯化钠等物质,遇空气发生反应的化学方程式:
4Fe+3O2+6H2O=4Fe(OH)3
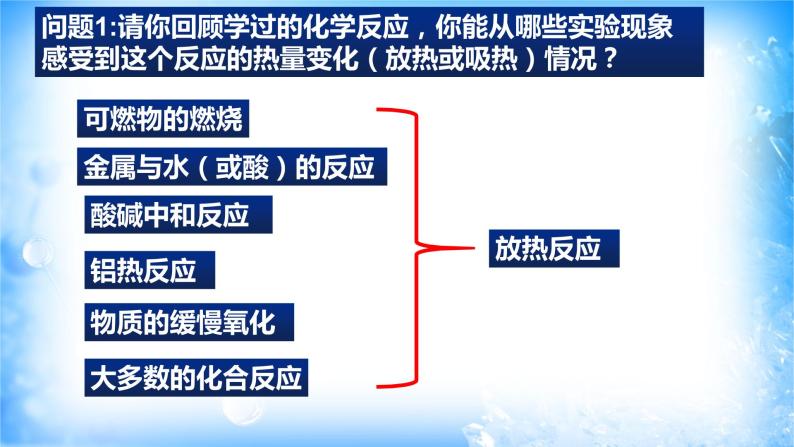
问题1:请你回顾学过的化学反应,你能从哪些实验现象感受到这个反应的热量变化(放热或吸热)情况?
金属与水(或酸)反应是一类放热反应
NaOH+HCI=NaCl+H2O
酸碱中和反应是放热反应
实验现象:反应放出大量的热,并发出耀眼的光芒;纸漏斗的下部被烧穿,有熔融物落入沙中。
冶炼难溶的金属(物质变化)
利用放出的热,焊接钢轨等大截面钢材部件(能量变化)
金属与水(或酸)的反应
Ba(OH)2.8H2O+2NH4Cl=BaCI2+10H2O+2NH3↑
NaHCO3+HCl=NaCl+H2O+CO2↑
N2+O2= 2NO
注意:大多数的吸热反应需要加热高温等条件;但也有常温的吸热反应和需要加热或高温的放热反应(例如铝热反应)
问题2:化学反应中为什么会有能量变化?能量变化的本质是什么?
物质中的原子(或离子)之间是通过化学键相结合的。当发生化学反应时,破坏旧化学键需要吸收能量,而形成新化学键需要释放能量。因此,在化学反应中,不仅有新物质生成,而且伴随着能量变化。
角度一:比较旧化学键断裂吸收与新化学键生成放出的能量(微观)
【算一算】请根据下列信息判断氢气和氯气化合生成氯化氢的反应是吸收能量还是放出能量?
H2 + CI2 = 2HCI
H—H + Cl—Cl → 2H—Cl
(436+243)KJ
(431+431)KJ
【算一算】请根据下列信息判断水蒸气分解生成氢气和氧气的反应是吸收能量还是放出能量?
2H2O = 2 H2 + O2
4H—O → 2H—H + O=O
(2×436+498)KJ
各种物质都具有能量,物质的组成、结构与状态不同,所具有的能量也不同。放热反应可以看成是反应物所具有的化学能转化为热能释放出来,吸热反应可以看成是热能转化为化学能被生成物所“储存”。
角度二:比较反应物与生成物的总能能量(宏观)
你能否将这幅图变得更简单直观,能一目了然的看出一个化学反应是吸热也还是放热呢?
问题2小结:化学反应中能量变化的原因和本质
1.判断下列说法的正误,正确的在括号内划“√”,错误的在括号内划“×”。(1)所有化学反应必然引起物质状态的变化( )(2)不同的化学反应放出或吸收的能量一般是不相同的( )(3)放出能量越多的反应,通常生成物越不稳定( )(4)因为氢气在氧气中燃烧是放出能量的,所以水的分解反应一定是吸收能量的( )
解析:放出能量越多的反应,说明生成物的能量越低,生成物越稳定
2.从如图所示的某气体反应的能量变化分析,以下判断正确的是( )
C.生成物的总能量低于反应物的总能量
D.反应物比生成物更稳定
3.下列变化中属于吸热反应的是( )①液态水汽化 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华A.①④ B.②④ C.③⑤ D.④⑥
解析 ①③⑥不是化学反应,②④是吸热反应,⑤是放热反应。
4.下列说法正确的是( )A.物质发生化学反应时都伴随着能量变化B.伴有能量变化的物质变化都是化学变化C.在一个确定的化学反应体系中,反应物的总能量与生成物的总能量一定相同D.在一个确定的化学反应体系中,反应物的总能量总是高于生成物的总能量
物质发生化学反应时都伴随着能量变化,伴有能量变化的物质变化不一定是化学变化,如物质发生核变(如原子弹的爆炸)时也伴有能量变化。在一个确定的化学反应体系中,反应物的总能量(设为x)与生成物的总能量(设为y)之间的关系:①x>y,化学反应为放热反应;②x<y,化学反应为吸热反应。
高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化精品作业ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化精品作业ppt课件,文件包含611化学反应与热能课件pptx、611化学反应与热能分层作业含解析docx、611化学反应与热能分层作业无答案docx等3份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化备课课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第一节 化学反应与能量变化备课课件ppt,共25页。PPT课件主要包含了小知识,有气泡产生,镁与盐酸反应放出热量,镁条逐渐溶解,温度计指示温度升高,有刺激性气味气体产生,吸热反应与放热反应,放热反应与吸热反应,化学反应的特征,化学反应的实质等内容,欢迎下载使用。
高中化学第六章 化学反应与能量第一节 化学反应与能量变化背景图课件ppt: 这是一份高中化学第六章 化学反应与能量第一节 化学反应与能量变化背景图课件ppt,共29页。PPT课件主要包含了学习目标,实验探究,1放热反应,常见的放热反应,常见的吸热反应,2吸热反应,思考与讨论,课堂练习,化学反应放出能量,化学反应吸收能量等内容,欢迎下载使用。














