化学必修一专题2 从海水中获得的化学物质第一单元 氯、溴、碘及其化合物教案
展开2.1.1 氯气的生产原理
评价 | 签字 |
班级_______姓名_________学号_______
[学习目标]
1、了解从海水中获得Cl2的基本原理和方法;
2、了解氯气的实验室制法;
[调查研究]浩瀚的大海,巨大的宝藏。在众多的自然资源中,海水是十分重要的资源之一,能利用的海水中富含的化学物质如:NaCl、MgCl2、NaBr、NaI等。椐估计:每立方千米的海水中含NaCl 4×107t,查阅有关资料,了解人们是如何从海水中获得氯化钠和使用氯化钠的。并将有关情况与同学们交流讨论。
[新课导入]从海水晒盐得到的食盐,除去杂质后,不仅可以作调料,还可以作为工业原料。19世纪,科学家发明了电解饱和食盐水制取氯气的方法,为工业制氯气奠定了基础。
[知识形成1]
⑴接通电源,观察两极现象;
⑵通电一段时间后,用小试管收集U形管左端产生的气体,2min后,提起小试管,并迅速用拇指堵住试管口,移近点燃的酒精灯,松开拇指,检验收集到的气体;
⑶取一只小试管,用向上排空法收集从U形管右端导出的气体,观察收集到气体的颜色;
⑷关闭电源,打开U形管两端的橡皮塞,分别向溶液中滴加1~2滴酚酞溶液,观察现象;
将上述实验中观察到的现象和所得结论填入下表。
| 实验现象 | 结论 |
⑴ |
|
|
⑵ |
|
|
⑶ |
|
|
⑷ |
|
|
根据实验现象推断,电解饱和食盐水:
①化学方程式:__________________________
②与电源正极相连的电极(阳极)上产生__气;与电源负极相连的电极(阴极)上产生__气。
[问题解决1]
1、b端为何要通入氢氧化钠溶液?
2、两电极产生的气体体积比为____;电解食盐水除了得到氯气以外,还能得到___________ 。人们把以电解食盐水为基础制取氯气、烧碱(NaOH)等产品的工业称为 ,它是目前化学工业的重要支柱之一。
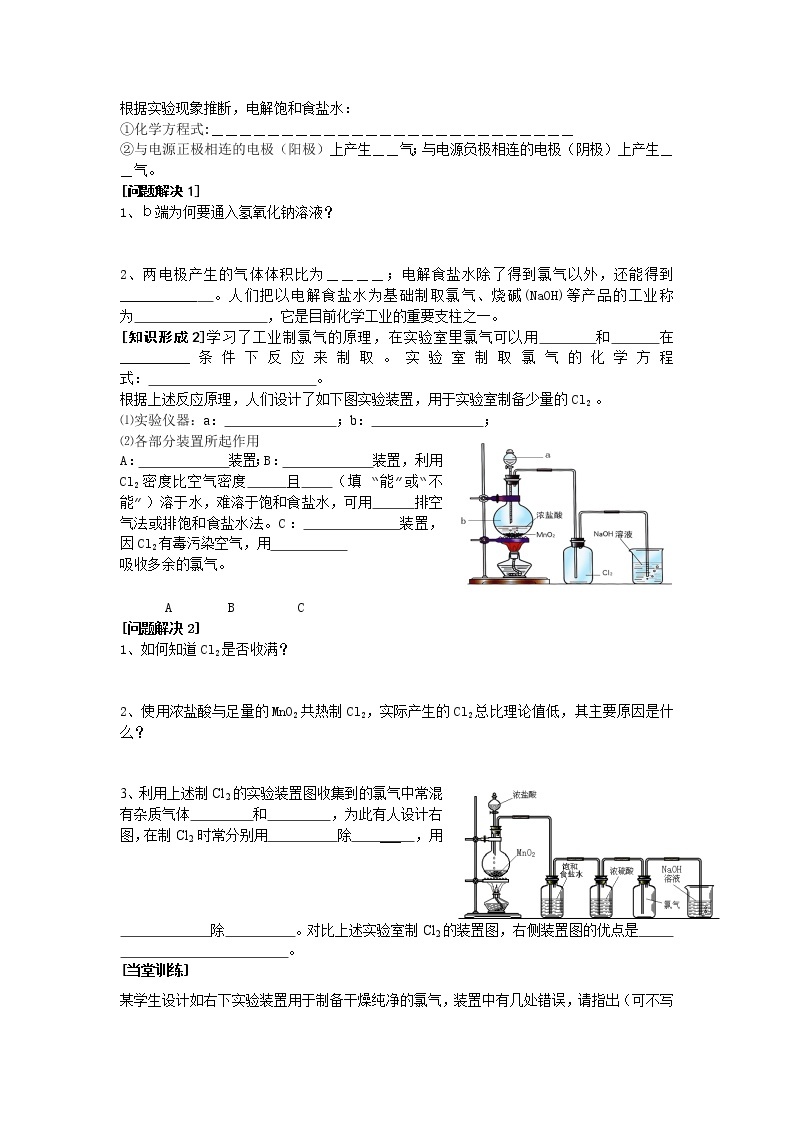
[知识形成2]学习了工业制氯气的原理,在实验室里氯气可以用 和 在__________条件下反应来制取。实验室制取氯气的化学方程式: 。
根据上述反应原理,人们设计了如下图实验装置,用于实验室制备少量的Cl2 。
⑴实验仪器:a: ;b: ;
⑵各部分装置所起作用
A: 装置;B: 装置,利用Cl2密度比空气密度 且 (填 “能”或“不能”)溶于水,难溶于饱和食盐水,可用 排空气法或排饱和食盐水法。C: 装置,因Cl2有毒污染空气,用
吸收多余的氯气。
A B C
[问题解决2]
1、如何知道Cl2是否收满?
2、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
3、利用上述制Cl2的实验装置图收集到的氯气中常混有杂质气体 和 ,为此有人设计右图,在制Cl2时常分别用 除 ___ ,用
除 。对比上述实验室制Cl2的装置图,右侧装置图的优点是
。
[当堂训练]
某学生设计如右下实验装置用于制备干燥纯净的氯气,装置中有几处错误,请指出(可不写满)。
⑴ ;
⑵ ;
⑶ ;
⑷ ;
⑸ ;
⑹ ;
[课堂小结]
[课外练习](选择题每题有1-2个答案)
1.海水中含量最多的离子是 ( )
A.钠离子 B.氯离子 C.钙离子 D.镁离子
2.在电解饱和食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,不正确的操作顺序是 ( )
①过滤 ②加稍过量的NaOH溶液 ③加适量的盐酸
④加稍过量的碳酸钠溶液 ⑤加稍过量的氯化钡溶液
A.⑤④②①③ B.④⑤②①③
C.②⑤④①③ D.⑤②④①③
3.如图所示装配仪器,接通直流电源,电解饱和食盐水,则电解片刻,在碳棒和铁钉表面都有气体生成,其中碳棒表面生成的气体是 ( )
A. Cl2 B.O2 C.H2 D.HCl
4.若电解的是未精制的饱和食盐水(即是粗盐溶于水),结果很快在某一电极附近出现浑浊现象,造成浑浊的难溶物主要是 ( )
A.碳酸镁 B.硫酸钡 C.氢氧化镁 D.碳酸钡
5.下列物质中,可以用来除去Cl2中的水蒸气的是 ( )
①碱石灰 ②浓硫酸 ③无水CaCl2 ④固体烧碱
A. ①② B. ①③④ C. ②③ D. ①②③④
6.实验室制取氧气的试管壁上粘附有MnO2,除去粘附的MnO2可用的试剂是 ( )
A. 蒸馏水 B. KOH溶液 C. 稀盐酸 D. 热的浓盐酸
7.用下列两种方法制取氯气:①用含氯化氢146克的浓盐酸与足量的二氧化锰反应②用87克二氧化锰与足量的浓盐酸反应,则所得氯气 ( )
A.②比①多 B.①比②多 C.一样多 D.无法比较
8.将两个石墨电极插入500ml食盐水中进行电解,通电到一定时间后,某一电极收集到标准状况下224ml气体(设电解时溶液体积无变化)。此时溶液中氢氧化钠的物质的量浓度约为 ( )
A.0.2mol/L B. 0.1mol/L C. 0.04mol/L D. 0.02mol/L
9.在U型管里装入饱和食盐水,滴入几滴酚酞试液,用一根碳棒作阳极,一根铁棒作阴极,把湿润的碘化钾淀粉试纸放在阳极附近。接通直流电后,可以观察到U型管的两个电极上都有 ,阳极放出的气体有 气味,并且能使湿润的碘化钾淀粉试纸 ,说明放出的是 ;阴极放出的气体是 ,同时发现阴极附近溶液 ,这说明溶液里有 性物质生成。电解饱和食盐水的化学方程式为
。
10.实验室制氯气有如下操作,正确的操作顺序是_________
① 缓缓加热 ;②加入MnO2粉末;③连好装置,检查气密性;④从装有浓盐酸的分液漏斗中加浓盐酸;⑤将多余氯气用NaOH溶液吸收;⑥向上排气收集氯气;
11.氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
⑴在电解过程中,与电源正极相连的电极上的产物是________;与电源负极相连的电极附近溶液中c(OH-) ________(选填:“不变”、“增大”或“减小”);
⑵工业食盐中含Ca2+、Mg2+等杂质,精制过程分别除去Ca2+、Mg2+应选用的试剂是:________,________;
⑶如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是_______(填a,b,c);
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
⑷为有效除去Ca2+、Mg2+ 、SO42-,加入试剂的合理顺序为________(选填a,b,c。);
a.先加NaOH,再加Na2CO3,再加钡试剂 b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
⑸脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________,冷却,________,________,(填写操作名称)除去NaCl。
⑹电解饱和食盐水时,总的反应方程式为: ;
12.右图表示在没有通风橱的条件下制备氯气时设计的装置, 图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
⑴仪器C的名称是 ;水槽中应盛放的是 ;烧杯中盛放的是 ;圆底烧瓶中发生反应的化学方程式为:
;
⑵在收集氯气时,应打开 ,关闭___。当氯气收集完毕时打开 ,关闭___。(填A或B或C)
⑶ 若要制得标准状况下的Cl2 0.672L,理论上需要MnO2的物质的量是多少?
化学必修 第一册实验活动2 铁及其化合物的性质教学设计: 这是一份化学必修 第一册实验活动2 铁及其化合物的性质教学设计,共4页。教案主要包含了创设问题,学生讨论交流,学生自主探究实验,组织学生讨论,得出结论,学生回答,活动与探究,小结实验等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第一节 脂肪烃教案: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 脂肪烃教案,共4页。
高中苏教版第一单元 氯、溴、碘及其化合物教学设计: 这是一份高中苏教版第一单元 氯、溴、碘及其化合物教学设计,共5页。