
高中化学苏教版必修一专题2 从海水中获得的化学物质第一单元 氯、溴、碘及其化合物教案设计
展开专题二 第一单元 氯、溴、碘及其化合物
第1课时 氯气的生产原理
【教学目标】1、了解海水晒盐的过程及氯化钠的用途。
2、掌握氯气的生产原理——电解饱和食盐水制取氯气。
3、掌握氯气的工业制法、实验室制法。
4、通过引导学生观察实验,分析演示实验现象,培养学生观察和分析问题能力。
【教学重点】1、氯气的生产原理和工业制法 2、实验室制备氯气的原理
【教学难点】1、饱和食盐水的电解反应 2、氯气的发生、收集、净化装置
【教学手段】运用课件和演示实验
第一课时(氯气的生产原理)
【教学过程】
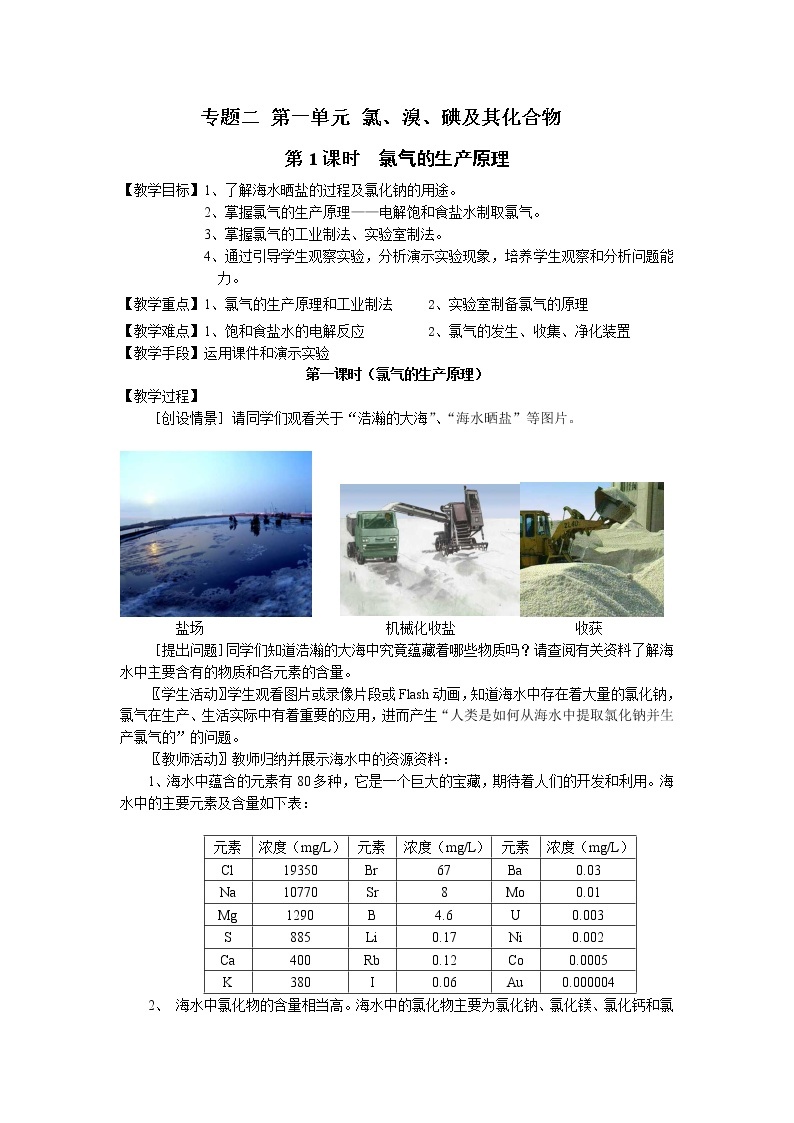
[创设情景]请同学们观看关于“浩瀚的大海”、“海水晒盐”等图片。
盐场 机械化收盐 收获
[提出问题]同学们知道浩瀚的大海中究竟蕴藏着哪些物质吗?请查阅有关资料了解海水中主要含有的物质和各元素的含量。
〖学生活动〗学生观看图片或录像片段或Flash动画,知道海水中存在着大量的氯化钠,氯气在生产、生活实际中有着重要的应用,进而产生“人类是如何从海水中提取氯化钠并生产氯气的”的问题。
〖教师活动〗教师归纳并展示海水中的资源资料:
1、海水中蕴含的元素有80多种,它是一个巨大的宝藏,期待着人们的开发和利用。海水中的主要元素及含量如下表:
元素 | 浓度(mg/L) | 元素 | 浓度(mg/L) | 元素 | 浓度(mg/L) |
Cl | 19350 | Br | 67 | Ba | 0.03 |
Na | 10770 | Sr | 8 | Mo | 0.01 |
Mg | 1290 | B | 4.6 | U | 0.003 |
S | 885 | Li | 0.17 | Ni | 0.002 |
Ca | 400 | Rb | 0.12 | Co | 0.0005 |
K | 380 | I | 0.06 | Au | 0.000004 |
2、 海水中氯化物的含量相当高。海水中的氯化物主要为氯化钠、氯化镁、氯化钙和氯化钾等。地球上99%以上的溴蕴藏在大海中,海水中溴的总储量高达 1×1014 t,因而溴被称为“海洋元素”。此外,海水中还含有丰富的碘元素,据估计,海水中碘的总量可达8×1010 t 。
课本P40〖调查研究〗查阅有关资料,了解人们是如何从海水中获得氯化钠和使用氯化钠的。将有关的情况与同学交流讨论。
2、氯化钠用途:医疗上用的生理盐水;农业上用氯化钠溶液来选种;用食盐腌渍蔬菜、鱼、肉、蛋等;公路上的积雪可用氯化钠来消除;氯碱工业上用氯化钠为原料。
演示P40实验:完成实验内容:
一、氯气的生产原理
1、电解饱和食盐水实验
实验现象 | 结论 |
(1)电极周围均有气泡产生 | 通电后有气体物质生成 |
(2)收集到的气体靠近火焰有爆鸣声。 | 有氢气生成 |
(3)湿润的淀粉碘化钾试纸变蓝。 | 有氯气生成 |
(4)阴极的溶液变红色。 | 有碱性物质生成(NaOH) |
2、反应原理的化学方程式
【简述】1774年,瑞典化学家舍勒把浓盐酸与软锰矿混合在一起加热,意外发现生成了一种黄绿色气体。他发现这种气体的水溶液略显酸性,并且还能使花朵、纸张、叶子等物质褪色,还能与金属物质发生化学反应。1810年,英国化学家戴维确认:这种气体是由一种元素组成的。他将这种元素命名为chlorine,希腊文意为“绿色的”。
二、氯气的实验室制法:
1、主要仪器:分液漏斗、圆底烧瓶、铁架台、石棉网、酒精灯、集气瓶、烧杯、导管、双孔橡皮塞等
2、反应原料:浓盐酸与二氧化锰
3、实验原理:4HCl(浓)+MnO2MnCl2+2H2O+Cl2↑
4、发生装置:固体+液体气体
5、收集装置:向上排空气法或排饱和食盐水法
6、尾气处理:氢氧化钠溶液
2NaOH + Cl2 = NaCl + NaClO + H2O
7、除杂干燥:饱和食盐水:除HCl 浓硫酸:除水蒸气
总结:
课堂练习:
1、下列方法不能用于制取氯气的是( A )
A、稀盐酸与二氧化锰共热 B、将氯酸钾与浓盐酸共热
C、氯化钾与浓硫酸共热 D、将高锰酸钾与浓盐酸共热
2、实验室制取氯气有如下操作,正确顺序是 ( D )
①连好装置检查气密性;② 缓缓加热;③加入二氧化锰粉末;④从装有浓盐酸的分液漏斗中加入浓盐酸;⑤将多余氯气用氢氧化钠溶液吸收 ⑥向上排气收集氯气
A、① ② ③ ④ ⑤ ⑥ B、③ ④ ② ① ⑥ ⑤
C、① ④ ③ ② ⑥ ⑤ D、① ③ ④ ② ⑥ ⑤
3、除去实验室制取氯气的试管壁上粘有的二氧化锰,可用的试剂是( D )
A、 蒸馏水 B、氢氧化钾溶液 C、稀盐酸 D、热的浓盐酸
4、实验室用下列两种方法制取氯气( B )
①用含HCl 146g的浓盐酸与足量的MnO2反应
②用87g MnO2与足量的浓HCl反应。则所得的Cl2(同温同压下)
A、①比②多 B、②比①多 C、一样多 D、无法比较
5、在U型管里装入饱和食盐水,滴入几滴酚酞试液,用一根碳棒作阳极,一根铁棒作阴极,把湿润的碘化钾淀粉试纸放在阳极附近。接通直流电后,可以观察到U型管的两个电极上都有 ,阳极放出的气体有 气味,并且能使湿润的碘化钾淀粉试纸 ,说明放出的是 ;阴极放出的气体是 ,同时发现阴极附近溶液 ,这说明溶液里有 性物质生成。电解饱和食盐水的化学方程式为 。
参考答案:
1、A 2、D 3、D 4、B
5、气体放出;刺激性;变蓝;Cl2 ;H2 ;变红;碱;
补充作业:
1、某学生设计如下实验装置用于制备纯净的氯气。
装置中有六处错误,请指出。
(1) ,
(2) ,
(3) ,
(4) ,
(5) ,
(6) 。
2、在更正后的装置图中:
(1)饱和食盐水的作用 ;
(2)浓硫酸的作用 ;
(3)氢氧化钠的作用 。
参考答案:
1、(1)铁架台上未加点燃的酒精灯;(2)铁圈上未放石棉网;
(3)不应用稀盐酸;(4)盛浓硫酸和盛饱和食盐水的两个洗气瓶位置错误;
(5)盛浓硫酸的洗气瓶中的进气导管和出气导管连接错误;(6)不应使用长颈漏斗。
2、(1)洗去氯气中所含的少量氯化氢气体;(2)可以除去氯气中的水蒸气;
(3)吸收多余的氯气,防止污染空气。
板书设计:
一、氯气的生产原理
1、电解饱和食盐水实验
实验现象 | 结论 |
(1)电极周围均有气泡产生 | 通电后有气体物质生成 |
(2)收集到的气体靠近火焰有爆鸣声。 | 有氢气生成 |
(3)湿润的淀粉碘化钾试纸变蓝。 | 有氯气生成 |
(4)阴极的溶液变红色。 | 有碱性物质生成(NaOH) |
2、反应原理的化学方程式;
二、氯气的实验室制法:
1、主要仪器:
2、反应原料:浓盐酸与二氧化锰
3、实验原理:4HCl(浓)+MnO2MnCl2+2H2O+Cl2↑
4、发生装置:固体+液体气体
5、收集装置:向上排空气法或排饱和食盐水法
6、尾气处理:氢氧化钠溶液 2NaOH + Cl2 = NaCl + NaClO + H2O
7、除杂干燥:饱和食盐水:除HCl 浓硫酸:除水蒸气
高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学设计及反思: 这是一份高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学设计及反思,共5页。教案主要包含了演示实验,学生活动等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第一节 脂肪烃教案: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 脂肪烃教案,共4页。
高中苏教版第一单元 氯、溴、碘及其化合物教学设计: 这是一份高中苏教版第一单元 氯、溴、碘及其化合物教学设计,共5页。













