




人教版九年级上册课题3 制取氧气教课内容课件ppt
展开1、化合反应的特点是:
2、用高锰酸钾、氯酸钾和过氧化氢(双氧水)制取氧气的反应是化合反应吗?请你写出实验室制取氧气的三个反应原理。
化合反应: 。分解反应: 。氧化反应: 。
辨别下列反应中的化合反应、分解反应、氧化反应1、水 氢气 + 氧气2、木炭 + 氧气 二氧化碳3、石蜡 + 氧气 水 + 二氧化碳4、氧化钙 + 水 氢氧化钙5、氢氧化铜 氧化铜 + 水
过氧化氢制氧气和氯酸钾制氧气的发生装置能否相同?
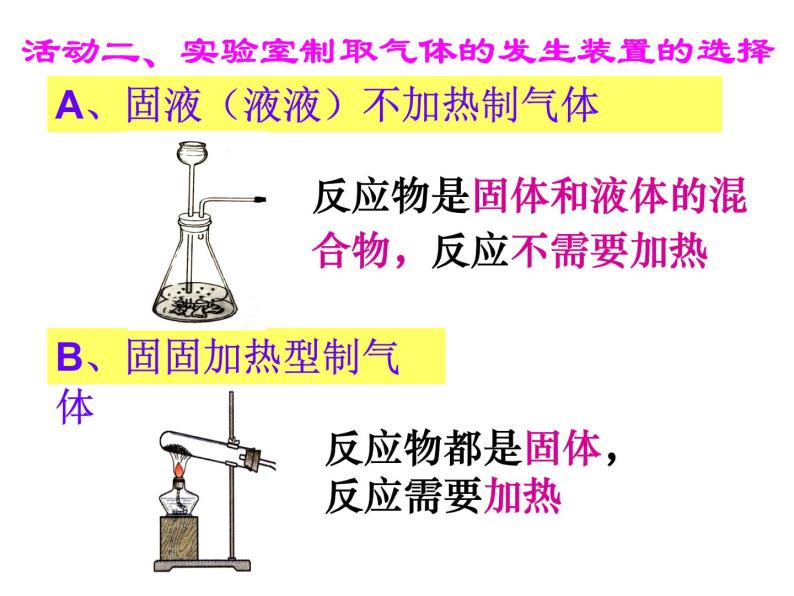
反应物都是固体,反应需要加热
活动二、实验室制取气体的发生装置的选择
反应物是固体和液体的混合物,反应不需要加热
A、固液(液液)不加热制气体
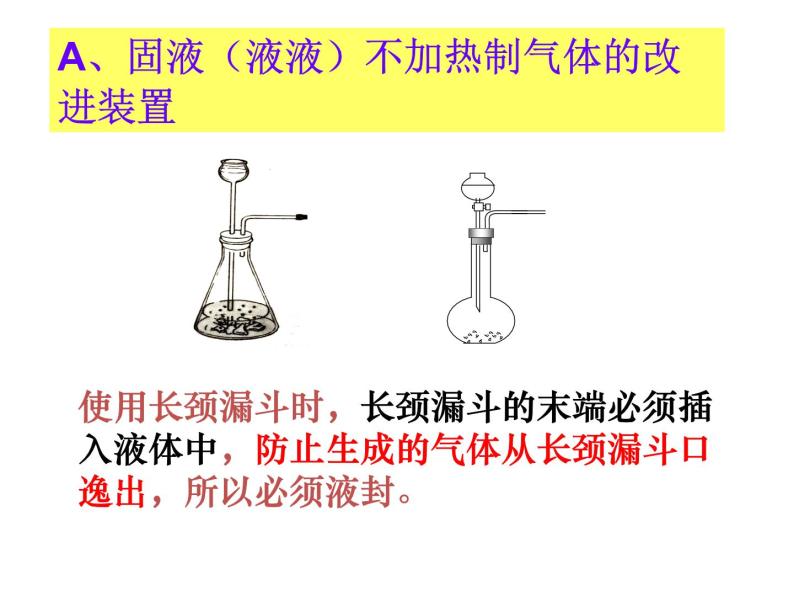
使用长颈漏斗时,长颈漏斗的末端必须插入液体中,防止生成的气体从长颈漏斗口逸出,所以必须液封。
A、固液(液液)不加热制气体的改进装置
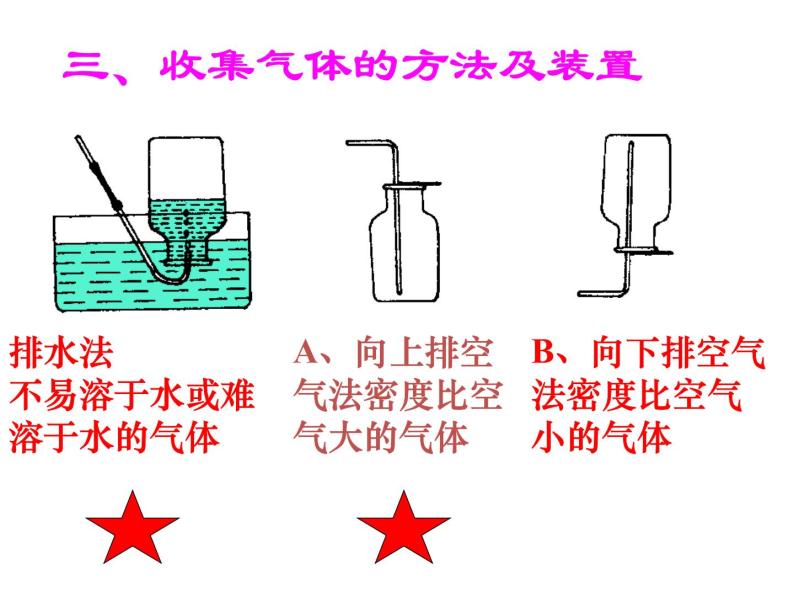
三、收集气体的方法及装置
排水法不易溶于水或难溶于水的气体
A、向上排空气法密度比空气大的气体
B、向下排空气法密度比空气小的气体
如何检验收集到的是氧气?
将一支带火星的木条伸进集气瓶内,若木条复燃,证明是氧气。检验存在
将一支带火星的木条伸到集气瓶口,若木条复燃,证明已集满。检验收满
用向上排空气法收集氧气,如何验满?
活动四、加热高锰酸钾制氧气
探究:用高锰酸钾制氧气
高锰酸钾 锰酸钾 + 二氧化锰 + 氧气
KMnO4 K2MnO4 + MnO2 + O2
防止加热时高锰酸钾粉末进入导管
(7)先把导管移出水面,
(2)检查装置气密性,
1、药品平铺在试管底部
3、导管伸入试管不能太长
实验中应该注意哪些事项?
2、铁夹夹在离试管口1/3处
原因:不利于气体的排出
5、用酒精灯的外焰先均匀预热,再集中在有药品的部位集中加热,
6、等有连续的气泡产生时再收集
原因:防止冷凝水倒流至试管底部,炸裂试管
原因:刚加热时产生的气泡中混有空气,这时的气体不纯
7、实验完毕,先撤导管,后移酒精灯
8、收集满的氧气,应正放在桌面上,并用玻璃片盖上
原因:防止试管冷却后,水槽内的水沿导管上升,进入试管,使试管炸裂
原因:氧气密度比空气略大
小结:实验仪器和实验装置:
夹持在距管口约1/3处
若用高锰酸钾制氧气应在管口塞一团棉花
导管伸出橡 皮塞约0.5cm
1、比较下列三个实验装置图:
装置A与B、C相比较,其优点有:
③可以控制氧气的产生速率。
①可以随时添加药品,不断产生氧气。
②不需要加热,节约能源。
要收集到较干燥的氧气:选用_____________。要收集到较纯净的氧气:选用_____________。
不易溶或难溶于水的气体
2、根据气体的溶解性和密度确定
3、实验室用氯酸钾制氧气的实验中,不需要使用的仪器是( ) A.烧杯 B.大试管 C.酒精灯 、铁架台 D.导管、单孔塞
(1)催化剂只能加快化学反应的速率。( )(2)在过氧化氢制氧气的反应中,如果不加入二氧化锰,产生氧气的量就少。( )(3)一个反应只有一种催化剂。( )(4)二氧化锰是催化剂。( )(5)不同的反应,催化剂一定不同。( )
2、下列关于催化剂的说法不正确的是( )A.化学反应前后,催化剂的质量和化学性质都不变B.催化剂可以提高某些化学反应的速率C.催化剂可以降低某些化学反应的速率D.任何化学反应都需要催化剂
3、下列有关催化剂的叙述正确的是( ) A、在化学反应里能加快其他物质的化学反应速率,而本身的质量和性质在反应前后没有改变的物质。 B、二氧化锰是催化剂。 C、在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都没有改变的物质。 D、要使过氧化氢溶液分解出氧气,必须要加入二氧化锰,否则就不能发生反应。 4.三份质量相等的氯酸钾固体。第一份中加入少量二氧化锰,第二份中加入少量高锰酸钾,第三份不加任何物质。给它们分别加热完全分解,放出氧气的 量( ) A、第一份最多 B、第二份最多 C、第三份最多 D、一样多
人教版九年级上册课题3 制取氧气教案配套ppt课件: 这是一份人教版九年级上册课题3 制取氧气教案配套ppt课件,共20页。PPT课件主要包含了新课引入,实验药品,实验原理,实验装置,实验步骤,思考交流,催化剂和催化作用,用氯酸钾制取氧气,分解反应,学完本课题你应该知道等内容,欢迎下载使用。
初中课题3 制取氧气授课ppt课件: 这是一份初中课题3 制取氧气授课ppt课件,共29页。PPT课件主要包含了高锰酸钾,过氧化氢,氯酸钾,氧气不易溶于水,带火星的木条复燃等内容,欢迎下载使用。
人教版九年级上册第二单元 我们周围的空气课题3 制取氧气图文ppt课件: 这是一份人教版九年级上册第二单元 我们周围的空气课题3 制取氧气图文ppt课件,共14页。PPT课件主要包含了新课引入,新课讲解,实验室制取氧气,制取氧气的步骤,氧气的工业制法,-196℃,-183℃,氧气的工业生产简析,强化练习,布置作业等内容,欢迎下载使用。













