
化学九年级上册课题3 制取氧气学案
展开一、学习目标:
1.掌握实验室制取氧气的方法和原理,初步了解通过化学实验制取新物质的方法。
2. 理解分解反应,区别化合反应和分解反应。
3. 知道催化剂和催化作用。
4. 初步建立“理论分析----实验设计----实验操作”的科学思路。
【情景导入】
1.如何检验一瓶无色气体是氧气?
2.如何鉴别三瓶无色气体:空气、氧气、氮气?
3.你知道在酿酒过程中酒曲的作用吗?
一、过氧化氢分解制氧气的反应中二氧化锰的作用
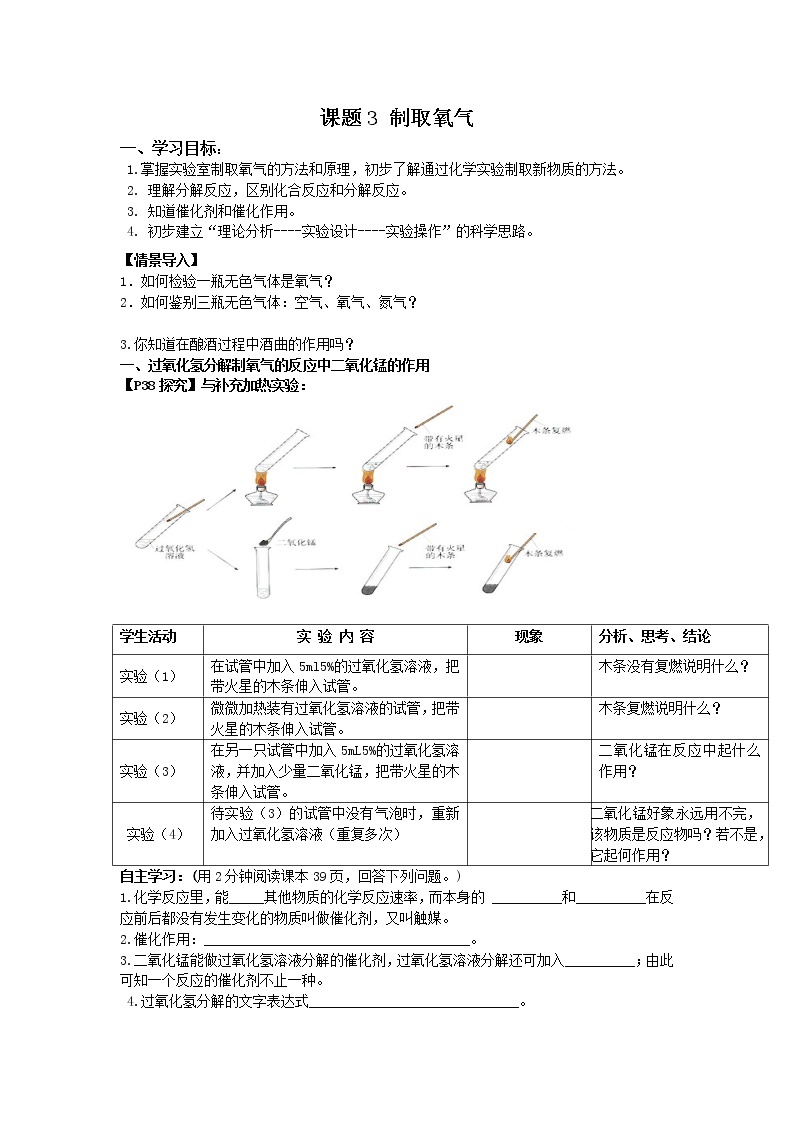
【P38探究】与补充加热实验:
自主学习:(用2分钟阅读课本39页,回答下列问题。)
1.化学反应里,能_____其他物质的化学反应速率,而本身的 __________和__________在反应前后都没有发生变化的物质叫做催化剂,又叫触媒。
2.催化作用:______________________________________。
3.二氧化锰能做过氧化氢溶液分解的催化剂,过氧化氢溶液分解还可加入__________;由此可知一个反应的催化剂不止一种。
4.过氧化氢分解的文字表达式______________________________。
讨论交流:
1.催化剂的作用:
2.催化剂的特点:
二、加热氯酸钾或高锰酸钾制取氧气
【观察与思考】
(1)仔细观察教师所展示的氯酸钾,将其物理性质记录在下面:
(2)观察老师演示【实验2-5】、观察并记录实验现象。
二氧化锰在(2)中所起的作用是 ;该反应的文字表达式: _____。
自主学习:
(1)仔细观察教师所展示的高锰酸钾,将其物理性质记录在下面:
(2)记住课本37页高锰酸钾制取氧气的文字表达式,并默写在下面:
讨论交流:根据用加热氯酸钾和二氧化锰的混合物或者高锰酸钾制取氧气所需药品的状态及反应条件,并根据氧气的性质,实验室用上述方法制取氧气所需要的装置是( )
合作学习:
(1)默写用二氧化锰催化过氧化氢、加热氯酸钾和二氧化锰的混合物、加热高锰酸钾制取氧气的文字表达式:
(2)从反应物和生成物的种类上分析以上反应的共同点。
(3)上述三个反应都是分解反应,你能根据他们的共同点说出分解反应的概念吗?写在下面。(分解反应也是化学基本反应类型之一)
精讲点拨:
【例题1】实验室里用二氧化锰作催化剂,加热氯酸钾制取氧气。若忘记加入二氧化锰,其结果是( )
A.不能产生氧气B.产生氧气的速率慢C.产生氧气的总量减少D.没有氯化钾生成
【解析】二氧化锰起催化作用,加快了反应的速率,但本身的质量和化学性质在反应前后没有变化;二氧化锰可以改变氯酸钾分解速率,没有加入二氧化锰,氯酸钾分解很慢;对于某反应来说,有时可以选用多种不同的催化剂。
【答案】B
【例题2】实验室里加热氯酸钾制取氧气。若把高锰酸钾误以为二氧化锰加入,其结果是:氯酸钾的反应速率________,生成氧气的质量_____________,氯酸钾和高锰酸钾混合加热,完全反应后,生成物有______种。
【解析】氯酸钾和高锰酸钾混合加热,高锰酸钾先分解,同时生成锰酸钾、二氧化锰和氧气。其中,二氧化锰做氯酸钾分解反应的催化剂,使发应速度加快;产生的氧气是高锰酸钾和氯酸钾分解反应的总和,也增加;完全反应后,物质的种类有四种。
【答案】加快,增加,四。
达标体验:
1.催化剂在化学反应中所起的作用是( )。
A.加快化学反应速率 B.使生成物质量增加
C.改变化学反应速率 D.减慢化学反应速率
2.实验室可用于制取氧气的药品( )
A.空气 B.过氧化氢或二氧化锰 C.高锰酸钾或过氧化氢 D.二氧化锰
3. (2012年湖南娄底)下列关于催化剂的说法不正确的是( )
A.化学反应前后,催化剂的质量和化学性质都不变
B.催化剂可以提高某些化学反应的速率
C.催化剂可以降低某些化学反应的速率
D.任何化学反应都需要催化剂
4.下列反应属于分解反应的是( )
A.铁+氧气四氧化三铁 B.硫+氧气二氧化硫
C.石蜡+氧气二氧化硫 D. 水氢气+氧气
5. (2012•湖北黄石)加热高锰酸钾制取氧气的操作中正确的是( )
A.固定装有高锰酸钾的试管时,试管口略向上倾斜
B.开始加热时,导管口出现气泡立即收集
C.加热试管时,先使酒精灯火焰在试管下方来回移动
D.停止加热时,先熄灭酒精灯再将导管移出水面
课堂小结:
1.实验室制取氧气的原理:写出用过氧化氢和二氧化锰、氯酸钾和二氧化锰、高锰酸钾分别制取氧气的文字表达式。
化合反应
分解反应
定义: 特点:
定义: 特点:
2.化学基本反应类型
拓展提升:
1.某同学取用一定量的过氧化氢溶液与一定量的二氧化锰混合制取氧气,下列有关氧气的体积(V)、二氧化锰的质量(m)与时间(t)关系的图示中正确的是( )
A B C D
2. 在实验室里,常采用分解 溶液或加热 的方法制取氧气,两个反应均属于 反应。在两个反应中,都接触到一种物质,它的名称叫做 。在前一个反应中,它是该反应的 ,在后一个反应中,它是该反应的 。
3.将一种无味的液体A装入试管,用带火星的木条试验,无现象,而向其中加入少量黑色粉末B后,迅速产生气泡,生成了使带火星的木条复燃的气体C,使金属E红热并伸入盛有气体C、瓶底有少量液体D的集气瓶中,金属E剧烈燃烧,火星四射,生成黑色固体F。
①写出它们的名称A: B: C: D: E: F:
②黑色粉末B在A的分解反应中起 作用,是这个反应的 剂。
答案:
达标体验:1.C 2.C 3.D 4.D 5.C
拓展提升:1.D 2. 过氧化氢,高锰酸钾,分解,二氧化锰,催化剂,生成物
3. ①过氧化氢,二氧化锰,氧气,水,铁,四氧化三铁 ②催化,催化
学生活动
实 验 内 容
现象
分析、思考、结论
实验(1)
在试管中加入5ml5%的过氧化氢溶液,把带火星的木条伸入试管。
木条没有复燃说明什么?
实验(2)
微微加热装有过氧化氢溶液的试管,把带火星的木条伸入试管。
木条复燃说明什么?
实验(3)
在另一只试管中加入5mL5%的过氧化氢溶液,并加入少量二氧化锰,把带火星的木条伸入试管。
二氧化锰在反应中起什么作用?
实验(4)
待实验(3)的试管中没有气泡时,重新加入过氧化氢溶液(重复多次)
二氧化锰好象永远用不完,该物质是反应物吗?若不是,它起何作用?
九年级上册课题1 空气导学案: 这是一份九年级上册课题1 空气导学案,共5页。学案主要包含了学习目标,自主探究,自我测评等内容,欢迎下载使用。
人教版九年级上册课题3 走进化学实验室学案设计: 这是一份人教版九年级上册课题3 走进化学实验室学案设计,共4页。学案主要包含了学习目标,自主探究,自我测评等内容,欢迎下载使用。
人教版九年级上册课题2 氧气学案及答案: 这是一份人教版九年级上册课题2 氧气学案及答案,共4页。学案主要包含了学习目标,自主探究,自我测评等内容,欢迎下载使用。













