





人教版 (新课标)必修2第一节 化学能与热能备课ppt课件
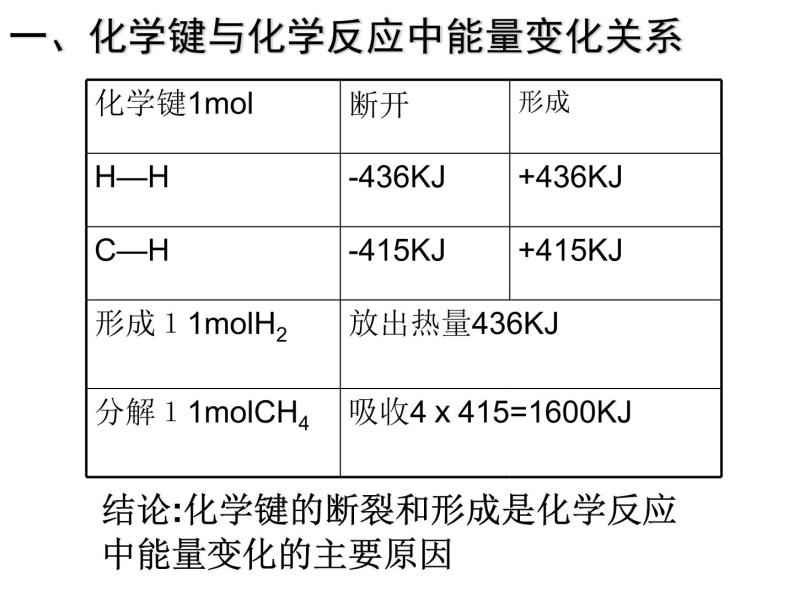
展开结论:化学键的断裂和形成是化学反应中能量变化的主要原因
一、化学键与化学反应中能量变化关系
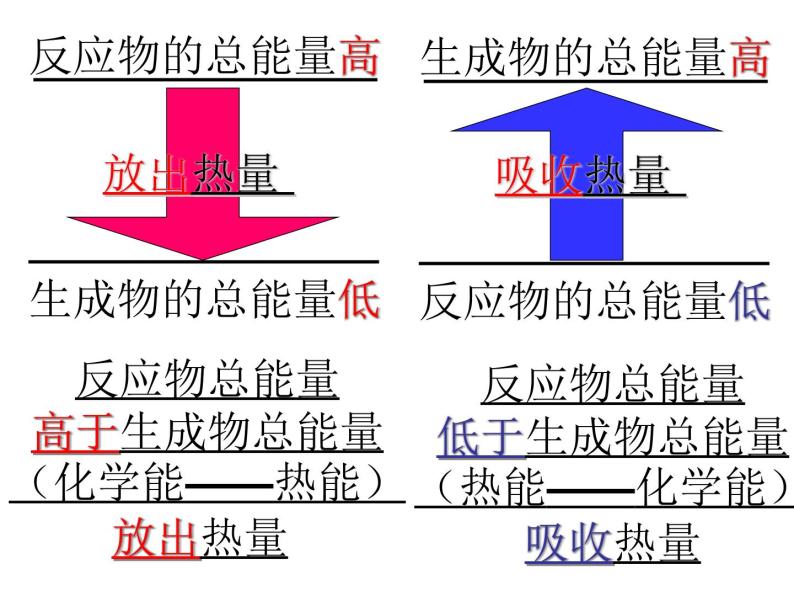
反应物总能量高于生成物总能量(化学能——热能)放出热量
反应物总能量低于生成物总能量(热能——化学能)吸收热量
E(反应物)>E(生成物)
E(反应物)<E(生成物)
结论:一个化学反应是释放能量还是吸收能量取决于反应物总能量与生成物总能量的相对高低
E(反)-E(生)=E(放)
E(生)-E(反)=E(吸)
1. 当物质发生化学反应时,断开反应物中的化学 键要 ;而形成生成物中的化 学键要 。一个化学反应 是释放能量还是吸收能量取决于 。
放出能量
反应物总能量与生成物总能量的相对大小
2. 已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是 A. A的能量一定高于CB. B的能量一定高于DC. A和B的总能量一定高于C和D的总能 量D. 该反应为放热反应,故不必加热就一定能发生
1mL H-H 键断裂所需能量 436kJ 1mL Cl-Cl 键断裂所需能量 243kJ 1ml H-Cl 键形成放出能量 431kJ
反应物吸收总能量 436kJ + 243kJ = 679kJ生成物释放总能量 431kJ × 2 = 862kJ
吸收能量 < 放出能量 反应放热
吸收能量 > 放出能量 反应吸热
3.下列各图中,表示正反应是吸热 反应的是 ( )
4. 下列说法中正确的是 ( )A. 物质发生化学反应都伴随着能量的变化B. 伴有能量变化的物质变化都是化学变化C. 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同D. 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
二、化学能与热能的相互转化
实验2-1:盐酸与铝片的反应
实验2-2 :Ba(OH)2· 8H2O与NH4Cl的反应
有气泡放出,温度升高。
有刺激性气味,烧杯底部很冷,烧杯下面的玻璃片被冻在一起。
实验2-3 :酸与碱的中和反应
HCl与NaOH发生中和反应时放热。
强酸和强碱发生反应时放出热量。
测量中和反应热应该注意哪些问题?
1. 保温隔热的效果一定要好。
2. 酸碱浓度要准确。
3. 温度计要读准,水银球要全浸在
4. 实验操作时动作要快,以尽量
溶液中,且要稳定一段时间再读。
三、常见放热反应和吸热反应
放热反应:1. 燃料物质的燃烧:C + O2 = CO2
2. 常见金属(Al、Fe、Zn等) 与酸(HCl、H2SO4等)的反应
3. 酸碱中和反应: HCl + NaOH = NaCl + H2O
5. 缓慢氧化:食物的腐败
4. 大多数化合反应
吸热反应:1. 大多数分解反应:CaCO3 = CaO + CO2↑
2. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应:Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
3. 碳与CO2气体的反应: C + CO2 =2CO
1. 下列物质加入水中显著放热的是:
A.生石灰 B.酒精
C.固体NaCl D.固体NaOH
2. 下列反应中既属于氧化还原反应同时又是吸热反应的是:
A.Ba(OH)2 · 8H2O与NH4Cl反应
B.镁与稀盐酸 C.灼热的炭与CO2
3. 下列反应属于放热反应的是:
A. NaOH与HCl反应 B. C和CO2共热
C. 碳酸钙的分解 D. 制备水煤气的反应
4. 1mlBa(OH)2 和1ml H2SO4反应放出的热量为Q,则Q为它们的中和热
四、化学反应提供的热能对人类社会意义利用热量进行生活、生产、和科研。利用热能使许多化学反应得以发生。
2020-2021学年第二节 资源综合利用,环境保护备课ppt课件: 这是一份2020-2021学年第二节 资源综合利用,环境保护备课ppt课件,共60页。PPT课件主要包含了第四章,有机物,无机物,碳元素,氧氮硫,2煤的综合利用,煤的焦化,焦炉气,煤焦油,可燃性气体等内容,欢迎下载使用。
高中化学人教版 (新课标)必修2第三章 有机化合物第四节 基本营养物质教学演示ppt课件: 这是一份高中化学人教版 (新课标)必修2第三章 有机化合物第四节 基本营养物质教学演示ppt课件,共60页。PPT课件主要包含了有机化合物,第三章,第四节基本营养物质,油脂蛋白质,无机盐和水,葡萄糖,C6H12O6,麦芽糖,C12H22O11,纤维素等内容,欢迎下载使用。
高中人教版 (新课标)第一节 化学能与热能背景图ppt课件: 这是一份高中人教版 (新课标)第一节 化学能与热能背景图ppt课件,共60页。PPT课件主要包含了化学反应与能量,第二章,可逆反应,不可逆反应,氧化还原反应,非氧化还原反应,吸热反应,放热反应,放出热量,吸收热量等内容,欢迎下载使用。













