





第八章常见的酸碱盐8.3酸和碱的反应课件(科粤版九年级下册)
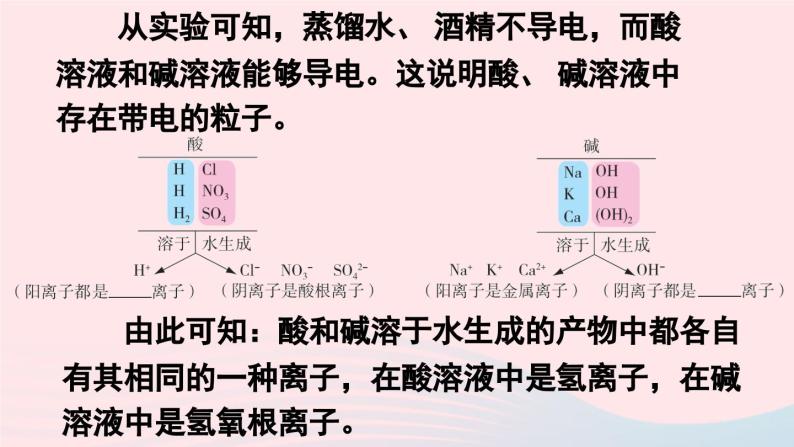
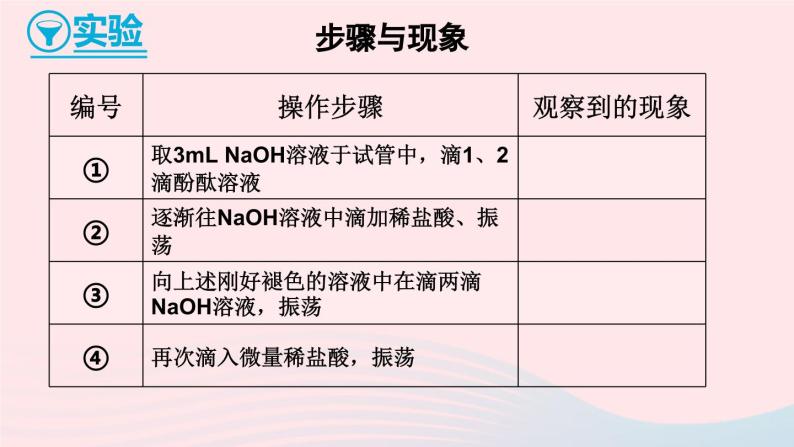
展开8.3 酸和碱的反应科粤版 九年级化学下册新课导入 从前面的学习中,我们已经知道酸、 碱各自有相似的化学性质,这是什么原因造成的呢? 先让我们观察一个实验。溶液的导电性【实验】在5只小烧杯中分别装有下表列出的溶液各100mL,再按图中装置进行实验,当闭合开关接通电源后,观察灯泡是否发亮。 从实验可知,蒸馏水、 酒精不导电,而酸溶液和碱溶液能够导电。这说明酸、 碱溶液中存在带电的粒子。 由此可知:酸和碱溶于水生成的产物中都各自有其相同的一种离子,在酸溶液中是氢离子,在碱溶液中是氢氧根离子。酸与碱的中和反应步骤与现象解释与结论 解释与结论 指示剂颜色说明碱溶液与滴入的酸溶液发生了化学变化,其反应原理用化学式表示如下:盐酸与氢氧化钠反应:HCl+NaOH=NaCl+H2O(酸) (碱) (盐) (水)酸跟碱生成盐和水的反应,叫做中和反应。下表归纳了酸和碱的主要化学性质: 变红变蓝不变色变红盐水金属盐水非金属盐水新盐新酸新盐新碱盐氢气上述酸和碱性质的许多变化中都有这样的特点: 参加反应的两种化合物互相交换成分生成另外两种化合物。像这类由两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应。 酸碱中和在人们的生产生活中有广泛的应用,主要事例有:1.改良酸性或碱性的土壤;2.废水处理;3.医药应用;4.调节溶液的酸碱性.中和反应的应用改良酸性或碱性的土壤 夏天的农户向放干的鱼塘底撒熟石灰,这是为了中和鱼塘底泥中过多的有机酸(同时达到杀菌消毒的目的),使放水后的鱼塘达到适合鱼苗生长的pH。 我们可以利用熟石灰的碱性中和土壤和某些水源的过多酸性,以减轻酸雨的危害。 如果废水中含有酸性物质 (如硫酸、 盐酸),我们必须先用碱性物质(如烧碱、 熟石灰) 将其中和成中性以后才能排放,否则会造成水体污染。废水处理 如果你被蚊虫叮咬,皮肤会出现红肿而疼痛,这是因为它们向你的皮肤 “注射”了“蚁酸”———甲酸。这时可以涂抹弱碱性的肥皂水、 小苏打水、稀氨水或清凉油以减轻疼痛。医药应用 在科学实验中,经常需要将溶液的pH控制在某一特定范围。当溶液的酸性或碱性太强或太弱时,可以加适当的碱或酸进行调节。调节溶液的酸碱性部分非金属氧化物能跟水化合生成酸,例如:SO2+H2O=H2SO3 SO3+H2O=H2SO4酸雨煤和石油燃烧后所产生的烟气中,含有二氧化硫和氮氧化物,排放到空气中被云层吸收,并经过化学作用形成酸雾,随同雨水下降便成为显酸性的雨水,若pH小于5.6,称为酸雨。酸雨的危害随堂练习1.中和反应在工农业生产和日常生活中有广泛的用途。下列应用一定与中和反应原理无关的是( )A.施用熟石灰改良酸性土壤B.服用含Al(OH)3的药物治疗胃酸过多C.用熟石灰和硫酸铜配置波尔多液D.用NaOH溶液洗涤石油产品中的残余硫酸C2.下列变化不能表明盐酸与氢氧化钠发生了反应的是( )A.向氢氧化钠溶液中加入盐酸后,混合溶液的温度升高B.向氢氧化钠溶液中加入盐酸后,混合溶液的质量增大C.向滴有酚酞的氢氧化钠溶液中加入盐酸后,红色褪去D.向氢氧化钠溶液中加入盐酸后,混合溶液的pH<7B3.家庭生活中一些常见物质的pH如下:D当我们被蚊虫叮咬后,蚊虫能在人的皮肤内分泌蚁酸(具有酸的性质),从而使皮肤肿痛。要减轻痛痒,应在叮咬处抹下列物质中的( )A.食醋 B.牛奶 C.食盐水 D.牙膏与肥皂水课后小结2. 酸和碱作用生成盐和水的反应叫做中和反应。3. 中和反应的实质是H+和OH-结合生成水。 H+ + OH- =H2O1. 酸 + 碱 → 盐 + 水2HCl + Ca(OH)2 = CaCl2 + 2H2OHCl + NaOH = NaCl + H2O









