







- 《水的电离和溶液的PH》第二课时课件+教学设计 课件 18 次下载
- 《水的电离和溶液的PH》第三课时课件+教学设计 课件 17 次下载
- 《盐类的水解》第二课时课件PPT+教学设计 课件 17 次下载
- 《盐类的水解》第三课时课件PPT+教学设计 课件 18 次下载
- 《盐类的水解》第四课时课件PPT+教学设计 课件 20 次下载
高中化学第三节 盐类的水解教学ppt课件
展开(人教版高中化学选择性必修1)
《盐类的水解》第一课时 教学设计
课题名 | 《盐类的水解》第一课时 |
教材分析 | 本节课是有关讲解盐溶液呈现不同酸碱性的原因,需要学生理解盐类水解的本质,特点和规律。为后面的影响盐类水解的因素,盐类水解的应用打基础。在高考中盐类水解是考察的重点内容,难度较大。 |
教学目标 | 宏观辨识与微观探析:掌握盐溶液呈现不同酸碱性的原因,理解盐类水解的本质,特点和规律。 证据推理与模型认知:掌握盐类水解的离子方程式的书写原则,会书写盐类水解的离子方程式。 科学探究与创新意识:能根据盐类水解理论判断盐溶液的酸碱性。 科学精神与社会责任:能根据盐类水解理论解释一些生活中的有关问题。 |
教学重点 | 盐类水解的本质,特点和规律,盐类水解的离子方程式的书写。 |
教学难点 | 盐类水解的本质,特点和规律。 |
教学方法 | 讲解,实验法 |
教学准备 | 教师准备:PPT、实验 学生准备:预习课本 |
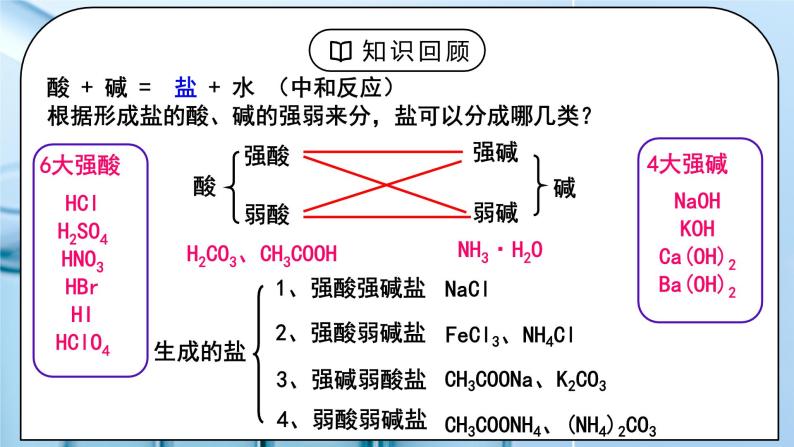
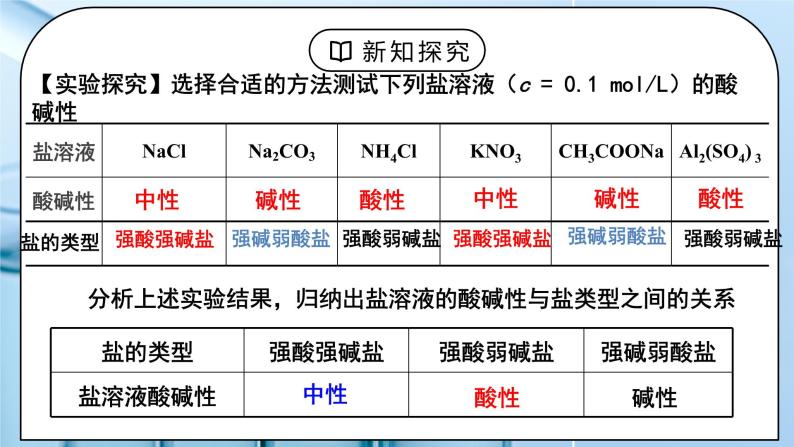
教学过程 | 一、新课导入 1.思考:Na2CO3是日常生活中常用的盐,俗称纯碱,常在面点加工时用与中和酸并使食物松软或酥脆,也常用于油污的清洗等。为什么Na2CO3可以被当作“碱”使用呢? 教师:酸 + 碱 = 盐 + 水 (中和反应) 根据形成盐的酸、碱的强弱来分,盐可以分成哪几类? 6大强酸:HCl H2SO4 HNO3 HBr HI HClO4 4大强碱:NaOH KOH Ca(OH)2 Ba(OH)2 学生:生成的盐:强酸强碱盐、强酸弱碱盐、强碱弱酸盐、弱酸弱碱盐 [设计意图]回顾酸碱中和反应的生成物盐,尝试按照酸碱强弱进行分类。 二、探究新知 1.一、盐溶液酸碱性 教师:【实验探究】选择合适的方法测试下列盐溶液(c = 0.1 mol/L)的酸碱性 分析上述实验结果,归纳出盐溶液的酸碱性与盐类型之间的关系 规律:谁强显谁性,同强显中性 例1:下列盐溶液中,呈酸性: ___________, 呈碱性:________。 ① FeCl3 ② NaClO ③ AgNO3 ④ Na2S ⑤ NH4I ⑥NaF⑦NH4ClO4 例2:等物质的量浓度的下列溶液,其pH由小到大的顺序是 ①CH3COONa ②NaOH ③NaNO3 ④HCl ⑤CH3COOH 盐溶液呈现不同酸碱性的原因: 纯水中:H2O H+ + OH– 当分别加入NaCl、NH4Cl、CH3COONa形成溶液后,请思考: (1)相关的电离方程式? (2)盐溶液中存在哪些粒子? (3)哪些粒子间可能结合(生成弱电解质)? (4)对水的电离平衡有何影响? (5)相关的化学方程式? 往水中加NaCl形成溶液: 往水中加NH4Cl形成溶液: 往水中加CH3COONa形成溶液: 学生:小结: [设计意图]知道盐溶液有酸碱性,并理解盐溶液呈现不同酸碱性的原因。
教师:1.定义:盐溶液中,盐电离出的弱离子与水电离的H+或OH-结合生成弱电解质(弱酸或弱碱)的反应,叫盐类的水解。 2.实质: 生成弱电解质,破坏、促进水的电离。 3.盐类水解的特点:可逆;吸热;一般微弱 4.水解的规律:(1)有弱才水解,谁弱谁水解; (2)越弱越水解,越稀越水解;(3)谁强显谁性,同强显中性。 例3:已知 Ka(HF) > Ka(CH3COOH) ,同温度下,等浓度的NaF和CH3COONa溶液,哪一个的pH大? 例4:等浓度的三种盐溶液KX,KY, KZ ,若它们的PH依次为 8,9,10, 则 HX, HY, HZ的酸性由强到弱的顺序是啥? 5.盐溶液酸碱性的判断 ①根据”谁强显谁性,同强显中性“判断 ②弱酸弱碱盐溶液的酸碱性: ③酸式盐溶液的酸碱性: (1)强酸的酸式盐溶液显酸性,如NaHSO4,因为强酸的酸式根只电离不水解。 NaHSO4 = Na+ + H+ + SO42- (2)弱酸的酸式盐酸碱性: 由弱酸酸式根水解程度和电离程度的相对大小决定 弱酸酸式盐溶液的酸碱性取决于其电离程度和水解程度的相对大小:若水解程度大于电离程度,则溶液呈碱性。 如:NaHCO3、NaHS、Na2HPO4溶液等。 若电离程度大于水解程度,则溶液呈酸性。 如:NaHSO3、KHC2O4、NaH2PO4溶液等。 6、盐类水解的离子方程式 书写时方程式一般用“ ”符号;通常不用“↓”、“↑”符号,但完全双水解要用“=”,标“↑”、“↓”。 ① 多元弱酸根离子分步水解,水解程度第一步最大,水解方程式分步书写。 ② 多元弱碱盐的水解方程式一步完成 ③完全双水解: 即弱酸阴离子与弱碱阳离子水解相互促进,水解程度较大,能反应彻底。 能发生完全双水解反应的离子组合: Al3+ 与 AlO2-、CO32-、HCO3- 、 HS-、S2-、SiO32- Fe3+ 与 AlO2-、CO32-、HCO3- NH4+ 与 SiO32-、AlO2- 学生:练习1、下列物质分别加入到水中,因水解而使溶液呈酸性的是( )A、硫酸 B、NaOH C、硫酸铝 D. 碳酸钠 练习2、在Na2S溶液中,c (Na+) 与 c (S2–) 之比值( )于2。 A、大 B、小 C、等 D、无法确定 练习3、① PH均为4的醋酸溶液和氯化铵溶液中,水电离出的OH–分别是多少? ② PH均为9的NaOH溶液和醋酸钠溶液中,水电离出的OH–分别是多少? 练习4、Ka(HF) > Ka(CH3COOH) ,等PH的NaF和CH3COONa溶液中Na+的浓度哪个更大? 练习5:判断以下水解方程式是否正确 练习6、下列水解的离子方程式正确的( ) A.CO32-+2H2O ⇌CO2 ↑+2OH- B.I-+H2O ⇌HI+OH- C.SO32-+2H2O ⇌H2SO3+2OH- D.Fe3++3H2O ⇌Fe(OH)3+3H+ 练习7、写出水解反应的离子方程式。 ①NH4HCO3 ②Al2(SO4)3 ③NaF ④Na2S ⑤Fe3+ 与 AlO2- ⑥Al3+ 与S2- [设计意图]理解盐类水解的定义,特点和规律,能书写盐类水解的离子方程式 |
板书设计 | 一、盐溶液酸碱性 规律:谁强显谁性,同强显中性 二、盐类的水解: 1.定义: 2.实质: 3.盐类水解的特点: 4.水解的规律: 有弱才水解,谁弱谁水解; 越弱越水解,越稀越水解; 谁强显谁性,同强显中性。 5.盐溶液酸碱性的判断 6.盐类水解的离子方程式 |
课后作业 |
练习册上相关习题 |
教学反思 | 亮点:本节课详细阐述了盐类有酸碱性的原因,通过实验和列表总结的方法帮助学生理解。 课堂教学建议:本节课难度较大,教师应根据学生的学习情况采用边讲解边练习的模式进行学习。 |
高中化学人教版 (2019)选择性必修1第一节 反应热优质教学ppt课件: 这是一份高中化学人教版 (2019)选择性必修1第一节 反应热优质教学ppt课件,文件包含《反应热》第一课时课件pptx、《反应热》第一课时教学设计docx等2份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
高中人教版 (2019)第二节 电解池优秀教学ppt课件: 这是一份高中人教版 (2019)第二节 电解池优秀教学ppt课件,文件包含《电解池》第一课时课件pptx、《电解池》第一课时教学设计docx等2份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
高中化学人教版 (2019)选择性必修1第三节 盐类的水解教学ppt课件: 这是一份高中化学人教版 (2019)选择性必修1第三节 盐类的水解教学ppt课件,文件包含《盐类的水解》第四课时课件pptx、《盐类的水解》第四课时教学设计docx等2份课件配套教学资源,其中PPT共24页, 欢迎下载使用。














