




配制溶液PPT课件免费下载
展开一、【基础巩固】
在室温下,小乐完成了如下实验,若固体A(不含结晶水)溶于水既不吸热,也不放热,且实验过程中,不考虑水的蒸发。则下列说法正确的是( )
A.在室温下,溶液①为饱和溶液B.在t ℃时,A的溶解度一定为50克C.溶液②和溶液④的溶质质量分数相同D.溶液③和溶液④的溶液质量相同
【点拨】在室温下,溶液①中加入5 g A,部分溶解,可见溶液①是不饱和溶液,A不符合题意;加热到t ℃时,溶液②中的A物质全部溶解,但A的溶解度不一定为50 g,B不符合题意;溶液②和溶液④都是室温下的饱和溶液,所以两者的溶质质量分数相同,C符合题意;溶液③→溶液④,物质A析出,溶液质量不相同,D不符合题意。
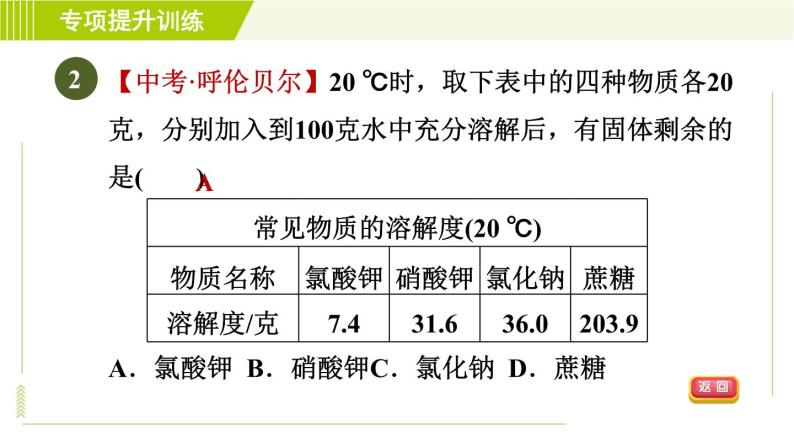
【中考·呼伦贝尔】20 ℃时,取下表中的四种物质各20克,分别加入到100克水中充分溶解后,有固体剩余的是( )A.氯酸钾 B.硝酸钾C.氯化钠 D.蔗糖
下列关于溶解度的说法,不正确的是( )A.溶解度能够表示物质在一定温度下溶解性的强弱程度B.在同温度、同溶剂下,同物质的饱和溶液一定比不饱和溶液的质量分数大C.溶液溶解过程中,当溶液底部存在着未溶解的固体物质时,该溶液一定是饱和溶液D.饱和溶液恒温蒸发部分溶剂后溶质的质量分数一定不变
【点拨】物质溶解性的强弱程度是用溶解度来表示的,故A正确;同一温度、相同溶剂和溶质,饱和溶液溶质质量分数最大,故B正确;物质溶解过程中,当溶液底部存在着未溶解的固体物质时,该溶液不一定是饱和溶液,固体物质的质量必须不再减少才行,故C错误;
二、【整体提升】
下列有关溶液的说法,不正确的是( )A.蔗糖溶液是均一的、稳定的混合物B.硝酸钾在20 ℃溶解度是31.6 g,则100 g硝酸钾溶液中含有硝酸钾31.6 gC.打开汽水瓶盖时,汽水会自动喷出来,说明气体的溶解度与压强有关D.冷却或蒸发溶剂都能使接近饱和的硝酸钾溶液达到饱和
【点拨】溶液是具有均一性和稳定性的混合物,故A正确;由溶解度的概念可知,硝酸钾在20 ℃时的溶解度是31.6 g,则在该温度下,131.6 g硝酸钾饱和溶液中含有硝酸钾31.6 g,故B错误;打开汽水瓶盖,瓶内压强变小,二氧化碳的溶解度减小,故汽水会自动喷出来,故C正确;硝酸钾的溶解度随着温度的升高而增大,随着温度的降低而减小,所以冷却或蒸发溶剂都能使接近饱和的硝酸钾溶液达到饱和,故D正确。
20 ℃时,食盐的溶解度为36克。将20克食盐放入50克水中充分搅拌后,所得溶液一定是________(填“饱和”或“不饱和”)溶液。其中含有________克固体食盐不溶解。溶液的质量为________克。溶液中溶质的质量分数为________。溶液中溶质、溶剂、溶液的质量之比为____________。
【点拨】20 ℃时,食盐的溶解度为36 g。其含义是20 ℃时,100 g水中最多溶解36 g氯化钠,溶液达到饱和状态。将20 g食盐放入50 g水中充分搅拌后,最多能溶解18 g,所得溶液一定是饱和溶液;其中还有20 g-18 g=2 g固体食盐不溶解;溶液的质量为18 g+50 g=68 g。
氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )
A.硝酸钾的溶解度比氯化铵的大B.a ℃时,氯化铵与硝酸钾溶液中溶质的质量分数相等C.将20 ℃的硝酸钾不饱和溶液升温可以变为饱和溶液D.40 ℃时,50 g水中加入50 g硝酸钾,充分搅拌,得到质量分数为39.02%的硝酸钾溶液
【点拨】在比较物质的溶解度时,需要指明温度,故A错误;未指明t ℃时氯化铵与硝酸钾溶液是否为饱和溶液,所以两溶液中溶质的质量分数大小不能确定,故B错误;硝酸钾的溶解度随温度的升高而增大,所以将20 ℃的硝酸钾不饱和溶液降温可以变为饱和溶液,故C错误;
依据实验和溶解度曲线回答问题。下列4只盛有100 g水的烧杯,t1 ℃时,向①②中分别加入20 g、30 g固体X;t2 ℃时,向③④中分别加入50 g、60 g固体Y,充分溶解。
①中溶液的质量为( )A.20 g B.80 g C.120 g D.125 g
【点拨】由溶解度曲线图可知,t1 ℃时X的溶解度为25 g,该温度下100 g水中最多能溶解X 25 g,溶液达到饱和状态;t1℃时,向①中加入20 g固体X,能全部溶解,形成溶液的质量为20 g+100 g=120 g。
甲、乙两种固体的溶解度曲线如图所示,相关分析正确的是( )
A.M点表示t3 ℃时,乙饱和溶液溶质质量分数为20%B.N点表示t1 ℃时,甲和乙的饱和溶液溶质质量分数相同C.t2 ℃时,甲、乙饱和溶液降低温度,甲先析出晶体D.t3 ℃时,溶剂质量均为100 g的甲、乙饱和溶液降温至t1 ℃,乙溶液析出的固体更多
乙的溶解度均随着温度降低而减小,因此将t2 ℃时两者饱和溶液降低温度,甲、乙会同时析出晶体,没有先后之分,故C错误;t3 ℃时,溶剂质量均为100 g的甲、乙饱和溶液降温至t1 ℃,甲溶液析出的固体更多,故D错误。
【中考·张家界】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲和丙的溶解度相等B.降温可使丙物质的不饱和溶液变成饱和溶液C.t1 ℃时,甲、乙和丙各30 g分别加入100 g水中,均形成饱和溶液D.t2 ℃时,将15 g甲物质加入50 g水中,再降温到t 1℃时,所得溶液溶质的质量分数不变
【点拨】在比较物质的溶解度大小时,需要指明温度,故A错误;丙物质的溶解度随温度的降低而增大,所以升温可使丙物质的不饱和溶液变成饱和溶液,故B错误;t1 ℃时,乙物质的溶解度大于30 g,甲、丙物质的溶解度等于30 g,所以甲、乙和丙各30 g分别加入100 g水中,甲、丙形成饱和溶液,乙形成不饱和溶液,故C错误;t2 ℃时,将15 g甲物质加入50 g水中,再降温到t1 ℃时,甲物质的溶解度是30 g,所以所得溶液溶质的质量分数不变,故D正确。
二、【拓展培优】
如图是甲、乙的溶解度曲线,下列说法不正确的是( )
A.t1 ℃时,乙的溶解度大于甲的溶解度B.t1 ℃时甲和乙的饱和溶液升高到t2 ℃时,溶质质量分数相等C.降低温度能使接近饱和的甲溶液变为饱和溶液D.t3 ℃时,分别用100 g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
【点拨】由溶解度曲线可知,t1 ℃时,乙的溶解度大于甲的溶解度,故A正确;t1 ℃时甲和乙的饱和溶液升温到t2 ℃时,甲、乙溶质质量分数不变,甲小于乙,故B错误;降低温度能使接近饱和的甲溶液变为饱和溶液,因为甲固体物质的溶解度随温度升高而增大,故C正确;t3 ℃时,分别用100 g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量,因为在该温度下,甲的溶解度大于乙,故D正确。
水是最常见的溶剂。(1)下列溶液用水作溶剂的是________(填字母序号)。a.生理盐水 b.碘酒 c.葡萄糖溶液
【点拨】生理盐水中溶质是氯化钠,溶剂是水;碘酒中溶质是碘,溶剂是酒精;葡萄糖溶液中溶质是葡萄糖,溶剂是水。
(2)如图1是甲、乙、丙三种固体物质的溶解度曲线。请回答:
①t2℃时,将甲、丙的饱和溶液分别降温至t1℃,仍然饱和的是________的溶液。
【点拨】t2℃时,将甲、丙的饱和溶液分别降温至t1℃,甲的溶解度变小,析出晶体,仍然是饱和溶液,丙的溶解度变大,变为不饱和溶液;
②欲从含有少量乙的甲的饱和溶液中提纯甲,可采用________结晶的方法。
【点拨】由于甲的溶解度受温度影响较大,所以提纯甲的方法是降温结晶;
③某温度下,为使图2试管中丙的固体溶解,可向烧杯中加入________(填字母)。A.氢氧化钠固体 B.硝酸铵固体 C.氯化钠固体
【点拨】某温度下,为使图2试管中丙的固体溶解,则需要降低温度,故可向烧杯中加入硝酸铵固体,因为硝酸铵固体溶于水吸收热量而导致溶液的温度降低。
【中考·营口】如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
(1)t3 ℃时,甲、乙、丙三种物质的溶解度大小关系是_____________(用“甲”“乙”或“丙”及“>”“<”或“=”表示)。
【点拨】通过分析溶解度曲线可知,t3 ℃时,甲、乙、丙三种物质的溶解度大小关系是甲>乙>丙。
(2)t2 ℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为________(填最简整数比)。
【点拨】t2 ℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为1∶2。
(3)欲配制相同质量分数的乙、丙饱和溶液,应保持温度在________℃。
【点拨】t1 ℃时,乙、丙物质的溶解度相等,所以欲配制相同质量分数的乙、丙饱和溶液,应保持温度在t1 ℃。
电生磁PPT课件免费下载: 浙教版初中科学八年级下册课文《电生磁》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。
月相PPT课件免费下载: 浙教版初中科学七年级下册课文《月相》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。
电能PPT课件免费下载: 浙教版初中科学九年级上册课文《电能》,完整版PPT课件免费下载,优秀PPT背景图搭配,精美的免费ppt模板。轻松备课,欢迎免费下载使用。