



高中化学人教版 (新课标)选修5 有机化学基础第一节 醇 酚课前预习课件ppt
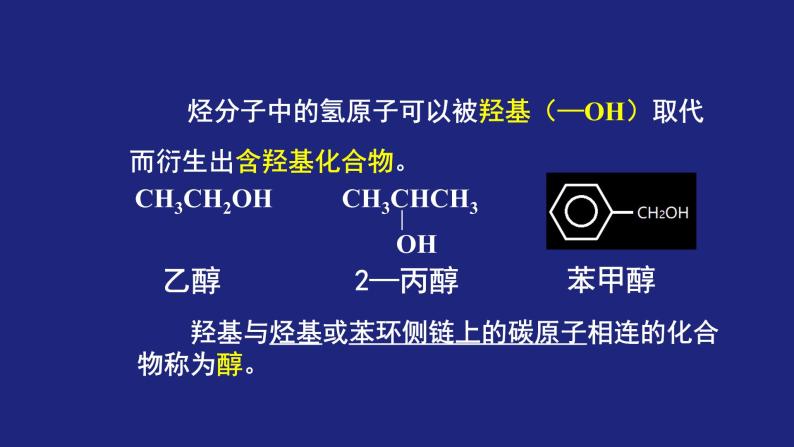
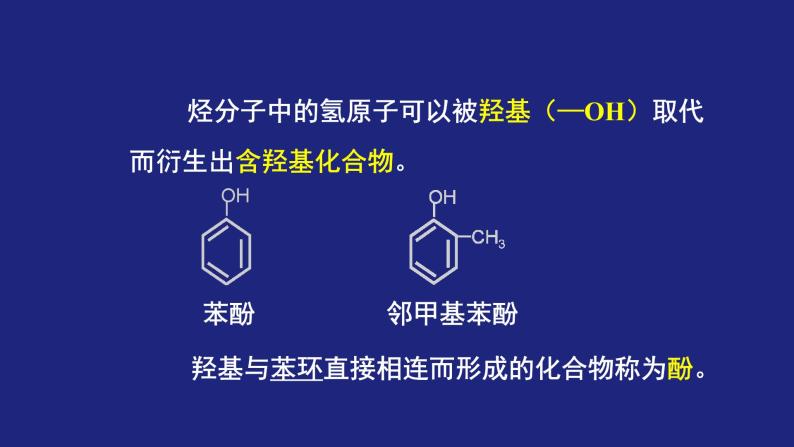
展开烃分子中的氢原子可以被羟基(—OH)取代而衍生出含羟基化合物。
羟基与烃基或苯环侧链上的碳原子相连的化合物称为醇。
羟基与苯环直接相连而形成的化合物称为酚。
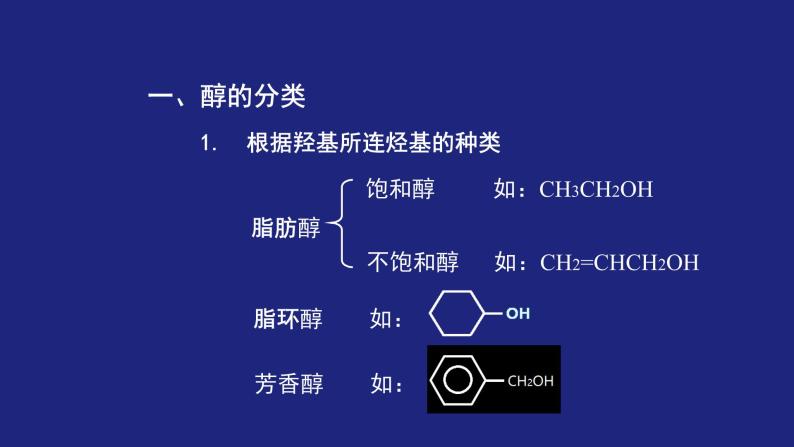
1. 根据羟基所连烃基的种类
饱和醇 如:CH3CH2OH
不饱和醇 如:CH2=CHCH2OH
脂环醇 如:
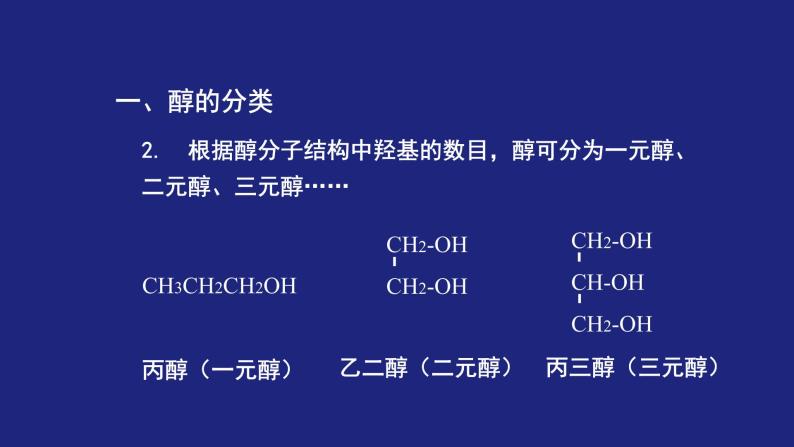
2. 根据醇分子结构中羟基的数目,醇可分为一元醇、二元醇、三元醇……
CH3CH2CH2OH
乙二醇 和 丙三醇 都是无色、粘稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。例如,汽车用乙二醇防冻液;丙三醇(俗称甘油)吸湿性强,常用于配制化妆品。
CnH2n+1OH 或 CnH2n+2O
选含与—OH相连碳原子的最长碳链为主链
从距离—OH最近的一端给主链碳原子编号定位
羟基位置用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。
2 3
取代基位置— 取代基名称 — 羟基位置— 母体名称
1,2,3—丙三醇或 丙三醇
下表是相对分子质量相近的醇与烷烃的沸点比较
相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃的沸点。
原因:由于醇分子中羟基的氧原子与另一醇分子羟基的氢原子间存在着相互吸引作用,这种吸引作用叫氢键。(分子间形成了氢键)
下表是含相同碳原子数不同羟基数的醇的沸点比较
由于羟基数目增多,使得分子间形成的氢键增多、增强。
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,2—丙二醇,1,2—丙二醇的沸点高于1—丙醇
沸点随分子内羟基数目的增多而增大
1. 与金属钠的反应:
乙醇钠
三、醇类化学性质 — 以乙醇为例
乙醇分子中羟基上的氢不如水分子中的氢活泼。
羟基受乙基的影响而活性减弱
醇的化学性质主要由羟基(-OH)官能团决定。
在反应中,羟基的O-H键和C-O键容易断裂。
CH3CH2OH CH2=CH2 + H2O
①放入碎瓷片的作用?②浓硫酸的主要作用?③酒精与浓硫酸的体积比为?④温度计的位置?
⑤为何使液体温度迅速升到170℃?⑥混合液颜色如何变化?为什么?⑦有何杂质气体?如何除去?⑧用什么方法收集乙烯气体?
① 放入碎瓷片的作用?
防止暴沸
② 浓硫酸的主要作用?
催化剂和脱水剂
③ 酒精与浓硫酸的体积比为?
为了保证有足够的脱水性,硫酸要用98%的浓硫酸,酒精要用无水酒精,此时酒精与浓硫酸体积比以1:3为宜。
温度计感温泡要置于反应物的中央位置,因为需要测量的是反应物的温度。
⑤ 为何使液体温度迅速升到170℃?
因为无水酒精和浓硫酸混合物在170℃的温度下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。
⑥ 混合液颜色如何变化?为什么?
烧瓶中的液体逐渐变黑。因为浓硫酸的脱水性,使乙醇脱水炭化。
⑦ 有何杂质气体?如何除去?
由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通入10%NaOH溶液洗气除杂。
⑧ 用什么方法收集乙烯气体?
因为乙烯难溶于水,密度比空气密度略小,应选用排水集气法收集乙烯。
3. 取代反应 ①酯化反应: 断键位置:酸的羧基断裂C-O键,醇的羟基断裂O-H键
浓硫酸作催化剂和吸水剂
3. 取代反应 ②与氢溴酸在加热条件下的取代反应
断键位置: C-O键断裂,羟基被溴原子取代。
3. 取代反应 ③ 乙醇的分子间脱水成醚 断键位置:其中一个醇断裂C-O键,脱去了羟基, 另一个醇的羟基断裂O-H键,脱去H。
除了燃烧反应外,醇类还可以被其他适宜的氧化剂氧化。
事故调查显示:大约50%-60%的交通事故与酒后驾驶有关。此反应被用于交警判断驾驶员是否酒后驾车的方法。
实验:把灼热的铜丝插入乙醇中,观察铜丝颜色变化, 并小心扇闻试管中液体产生的气味。
有刺激性气味的物质产生
CH3CH2OH
与羟基相连的碳上有2个氢原子的醇催化氧化产生醛基
与羟基相连的碳上有1个氢原子的醇催化氧化产生羰基
连有羟基的碳原子上要有氢原子
从结构上看,醇能发生催化氧化的前提条件:
思考:下列醇能否发生催化氧化反应?产物是什么?
不能发生催化氧化反应
可以发生催化氧化反应,生成丙酮
小结:乙醇在各化学反应中化学键断裂的位置
课 后 作 业 题
下列物质中,不属于醇类的是 ( )
C3H7OH B. C6H5CH2OHC. C6H5OH D.
下列各醇,能发生催化氧化的是( )
CH3—C—CH2OH CH3
CH3 ∣B. CH3—C—OH ∣ CH3
C.CH3—CH—CH3 ∣ OH
CH3 ∣D.C6H5—C—CH3 ∣ OH
愿同学们振奋精神、志存高远、只争朝夕、不负韶华,创造出属于自己的不凡!
人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯课堂教学ppt课件: 这是一份人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯课堂教学ppt课件,共38页。PPT课件主要包含了学习目标,烃基不同,羧基数目,饱和一元羧酸通式,乙酸的酸性,CH3COOH,H2CO3,科学探究1,酯化反应,科学探究2等内容,欢迎下载使用。
高中人教版 (新课标)第二节 醛评课课件ppt: 这是一份高中人教版 (新课标)第二节 醛评课课件ppt,共36页。PPT课件主要包含了学习目标,乙醛的物理性质,乙醛的组成和结构,醛基上的氢,甲基上的氢,学与问,乙醛的化学性质,葡萄糖的结构式,二氧化反应,1配制银氨溶液等内容,欢迎下载使用。
人教版 (新课标)选修5 有机化学基础第三节 卤代烃教学演示ppt课件: 这是一份人教版 (新课标)选修5 有机化学基础第三节 卤代烃教学演示ppt课件,共24页。PPT课件主要包含了气雾剂,1分子式,C2H5Br,2结构式,3结构简式,4电子式,峰面积之比为23,存在两组峰,溴乙烷的结构特点,溴乙烷的化学性质等内容,欢迎下载使用。













