衡阳市第一中学2023届高三下学期5月月考化学试卷(含答案)
展开一、单选题
1.2022年11月《联合国气候变化框架公约》第二十七次缔约方大会(COP27)在埃及举行,会议主题为“实施(TgetherFrImplementatin)”。下列说法正确的是( )
A.燃煤中添加生石灰能有效吸收,实现碳中和
B.采取“静电除尘”可提高空气质量
C.空气中的含量越高越有利于人体健康
D.易产生“光化学烟雾”,可用碱性物质吸收
2.下列相关的化学用语正确的是( )
A.的电子式为
B.苯的实验式:
C.乙烯的结构简式:
D.分子的比例模型:
3.设为阿伏加德罗常数的值。下列叙述正确的是( )
A.甲醇中含有键的数目为
B.常温常压下,中含有的质子数和中子数均为
C.和充分反应后的混合气体中原子数小于
D.25℃时,的溶液中含有的数目为
4.下列有关离子方程式的书写正确的是( )
A.溶液中滴加稀氨水:
B.溶液刻蚀电路铜板:
C.溶于NaOH溶液:
D.稀硫酸滴入溶液中:
5.已知X、Y、Z、W为核电荷数依次增大的前20号主族元素,且位于不同周期,其形成的某种物质的结构如图,该物质的水溶液显酸性。下列说法正确的是( )
A.该化合物的焰色试验呈黄色
B.Z的简单气态氢化物的热稳定性比Y强
C.Z的最高价氧化物对应的水化物为强酸
D.Y与其他三种元素均可形成两种或两种以上的二元化合物
6.下图是我国科研工作者研究与作用最终生成与的物质相对能量-反应进程曲线。下列叙述错误的是( )
A.中间体比更稳定
B.该反应进程中的最大能垒(活化能)为
C.生成的过程中有极性键的断裂和形成
D.总反应的热化学方程式为
7.利用3-苯基丙酸催化脱氢制备异肉桂酸的反应如下所示,下列叙述错误的是( )
A.上述制备过程属于氧化反应
B.3-苯基丙酸的分子式为
C.异肉桂酸分子中最多有9个碳原子共面
D.异肉桂酸最多与发生加成反应
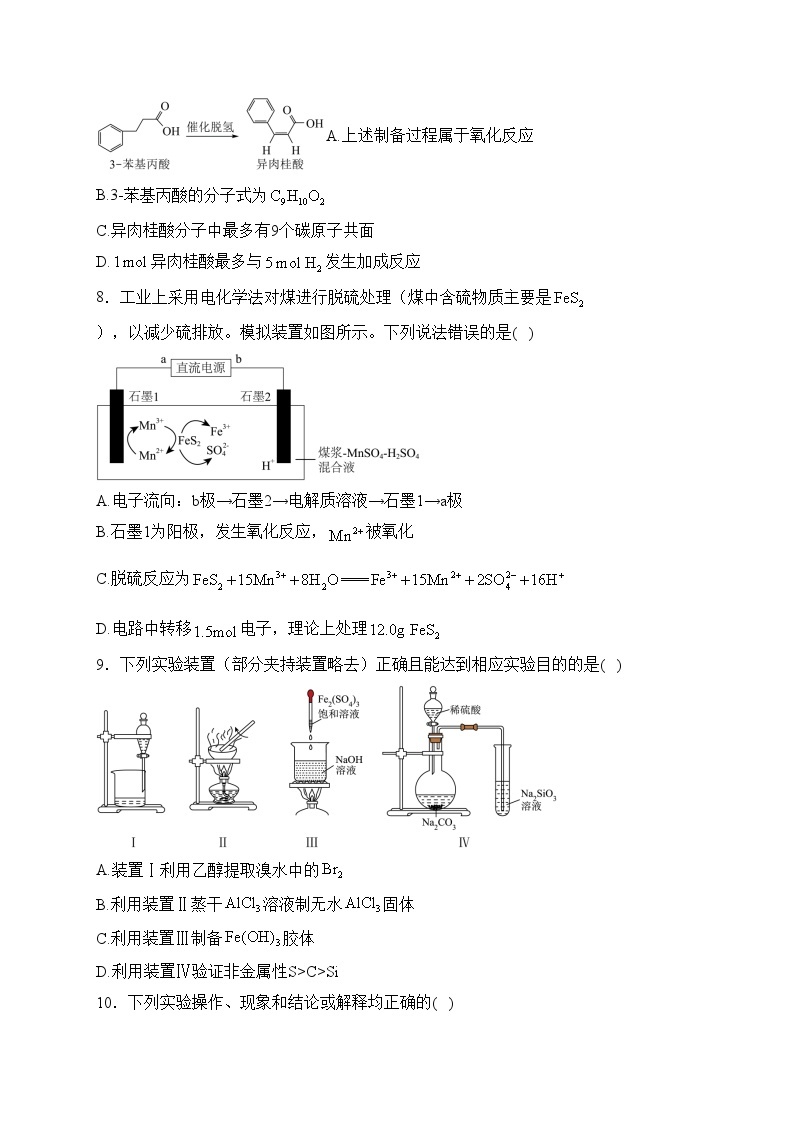
8.工业上采用电化学法对煤进行脱硫处理(煤中含硫物质主要是),以减少硫排放。模拟装置如图所示。下列说法错误的是( )
A.电子流向:b极→石墨2→电解质溶液→石墨1→a极
B.石墨1为阳极,发生氧化反应,被氧化
C.脱硫反应为
D.电路中转移电子,理论上处理
9.下列实验装置(部分夹持装置略去)正确且能达到相应实验目的的是( )
A.装置Ⅰ利用乙醇提取溴水中的
B.利用装置Ⅱ蒸干溶液制无水固体
C.利用装置Ⅲ制备胶体
D.利用装置Ⅳ验证非金属性S>C>Si
10.下列实验操作、现象和结论或解释均正确的( )
A.AB.BC.CD.D
11.乙烯水合法是工业制乙醇的方法:,该反应在密闭容器中进行,下列说法错误的是( )
A.恒温恒容,充入,的转化率增大
B.若升高温度,平衡常数减小,则该反应
C.压缩容积,活化分子百分数增大,反应速率加快
D.恒温恒压,通入,平衡向左移动
12.以含锌废液(主要成分为,含少量的)为原料制备的实验流程如下。下列说法不正确的是( )
A.1ml过二硫酸钠()中含有σ键数9
B.氧化除锰后的溶液中一定存在:
C.调节pH时试剂X可以选用Zn、ZnO、等物质
D.氧化除锰过程中生成的离子方程式:
13.含硼化合物的两种晶体如图所示。下列叙述正确的是( )
已知:甲中晶胞的边长为,为阿佛加德罗常数的值。图甲、图乙对应的晶体熔点依次为2700℃、830℃。
A.图乙晶体的化学式为
B.图甲、图乙对应的晶体都是离子晶体
C.图甲中B原子和N原子之间的最近距离为
D.图甲中,B原子填充在由N原子构成的四面体中
14.是易溶二元弱碱(,),常温下,向溶液中通入,溶液中随[]变化的曲线如图所示,下列说法错误的是( )
A.溶液:
B.当时,
C.水的电离程度:
D.当时,大于3.5
二、实验题
15.铁及其化合物在生活、生产中有着广泛应用。(易升华,易水解)是常见的化学试剂,某学习小组开展了与相关的系列实验,请回答下列问题:
Ⅰ.铁粉制备(实验装置如图所示)
(1)基态的电子排布式为________________。A中实验室制备的离子方程式为___________________________________________;
(2)装置中F的作用:____________________________;
Ⅱ.在水溶液中能够水解产生胶团从而具有净水作用。
(3)胶团如图所示,在静电吸附作用下,胶团可以除去废水中含价的砷微粒是_______________。(已知:价砷元素存在形式为)
(4)为探究和添加助凝剂对净水效果的影响,①实验小组选取一种含价的砷微粒废液进行探究实验。已知:净水效果可用相同时间内废液中含价的砷微粒变化来衡量。废液中砷微粒越高,代表废液污染越严重。
②实验结论一:通过1、2、3组实验,发现随着增大,净水效果依次增强。减小,净水效果减弱的原因是______________________________________。
③实验结论二:添加助凝剂能够显著提高净水效果。该实验结论成立的判断依据是______________________。(用表中数据表示)
Ⅲ.(5)①可与噻吩()和吡咯()形成配位化合物。噻吩、吡咯是类似于苯的芳香化合物,环中的五个原子形成了大键。噻吩难溶于水,吡咯能溶于水,原因是吡咯能与水形成分子间_______________________,而噻吩不能。
②一个立方体结构的晶胞如图所示,已知阿伏加德罗数值为,的晶体密度为,则晶胞的边长为_____________________(用含的代数式表示)。
16.运用化学反应原理研究合成氨反应有重要意义。请回答下列问题,
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。,该反应在低温下___________(“能”或“不能”)自发进行。
(2)已知在T℃时,反应的平衡常数K=0.5,相关化学键键能数据如表:
①T℃时,的ΔH=___________。
②T℃时,在1L密闭容器中进行合成氨反应,一段时间后,测得的物质的量分别为4ml、2ml、4ml,则此时反应___________(填“>”“<”“=”或“不能确定”)。
(3)已知合成氨反应的速率方程为:为反应速率常数。在合成氨过程中,需要不断分离出氨,该操作的目的是________________。
(4)以氨为原料生产尿素的方程式为。
①为进一步提高的平衡转化率,下列措施能达到目的的是___________(填字母)。
A.增大的浓度
B.增大压强
C.及时转移生成的尿素
D.使用更高效的催化剂
②尿素的合成分两步进行:
a.
b.
第一步反应速率快,可判断活化能较大的是___________(填“第一步”或“第二步”)。
③某实验小组为了模拟工业合成尿素,在恒温恒容的真空密闭容器中充入一定量的和发生反应:,反应过程中的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数___________(已知:分压=总压×体积分数)。
三、填空题
17.镍、钴元素在锂电池材料和国防工业方面应用广泛。一种利用酸浸出法从冶金厂废炉渣(含Ni、C及少量Cu、Mg、Ca的化合物)中提取镍和钴的工艺流程如图:
已知:ⅰ.;
ⅱ.在水中的溶解度随温度升高明显增大,不溶于乙醇和苯。
回答下列问题:
(1)“酸浸渣”主要成分的名称为_______________________________。
(2)基态C原子的核外M层电子排布式为_______________。
(3)“除铁”的离子方程式为________________________________。
(4)“除钙镁”时,pH不宜过低的原因是___________________________________。和沉淀完全。时,溶液中最小为____________ml·L-1
(5)“萃取”原理为(有机相)(有机相)。“反萃取”时为促进的转移,应选择的实验条件或采取的实验操作有①_____________;②多次萃取。
(6)获得(s)的“一系列操作”中洗涤产品可选用_________(填字母标号)试剂。
a.冷水
b.乙醇
c.苯
18.化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合成该化合物的路线如下图所示:
已知:Ⅰ.G的结构简式为
Ⅱ.
(1)反应①的反应条件为____________________。
(2)C中碳原子的杂化类型为_____________。
(3)E中官能团的名称为________,反应F→G的反应类型为__________。
(4)E与足量的完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为______________。
(5)已知N为催化剂,则的化学方程式为_______________________。
(6)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有________种。
①苯环上只有两个取代基;
②能与Na反应生成;
③能与银氨溶液发生银镜反应。
(7)根据上述信息,设计以苯酚和为原料,制备的合成路线_____(无机试剂任选)。
参考答案
1.答案:B
解析:A.燃煤中添加生石灰可以减少硫的氧化物的排放,可减少污染,但不能有效吸收,实现碳中和,A错误;
B.采取“静电除尘”可除去空气中的粉尘,提高了空气质量,B正确;
C.由空气的成分可知,臭氧不是空气的主要成分,且本身具有强氧化性,有毒,空气中臭氧含量越高,越不有利于人体健康,C错误;
D.不会产生“光化学烟雾”,其易形成酸雨,可用碱性物质吸收,而氮的氧化物易产生“光化学烟雾”,可用碱性物质吸收,D错误;
故答案为:B。
2.答案:B
解析:A.的电子式为,A错误;
B.苯的化学式为:,苯的实验式:CH,B正确;
C.乙烯的结构简式是,C错误;
D.分子碳原子和氧原子大小比例颠倒,实际应为C原子半径略大于O原子的,D错误;
故选B。
3.答案:B
解析:A.甲醇结构简式为,甲醇物质的量为1ml,含有键的数目为3,A错误;
B.常温常压下,的物质的量为0.1ml,每个含有10个质子和10个中子,故含有的质子数和中子数均为,B正确;
C.结合原子守恒,和充分反应后的混合气体中原子数等于,C错误;
D.25℃时,的溶液中含有的数目为,D错误;
故选B。
4.答案:D
解析:A.溶液中滴加稀氨水离子方程式为:,A错误;
B.溶液刻蚀电路铜板离子方程式为:,B错误;
C.溶于NaOH溶液离子方程式为:,C错误;
D.稀硫酸滴入溶液中离子方程式为:,D正确;
故选D。
5.答案:D
解析:A.该化合物含有K元素,焰色试验是紫色,A错误;
B.非金属性,故的热稳定性比差,B错误;
C.Z的最高价氧化物对应的水化物为,磷酸为弱酸,C错误;
D.O与H可形成,O与P可形成,O与K可形成,D正确;
故选D。
6.答案:B
解析:A.由图可知,中间体比能量更低,故更稳定,A正确;B.过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,峰值越小则活化能越小;该反应进程中的最大能垒(活化能)为,B错误;C.生成的过程中有碳氢键的断裂和氢氧键的生成,故有极性键的断裂和形成,C正确;
D.由图可知,总反应为氧化镁和甲烷反应生成镁和甲醇,反应放热,其热化学方程式为,D正确;
故选B。
7.答案:D
解析:A.加氢为还原反应,去氢为氧化反应,上述制备为去氢过程,属于氧化反应,A正确;B.3-苯基丙酸的分子式为,B正确;
C.苯环所连接的原子和碳碳双键所连接的原子均为平面结构,且单键可以旋转,则异肉桂酸分子中最多有9个碳原子共面,C正确;
D.1ml苯环可以3ml氢气发生加成反应,1ml碳碳双键可以和1ml氢气发生加成反应,羧基不能发生加成反应,1ml异肉桂酸最多与4ml发生加成反应,D错误;
故选D。
8.答案:A
解析:A.电子流向:b极→石墨2,石墨1→a极,电解质溶液无电子流动,A错误;
B.石墨1为阳极,发生氧化反应,被氧化,B正确;
C.脱硫反应为,C正确;
D.由图可知1ml氧化为和,电路中转移电子为(1+7×2)ml=15ml电子,电路中转移1.5ml电子,则处理的物质的量为0.1ml,处理的质量为0.1ml×120g/ml=12.0g,D正确;
故答案为:A。
9.答案:D
解析:A.装置Ⅰ中,分液漏斗的尖端没有紧靠烧杯内壁,缺乙醇与水混溶,不能用乙醇提取溴水中的溴,A不符合题意;
B.利用装置Ⅱ直接蒸干溶液时由于氯化铝会水解而不能制得无水固体,应在氯化氢气流中加热,B不符合题意;
C.利用装置Ⅲ制备胶体时,应该将饱和溶液滴入沸腾的蒸馏水中,而不能滴入NaOH溶液中,C不符合题意;
D.元素的非金属性越强,其最高价含氧酸的酸性就越强。将硫酸滴入溶液中发生复分解反应;反应产生的气体通入溶液中,发生反应:,说明酸性:,从而证明元素的非金属性:S>C>Si,D正确;
故合理选项是D。
10.答案:D
解析:A.稀硝酸具有强氧化性,可以把亚硫酸钠氧化为硫酸钠,如果过氧化钠与二氧化硫反应生成亚硫酸钠,加入稀硝酸后也能被硝酸氧化成硫酸钠,无法证明过氧化钠与反应生成了硫酸钠,A错误;
B.纤维素水解后检验葡萄糖应该在碱性环境中进行,水解后没有加碱将溶液调整至碱性,操作错误,B错误;
C.反应过程中挥发出来的乙醇也可被酸性高锰酸钾氧化从而使其褪色,此外反应可能会生成二氧化硫,同样能被酸性高锰酸钾氧化从而使其褪色,C错误;
D.水杨酸中含有酚羟基,乙酰水杨酸中没有酚羟基,向混合溶液中滴加1-2滴溶液,溶液变为紫色,说明混合溶液中有水杨酸,D正确;
故答案选D。
11.答案:C
解析:A.反应为气体分子数减小的反应,恒温恒容,充入,平衡正向移动,的转化率增大,A正确;
B.若升高温度,平衡常数减小,则反应逆向移动,那么正反应为放热反应,该反应,B正确;
C.压缩容积,活化分子百分数不变,反应物浓度变大导致反应速率加快,C错误;
D.恒温恒压,通入,容器体积变大,平衡向左移动,D正确;
故选C。
12.答案:C
解析:A.中含有1个过氧键(-O-O-),结构式为,单键均为σ键,双键中有1条σ键,1条π键,因此1ml过二硫酸钠()中含有σ键数9,A正确;
B.根据分析,氧化除锰后的溶液中存在的离子为,B正确;
C.溶液中能与锌反应生成和,所以调节溶液pH时试剂X不能选用Zn,C错误;
D.根据分析,“氧化除锰”工序用把氧化为,根据电子转移守恒和质量守恒可知,除锰发生反应的离子反应方程式是,D正确;
故选C。
13.答案:D
解析:A.图乙晶体中硼原子在内部,每个晶胞中有6个原子,镁原子位于晶胞的顶点和面心均摊法计算为:,所以化学式为,A错误;
B.图甲、图乙对应的晶体熔点依次为2700℃、830℃,所以前者熔点很高是共价晶体,后者熔点较高是离子晶体,B错误;
C.图甲中B原子和M原子之间的最近距离是内部小正方体体对角线的一半,为,C错误;
D.图甲晶体中,硼原子与氮原子的配位数都是4,所以硼原子位于氮原子构成的四面体中,D正确;故选D。
14.答案:
D解析:A.是易溶二元弱碱,而BOH+的水解平衡常数,则说明BOH+的水解程度大于电离程度,水解和电离都是微弱的,故溶液:,A正确;
B.当时,,,则,B正确;
C.向溶液中通入,发生反应生成更多的,越多,水解程度越大,水的电离程度越大,则水的电离程度:,C正确;
D.,当时,,,则,小于3.5,D错误;
故选D。
15.答案:(1);
(2)吸收尾气,防止空气中的水蒸气进入E中
(3)
(4)3.0;无;pH减小,氢离子浓度增大,抑制铁离子水解,生成氢氧化铁胶体变少,净水作用减弱;A4−B4的差值明显比A3−B3的差值大
(5)氢键;
解析:(1)Fe是26号元素,则基态的电子排布式为。A中是二氧化锰和浓盐酸在加热条件下反应得到氯气、氯化锰和水,则实验室制备的离子方程式为;故答案为:;。
(2)氯气会污染环境,氯化铁遇空气中水蒸气会水解,因此装置中F的作用:吸收尾气,防止空气中的水蒸气进入E中;故答案为:吸收尾气,防止空气中的水蒸气进入E中。
(3)胶团如图所示,由于氢氧化铁胶体粒子带正电,在静电吸附作用下,胶团可以除去废水中阴离子,则含价的砷微粒是;故答案为:。
(4)①根据下面实验结论,通过1、2、3组实验,发现随着增大,净水效果依次增强,说明1、2、3组实验只能是pH发生变化,而其他不能改变,则添加的助凝剂为无,再根据3、4组别是探究添加的助凝剂对净水效果,则pH应该相等,则pH=3.0;故答案为:3.0;无。
②实验结论一:通过1、2、3组实验,发现随着增大,净水效果依次增强。减小,净水效果减弱的原因是pH减小,氢离子浓度增大,抑制铁离子水解,生成氢氧化铁胶体变少,净水作用减弱;故答案为:pH减小,氢离子浓度增大,抑制铁离子水解,生成氢氧化铁胶体变少,净水作用减弱。
③实验结论二:添加助凝剂能够显著提高净水效果,说明4组别实验很明显即得到A4−B4的差值明显比A3−B3的差值大,则结论成立的判断依据是A4−B4的差值明显比A3−B3的差值大;故答案为:A4−B4的差值明显比A3−B3的差值大。
(5)①根据题意,噻吩难溶于水,吡咯能溶于水,由于吡咯中含有N−H,由于氮的电负性大,原因是吡咯能与水形成分子间氢键,而噻吩不能;故答案为:氢键。
②一个立方体结构的晶胞如图所示,铁的个数为,的个数为,已知阿伏加德罗数值为,的晶体密度为,,则,则晶胞的边长为;故答案为:。
16.答案:(1)不能
(2)+90.8kJ/ml;=
(3)N≡N键在“热Fe”表面断裂,有利于提高合成氨的反应速率;氨气在“冷Ti”表面生成,有利于提高氨的平衡产率
(4)加快合成氨反应速率;促使平衡正向移动,提高氨的平衡产率
(5)AB;第二步;0.15
解析:(1)放热、气体增加有利于反应的发生,ΔH>0、ΔS>0在高温条件下可发生,所以该反应低温不能发生。答案为不能;
(2)ΔH=E(反应物断键吸收的总能量)-E(生成物成键放出的总能量)=6×390.8-(946+436×3)=+90.8kJ/ml。此时的浓度熵为,则反应为平衡状态,。答案为+90.8kJ/ml;=;
(3)N≡N键断裂吸收热量,在“热Fe”表面断裂,有利于提高合成氨的反应速率。同时,N-H键的形成释放热量,氨气在“冷Ti”表面生成,有利于提高氨的平衡产率。答案为N≡N键在“热Fe”表面断裂,有利于提高合成氨的反应速率;氨气在“冷Ti”表面生成,有利于提高氨的平衡产率;
(4)知v与浓度成反比,移走氨气降低浓度使v增大,同时移走产物使平衡正向移动。答案为加快合成氨反应速率;促使平衡正向移动,提高氨的平衡产率;
(5)A.增加反应物的浓度反应物平衡正向,的转化率增加,A项符合题意;
B.该体系为气体减小的过程,增大压强平衡正向,转化率增大,B项符合题意;
C.尿素为纯液体,移走对平衡无影响,C项不符合题意;
D.催化剂只能改变反应速率,无法改变平衡状态及转化率,D项不符合题意;
故选AB。
活化能越高反应速率小。已知第一步反应速率快,则第一步活化能低于第二步。
反应前的体积分数为50%,和按物质的量1:1投料。设起始为1ml,列出三段式为
平衡时的体积分数为20%,则,。则平衡时的体积分数为则的体积分数为30%。=20%×(10MPa)=2MPa,=50%×(10MPa)=5MPa,=30%×(10MPa)=3MPa,则。答案为0.15。
17.答案:(1)硫酸钙
(2);C的质量较大的同位素在自然界中丰度较高
(3)
(4)过高,减小,不利于钙镁沉淀完全;或
(5)酸性条件
(6)ab
解析:(1)酸浸时用硫酸,产生的硫酸钙微溶,故“酸浸渣”主要成分的名称为硫酸钙;
(2)C是27号元素,基态C原子的核外电子排布式为或,故其M层电子排布式为;
C的质量较大的同位素在自然界中丰度较高,故虽然C的核电荷数比Ni小1,但C的相对原子质量比Ni的略大;
(3)“除铁”时加入的氯酸钠将亚铁离子氧化,反应生成氢氧化铁,反应的离子方程式为;
(4)“除钙镁”时,随着pH的降低,溶液中的增加,的平衡正向移动,溶液中减小,为使和的溶解平衡逆向移动,NaF用量更多;已知离子浓度时,认为该离子沉淀完全,且,钙离子沉淀完全时镁离子已沉淀完全,,所以为使和沉淀完全,溶液中最小为或;答案为过高,减小,不利于钙镁沉淀完全;或;
(5)“反萃取”时为促进的转移,应选择的实验条件或采取的实验操作有①酸性条件;②多次萃取;
(6)获得(s)的“一系列操作”中洗涤产品使其溶解度降低而晶体析出,故可选用冷水或乙醇,答案选ab。
18.答案:(1)光照
(2)苯乙腈;sp;;
(3)羟基、酮羰基(或羰基);取代反应
(4)4
(5)
(6)18
(7)
选项
实验操作
实验现象
结论或解释
A
将与反应后的固体物质加水溶解后,先加足量的稀硝酸,再滴加溶液
产生白色沉淀
说明与反应后生成了
B
将脱脂棉放入试管中,加入浓硫酸后搅成糊状,微热得到亮棕色溶液,加入新制氢氧化铜悬浊液,加热
有砖红色沉淀生成
说明水解产物含有葡萄糖
C
向无水乙醇中加入浓硫酸,加热至,将产生的气体通入酸性溶液中
紫红色褪去
乙醇发生消去反应生成乙烯
D
取少量乙酰水杨酸样品,再加蒸馏水和少量乙醇,振荡,向混合溶液再滴加1-2滴溶液
溶液变为紫色
说明混合溶液中含有水杨酸
组别
废液体积
饱和溶液用量
添加的助凝剂
净水前砷微粒浓度
净水后砷微粒浓度
1
1.0
2滴
无
Al
B1
2
2.0
2滴
A2
B2
3
_________
2滴
_________
A3
B3
4
3.0
2滴
有
A4
B4
化学键
N≡N
H-H
N-H
键能/
946
436
390.8
安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析: 这是一份安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析,共19页。试卷主要包含了单选题等内容,欢迎下载使用。
2023届湖南省衡阳市第八中学高三下学期第七次月考化学试卷Word版含答案: 这是一份2023届湖南省衡阳市第八中学高三下学期第七次月考化学试卷Word版含答案,共14页。
2021-2022学年湖南省衡阳市第一中学高二(下)月考化学试卷(5月)(含答案解析): 这是一份2021-2022学年湖南省衡阳市第一中学高二(下)月考化学试卷(5月)(含答案解析),共20页。试卷主要包含了 下列离子方程式正确的是等内容,欢迎下载使用。