



化学九年级下册课题3 溶液的浓度评优课ppt课件
展开1.掌握溶液中溶质的质量分数的概念。2.学会计算有关溶质的质量分数。3.学会配制一定溶质质量分数的溶液。
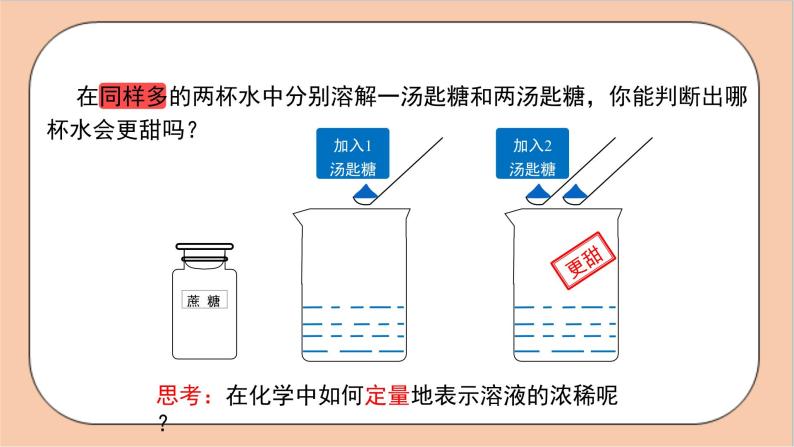
在同样多的两杯水中分别溶解一汤匙糖和两汤匙糖,你能判断出哪杯水会更甜吗?
思考:在化学中如何定量地表示溶液的浓稀呢?
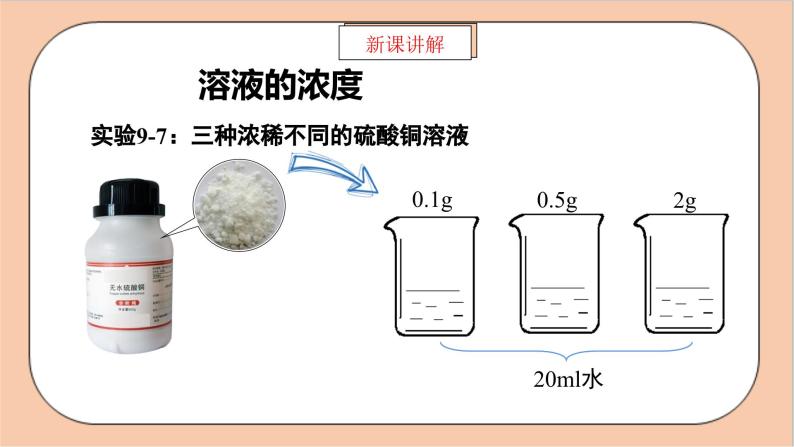
实验9-7:三种浓稀不同的硫酸铜溶液
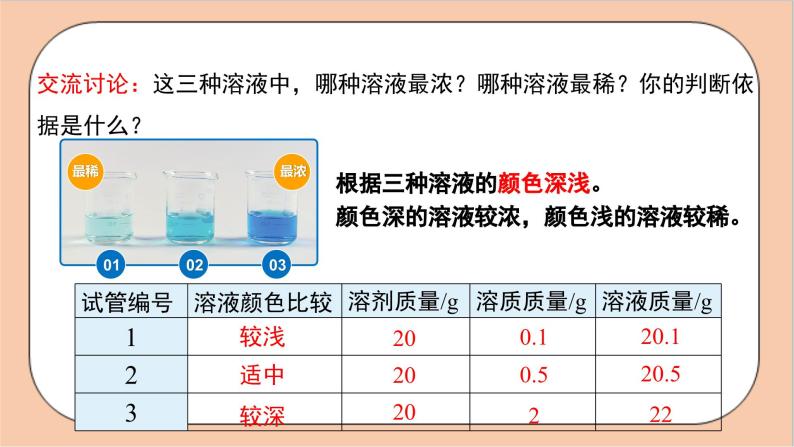
交流讨论:这三种溶液中,哪种溶液最浓?哪种溶液最稀?你的判断依据是什么?
根据三种溶液的颜色深浅。颜色深的溶液较浓,颜色浅的溶液较稀。
表示溶液浓度的方法很多,这里主要介绍 溶质的质量分数。
在实际应用中,常常要准确知道一定量的溶液里所含溶质的量,即溶液的浓度。
溶液中溶质的质量分数就是溶质质量与溶液质量之比。
溶质质量分数——定量表示溶液的浓度
实验9-8:配制两种质量分数不同的氯化钠溶液
交流讨论:根据溶质的质量分数的公式,能不能得到溶质和溶剂的质量?
溶质质量=溶液质量×溶质的质量分数
溶液质量=溶质质量+溶剂质量
溶剂质量=溶液质量-溶质质量
【例题1】在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg的这种溶液,需要氯化钠和水的质量各是多少?
解:溶质质量=溶液质量×溶质的质量分数 =150 kg×16% =24 kg 溶剂质量=溶液质量-溶质质量 = 150 kg-24 kg = 126 kg答:配制150 kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
【例题2】化学实验室现有质量分数98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50g上述浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
解:设稀释后溶液的质量为x
50g ×98% = x×20%
答:需要水的质量195g。
需要水的质量= 245 g– 50g = 195g
【分析】稀释前溶质质量=稀释后溶质质量
练习:配制10%的硫酸溶液98g,需要98%的浓硫酸(密度为1.84g/mL)的体积是多少?
解:设需要98%的浓硫酸的体积为V。
V×1.84g/mL×98%=98g×10%
答:需要98%的浓硫酸的体积为5.4mL。
交流讨论:已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时,氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
100 g + 36 g
溶质质量分数与溶解度的关系
练习:在20℃时,Ca(OH)2的溶解度是0.17g,问此温度下将1g Ca(OH)2固体放入200g水中,充分溶解后,所得溶液的溶质质量分数是多少?
该温度下200g水中只能溶解0.34g Ca(OH)2固体,溶液即饱和。
答:所得溶液的溶质质量分数是0.17%。
【例题3】40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?
解:设稀盐酸的质量为X,生成的NaCl的质量为Y
NaOH + HCl = NaCl + H2O
40g×10% X ×10% Y
40 36.5 58.5
反应后溶液的溶质的质量分数=
溶质的质量分数与化学方程式的综合计算
有关溶质的质量分数与化学方程式相结合的计算
解该类题时,一定要正确写出该反应的化学方程式。
有溶液参与的反应,只是溶液中的溶质参与了反应。
反应后溶液的质量=反应前的总质量-生成气体的质量- 生成沉淀的质量-不溶物的质量。
练习:100g某硫酸恰好与13g锌完全反应。试计算这种硫酸中溶质的质量分数。
解:设硫酸中溶质的质量为X
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g X
答:这种硫酸溶液中溶质的质量分数为19.6%。
实验演示——配制50g溶质质量分数为6%的氯化钠溶液
计算:配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠 g;水 g。
称量:用天平称量所需的氯化钠,放入烧杯中;
溶解:用玻璃棒搅拌,使氯化钠溶解。
量取:用量筒量取所需的水(水的密度近似看做1g/cm3),倒入盛有氯化钠的烧杯中。
实验室中配制一定溶质质量分数的溶液
思考:1.配置一定溶质质量分数的溶液需要用到哪些仪器?2.若所配溶液的溶质质量分数偏大或偏小,你认为可能的原因有哪些?
溶质质量与溶液质量之比
溶质质量分数的简单计算
一定溶质质量分数溶液的配制
1. 对“16%的食盐溶液”的含义解释错误的是( )A.100 g食盐溶液中溶解了l6 g食盐 B.将食盐与水按16﹕84的质量比配成的溶液C.将32 g食盐溶解于168 g水中所得到的溶液 D.100 g水中溶解了16 g食盐
2.现有一杯60℃的硝酸钾饱和溶液,下列操作会导致硝酸钾的质量分数减小的是( )
A. 升温至80℃ B. 恒温蒸发部分溶剂C. 加入一定量的硝酸钾D. 加入一定量的氯化钠
3.现需要将溶质质量分数为40%的氢氧化钠溶液稀释为40 g溶质质量分数为5%的氢氧化钠溶液。此时,需要水的体积为( )A.38 mL B.36 mL C.35 mL D.37 mL
化学课题3 溶液的浓度教学课件ppt: 这是一份化学课题3 溶液的浓度教学课件ppt,共8页。PPT课件主要包含了Vc泡腾片,实验演示,溶质的质量分数,拓展应用,推导提高等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度教案配套课件ppt: 这是一份初中化学人教版九年级下册课题3 溶液的浓度教案配套课件ppt,共8页。PPT课件主要包含了你知道吗,溶质质量分数,溶质质量,溶液质量,相关计算《一》,练一练1,中考易错点,让我们动起手来,相关计算《二》,让我们开动脑筋等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度说课ppt课件: 这是一份初中化学人教版九年级下册课题3 溶液的浓度说课ppt课件,共18页。PPT课件主要包含了喷洒药水,是浓还是稀,溶质的质量分数,表达式,表示物质溶解性的强弱,不一定,单位为1省略不写,必须饱和,质量单位克,溶质质量分数的含义等内容,欢迎下载使用。













