


- 8.2 化学品的合理使用(课件PPT) 课件 1 次下载
- 8.2 化学品的合理使用 整理提升(课件PPT) 课件 1 次下载
- 8.3 环境保护与绿色化学(课件PPT) 课件 1 次下载
- 8.3 环境保护与绿色化学 整理提升(课件PPT) 课件 1 次下载
- 人教版化学必修2 第八章 综合测评(课件PPT) 课件 1 次下载
人教版化学必修2 第八章 复习提纲(课件PPT)
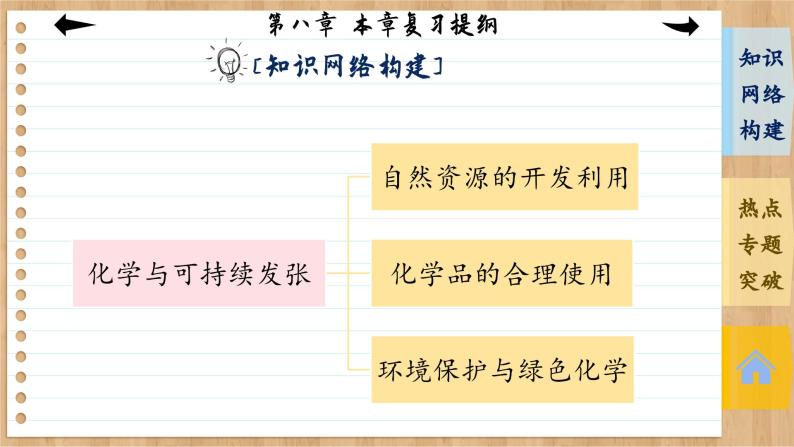
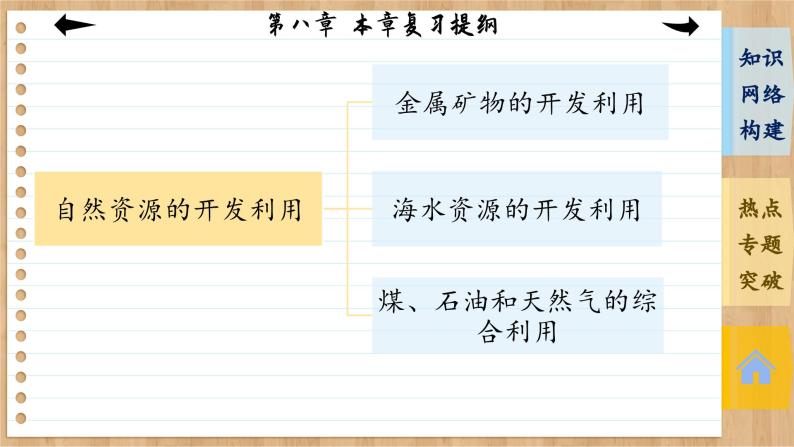
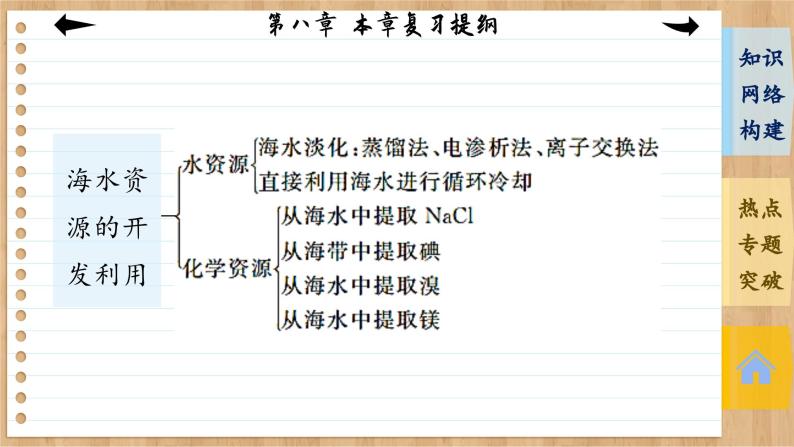
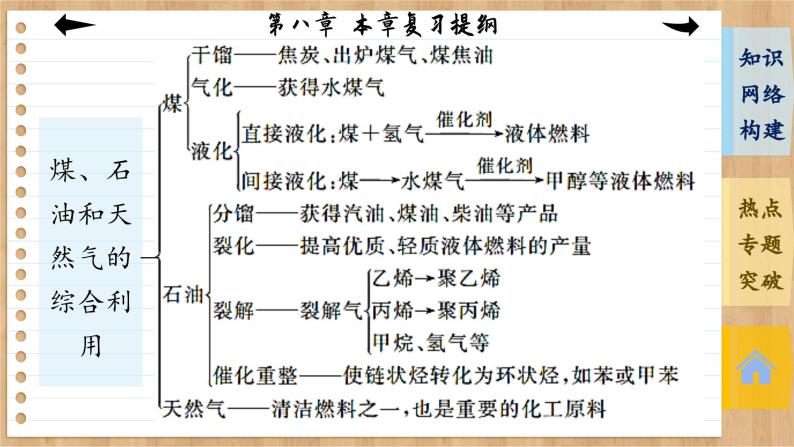
展开第八章 化学与可持续发展 本章复习提纲金属的冶炼:电解法、 热还原法、热分解法(按金属活动性顺序)金属的有效利用和回收再利用核心是利用化学原理和技术手段从源头上减少或消除工业生产对环境的污染最理想的“原子经济性反应”就是反应物的原子全部转化为期望的最终产物,即原子利用率为100%专题 无机化工生产流程综合分析1.问题设置与考查知识点 有关无机化工生产试题的考查内容归纳起来主要有六个方面:(1) 将原料转化为产品的生产原理:考查“复分解反应、氧化还原反应、水解反应”等原理。(3)提高产量与产率(转化率):考查“化学反应速率和化学平衡”。(4)减少污染:考查“绿色化学”生产。(5)原料的来源:考查物质的来源及成本问题。(6)生产设备简单,生产工艺简便可行等工艺生产问题:要准确、顺利解答无机化工生产流程题,除了要掌握物质的性质和物质之间相互作用的基本知识以及除杂、分离提纯物质的基本技能外,还要具备分析工艺生产流程的能力。2.解答无机化工生产流程题的程序(1) 基本步骤①从题干中获取有用信息,了解生产的产品。②整体阅读流程图,辨别出预处理、反应、提纯、分离等阶段。③ 分析流程中的每一个步骤,从几个方面了解流程:反应物是什么;发生了什么反应;该反应造成了什么后果;对制造产品有什么作用。抓住一个关键点:一切反应或操作都是为获得产品而服务。④ 从问题中获取信息,帮助解题。(2) 解题思路明确整个流程及每一步的目的―→仔细分析每步反应发生的条件以及得到的产物的物理或化学性质―→结合基础理论与实际问题思考―→注意答题的模式与要点。3.解题模板例 海水是一种丰富的资源,工业生产可以从海水中提取许多有用的物质,这些物质广泛应用于生活、生产、科技等方面。如图是从含碘CCl4溶液中提取碘的实验过程。请回答下列问题:(1) 向含碘CCl4溶液中加入稍过量的Na2SO3溶液,则发生反应的离子方程式为_________________________________________________;该操作将I2还原为I-的目的是__________________________________________________________________________。(2) 操作X的名称为________,所用的主要仪器是____________。SO32-+I2+H2O===2I-+SO42-+2H+ 使四氯化碳中的碘单质转化为碘离子进入水溶液分液 分液漏斗(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40 ℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是____________________________________________;锥形瓶里盛放的溶液为______________。 防止碘升华、增大氯气溶解度 NaOH溶液(4)已知:5SO32-+2IO3-+2H+===I2+5SO42-+H2O,某含碘溶液(pH约为8)中一定存在I2,可能存在I-、IO3-中的一种或两种。请补充完整检验含碘溶液中是否同时含有I-、IO3-的实验方案:________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。实验中可供选择的试剂:CCl4、稀盐酸、淀粉溶液。 取少量含碘溶液用四氯化碳多次萃取、分液;水层用淀粉溶液检验,当水层不含碘单质时,取少量水层溶液,加入1~2 mL淀粉溶液,加盐酸酸化,若溶液变蓝,说明溶液中同时含有I-和IO3-;如果溶液不变蓝,说明不同时含有I-和IO3-解析:(1)碘能将SO32-氧化为SO42-,自身被还原为I-,其发生反应的离子方程式为SO32-+I2+H2O===2I-+SO42-+2H+;将碘还原为I-,目的是使四氯化碳中的碘单质转化为I-进入水溶液,以便利用分液法分离出四氯化碳。(2)分离互不相溶的液体可采用分液法,四氯化碳和水溶液互不相溶,所以操作X为分液;使用的主要仪器是分液漏斗。(3)碘不稳定,易升华,且温度高时气体难溶解,所以实验控制在较低温度下的原因是防止碘升华、增大氯气溶解度;氯气能和强碱溶液反应,所以锥形瓶中的液体是NaOH溶液。(4)根据题给反应方程式可知,在酸性环境中,IO3-有强氧化性,故可推断,在酸性环境中,IO3-能将I-氧化。因此,检验含碘溶液中是否同时含有I-和IO3-,可先用四氯化碳多次萃取含碘溶液,然后分液,水层用淀粉溶液检验,当水层不含碘时,取少量水层溶液,加入淀粉溶液,再加盐酸酸化,如果同时含有I-和IO3-,二者发生氧化还原反应生成I2使溶液变蓝色,否则不同时含有I-和IO3-。本课结束This lesson is overTHANKS!









