


预测卷07-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
展开预测卷07
(满分:58分 建议用时:40分钟)
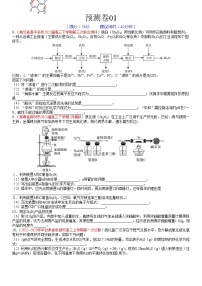
8.(陕西省咸阳市2023年高三一模)溴酸镉[Cd(BrO3)2]常用作分析试剂、生产荧光粉等。以镉铁矿(主要成分为CdO2、Fe2O3、Fe及少量的Al2O3和SiO2)为原料制备Cd(BrO3)2的工艺流程如图所示。
已知:Cd(SO4)2可溶于水。请回答下列问题:
(1)滤渣1为___________(填化学式),为提高镉的浸取率,酸浸时可采取的措施为___________(任写一种即可)。
(2)还原镉时,产生能使澄清石灰水变浑浊的气体,则该反应的离子方程式为_________________。
(3)加入H2O2溶液的目的是_____________________________(用离子方程式表示)。
(4)滤渣2的主要成分为___________(填化学式)。
(5)实际工业生产中,用阳离子交换树脂法来测定沉镉后溶液中Cd2+的含量,其反应原理是:Cd2++2NaR2Na++CdR2,其中NaR为阳离子交换树脂。常温下,将沉镉后的溶液(pH=6)经过阳离子交换树脂后,测得溶液中的Na+比交换前增加了0.0552g/L,则该条件下Cd(OH)2的Ksp为___________mol3•L-3。
9.(河南省六市2023届高三第一次联合调研)某实验小组利用如图装置模拟古法硫酸生产方法并进行SO2性质探究。
已知A中反应的化学方程式:2FeSO4·7H2OFe2O3+SO2↑+SO3↑+14H2O,实验开始前打开活塞K1、K2,关闭活塞K3,通入一段时间N2后,关闭活塞K1、K2,打开活塞K3,高温加热绿矾。完成下列填空:
(1)C装置中覆盖食用油的目的是___________________________________;B中所得硫酸溶液的质量分数理论值为___________(保留三位有效数字)。
(2)该装置存在的不足之处为___________________________________。
为探究SO2与钡盐溶液的反应,在装置C中先后四次加入不同的溶液:
① | ② | ③ | ④ |
已煮沸的BaCl2溶液 | 未煮沸的BaCl2溶液 | 已煮沸的Ba(NO3)2溶液 | 未煮沸的Ba(NO3)2溶液 |
注:锥形瓶中溶液体积相同,钡盐溶液浓度相同;油层厚度一致,通入SO2流速一致。 | |||
得到如下pH-t图:
(3)曲线①呈缓慢下降趋势,这是因为_________________________________________。曲线②出现骤降,表明溶液中生成了_________________(填物质名称)。对比分析上述四组数据,可得出的结论是_____________________________、______________________________(任写2条)。
(4)为对排气法收集到的SO2气体进行含量测定,将1120mL气体(已折算为标准状况)通入足量的Ba(NO3)2溶液中,经过滤、洗涤、烘干,最终得到沉淀10.718g.则SO2气体的体积分数为_______(保留两位有效数字)。若该实验数据较实际值偏大,则可能的原因是________(选填序号)。
a.气体通入速率过快 b.沉淀未进行恒重操作
c.收集的气体中有CO2 d.未用食用油覆盖液面
(5)SO2属于大气污染物,还可用H2与其高温反应消除SO2带来的污染,其反应原理如图所示:
①反应原理过程中X为___________(填名称)。
②写出检验X所需试剂及实验现象_______________________________。
10.(云南省楚雄市2022~2023学年高三3月模拟)绿色能源是科研工作者研究的主要方向,如氢能源、电能等都属于绿色能源。
Ⅰ.利用乙醇催化制氢气
总反应:CH3CH2OH(g)+3H2O(g)2CO2(g)+6H2(g)
第一步:CH3CH2OH(g)+H2O(g)2CO(g)+4H2(g)△H1=+255.9kJ•mol-1
第二步:CO(g)+H2O(g)CO2(g)+H2(g)△H2=-41.2kJ•mol-1
(1)总反应的△H=_________。
Ⅱ.CO制氢气
(2)工业上利用第二步制H2。在恒容绝热的密闭容器中通入一定量的CO和H2O反应制备H2,下列说法表示该反应达到最大限度的有______(填标号)。
a.装置内的气体无CO b.装置内的压强不变
c.H2的体积分数不变 d.装置内气体摩尔质量不变
(3)某温度下,若投料比[n(CO)∶n(H2O)=0.5],CO的转化率为50%,则该反应的Kp=______(以分压表示,分压=总压×物质的量分数)。·p(CO2),
(4)研究表明,第二步反应的速率方程为v=k·yCO·yH2O-,式中,yCO、yH2O、yH2分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大,根据速率方程分析,T>Tm时v逐渐减小的原因是__________________________。
Ⅲ.新型绿色电池
(5)某钠离子电池结构如图所示,电极A为含钠过渡金属氧化物(NaxTMO2),电极B为硬碳,充电时Na+得电子成为Na嵌入硬碳中,NaTMO2失去电子生成Na1-xTMO2,充电时B极的电极反应:______,放电时A极的电极方程式:_______________________________。
【化学-选修3:物质结构与性质】
11.(四川省遂宁市2023年高三2月模拟)离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
(1)碳原子价层电子的轨道表达式为______________,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______;NO3-与NO2-中O-N-O的键角:NO3-____NO2-(填“<”、“>”“=”)。
(3)EMIM+离子与金属阳离子形成的离子化合物常温下呈液态的原因是____________________________。
(4)EMIM+离子中,碳原子的杂化轨道类型为___________。分子中的大π键可用符号Π表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,则EMIM+离子中的大π键应表示为________________。
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______晶体,其中硼原子的配位数为_______。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为____________(列出化简后的计算式)。
【化学-选修5:有机化学基础】
12.(湖南省长沙市2022~2023学年高三3月模拟)解热镇痛类药物布洛芬对于缓解奥密克戎引起的疼痛有很好的作用,其合成方法如图:
(1)A的系统命名为________________。
(2)C→D的反应类型与______→_____相同。
(3)写出B→C的方程式:________________________________________。
(4)下列有关布洛芬(H)的叙述正确的是_____(填序号)。
①布洛芬中的官能团有羧基
②1mol该物质与碳酸钠反应生成标准状况下22.4CO2
③布洛芬分子中最多有19个原子共平面
④1mol布洛芬分子中含有手性碳原子的物质的量为2mol
(5)口服布洛芬对胃、肠道有刺激,用对布洛芬进行成酯修饰,能有效改善这种状况,发生反应的化学方程式是_____________________________。
(6)H的同分异构体同时满足下列条件,该同分异构体可能为___________、_________(任写两种,不考虑立体异构)。①有一个苯环外无其他环状结构;②1mol该物质与浓溴水反应时最多消耗4molBr2;③分子中含有6种不同化学环境的氢原子。
(7)请写出以和为原料制备的合成路线流程图(无机试剂和有机溶剂任选,合成路线流程图示例见本题题干)________________________。
预测卷08-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用): 这是一份预测卷08-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用),文件包含预测卷08-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用解析版docx、预测卷08-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用原卷版docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
预测卷06-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用): 这是一份预测卷06-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用),文件包含预测卷06-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用解析版docx、预测卷06-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用原卷版docx等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
预测卷05-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用): 这是一份预测卷05-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用),文件包含预测卷05-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用解析版docx、预测卷05-大题精做冲刺2023年高考化学大题突破+限时集训新高考专用原卷版docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。