

预测卷01-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
展开预测卷01
(满分:58分 建议用时:40分钟)
8.(湖北省高中名校2023届高三下学期第三次联合测评)锑白(Sb2O3,两性氧化物)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是Sb2O3、Sb2O5,含有CuO、Fe2O3和SiO2等杂质)中制取Sb2O3的工业流程如下图所示。
已知:①“滤液1”的主要阳离子是Sb3+、Sb5+、Fe3+、Cu2+、H+;②“滤饼”的成分是SbOCl。
回答下列问题:
(1)将“滤渣1”进行二次酸浸的目的是______________________。
(2)“滤渣2”的成分是____________。
(3)“稀释水解”主要反应的离子反应方程式为________________________________;该操作中需要搅拌的原因是______________________。
(4)“酸洗”后检验沉淀是否洗净的试剂是_________________。
(5)“中和”时反应的化学方程式为_____________________________________;“中和”需控制溶液的pH在7~8,碱性不能过强的原因是_________________。
9.(湖南省郴州市2023届高三下学期2月模拟)氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁同一主族,金属锶与氮气在加热条件下可生成氮化锶,氮化锶易水解,遇水剧烈反应。
Ⅰ.利用装置A和C制备Sr3N2
(1)装置A中仪器b的名称是____________,a导管的作用是_______________________。
(2)写出由装置A制备N2的化学方程式:_____________________________________。
(3)操作中,应先点燃装置A的酒精灯一段时间后,再点燃装置C的酒精灯,这样操作的理由是___________________________________________。
Ⅱ.利用装置B和C制备Sr3N2。(已知:氧气可被连苯三酚溶液定量吸收。)
(4)写出装置B的NaOH溶液中发生反应的离子方程式:___________________________。
(5)装置C中广口瓶盛放的试剂是______________________。
Ⅲ.测定Sr3N2产品的纯度
(6)取10.0g该产品,向其中加入适量的水,直接将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是______________________。经改进后测得浓硫酸增重1.02g,则产品的纯度为_______。
10.(2022~2023学年甘肃省张掖市高三上学期第一次诊断)硫化氢广泛存在于燃气及废水中,热分解或氧化硫化氢有利于环境保护并回收硫资源。回答下列问题:
(1)1gH2S气体完全燃烧,生成液态水和SO2气体,放出17.24kJ的热量,写出表示H2S(g)的燃烧热的热化学方程式:_____________________________________。
(2)利用H2S的热分解反应可生产H2:2H2S(g)S2(g)+2H2(g)。现将0.20molH2S(g)通入到某恒压(压强p=aMPa)密闭容器中,在不同温度下测得H2S的平衡转化率如图1所示。
已知:对于气相反应,用某组分(B)的平衡分压(PB)代替物质的量浓度(cB)也可表示平衡常数(Kp)。(P总=PB×B的物质的量分数,P总为平衡时气体总压强)。温度升高时,混合气体的平均摩尔质量_______(填“增大”“减小”或“不变”)。温度为T4℃时,该反应的平衡常数Kp=____________MPa(用含a的代数式表示)。
(3)用氯气除去废水中H2S的反应为Cl2(aq)+H2S(aq)S(s)+HCl(aq),该反应的可能机理如下:
A.Cl2→2Cl·慢 Cl·+H2S→HCl+HS·快 Cl·+HS·→HCl+S快 | B.Cl2→2Cl·快 Cl·+H2S→HCl+HS·慢 Cl·+HS·→HCl+S快 |
C.Cl2+H2S→Cl·+HS·+HCl慢 Cl·+HS·→HCl+S快 | D.Cl2+H2S→Cl·+HS·+HCl快 Cl·+HS·→HCl+S慢 |
①机理a的中间体为_______。
②已知v正=k·c(Cl2)·c(H2S),v正为正反应速率,k为速率常数,上述机理中与该速率方程一致的是_______(填字母)。
(4)科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构如图2所示。
①a极的电极反应式为______________________。
②电池工作时,H+经质子膜进入_______区(填“a极”或“b极”)。
【化学-选修3:物质结构与性质】
11.(宁夏石嘴山2023届高三2月模拟)“天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。
(1)镍原子价层电子表示式为____________,在元素周期表中,铼与锰在同族,铼在元素周期表中的位置是____________。
(2)铼易形成高配位数的化合物如Re2(CO)10,该配合物中_______(填元素符号)提供孤对电子与铼成键,原因是___________________________,1mol Re2(CO)10中有_______mol配位键。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为___________,CO32-的空间构型为_________(用文字描述)。与CO32-互为等电子体的分子是______________(写一种即可)。
(4)CH3分子中碳原子的杂化类型为_______,CH3比NH2的熔点沸点_____(填“高”或“低”),原因是_________________。
(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在____个氧原子围成的_______(填“四面体”“立方体”或“八面体”)空隙中,该晶胞的空间利用率为___________________(铼的原子半径为rRepm,氧原子半径为rOpm,列出计算式)。
【化学-选修5:有机化学基础】
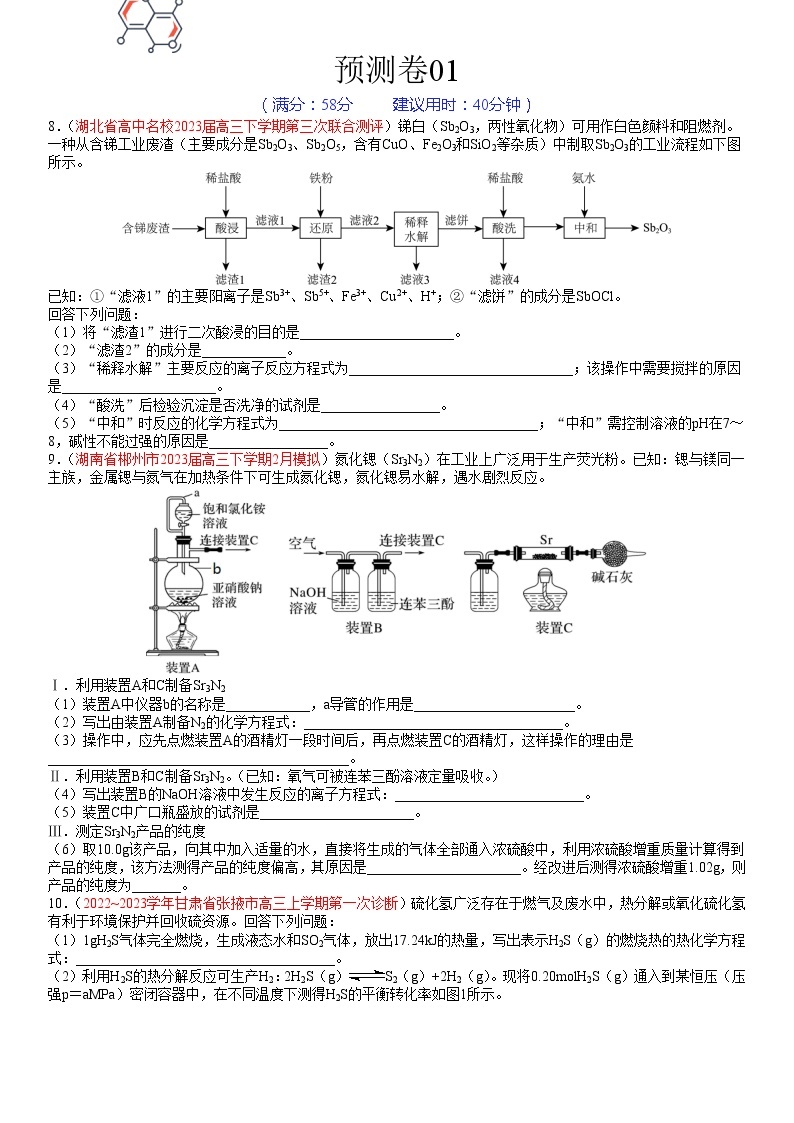
12.镇痛药物J的合成方法如图:
已知:①+Cl-R3+HCl
②R1COOR2+R3CH2COOR4+R2OH
③(R1、R2、R3、R4为氢或烃基)④+RCOOR′
回答下列问题:
(1)反应②的反应类型____________,B的名称__________。
(2)F中含碳的官能团的名称____________。
(3)反应D→E的化学方程式________________________________________。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有____种。①遇FeCl3溶液显紫色②苯环上有两个取代基。写出含有6种氢原子,且峰面积之比为1∶1∶2∶2∶2∶3的结构简式(任写一种即可)____________________。
(5)设计以CH3CH2OH和为原料制备X()的合成路线____________________。(无机试剂任选。)
预测卷01-【大题精做】冲刺2024年高考化学大题突破+限时集训(浙江专用): 这是一份预测卷01-【大题精做】冲刺2024年高考化学大题突破+限时集训(浙江专用),文件包含预测卷01原卷版docx、预测卷01解析版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
预测卷01-冲刺高考化学大题突破+限时集训(浙江专用): 这是一份预测卷01-冲刺高考化学大题突破+限时集训(浙江专用),文件包含预测卷01解析版docx、预测卷01原卷版docx等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。
预测卷01-【大题精做】冲刺2023年高考化学大题突破+限时集训(浙江专用): 这是一份预测卷01-【大题精做】冲刺2023年高考化学大题突破+限时集训(浙江专用),文件包含预测卷01解析版docx、预测卷01原卷版docx等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。