




鲁教版九年级上册第三节 原子的构成优秀ppt课件
展开第二单元 探秘水世界
第三节 原子的构成
第二课时 原子中的电子
教学过程
导入新课
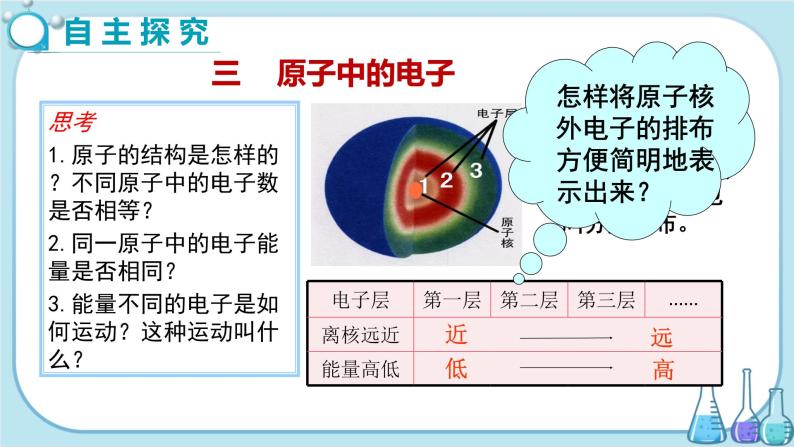
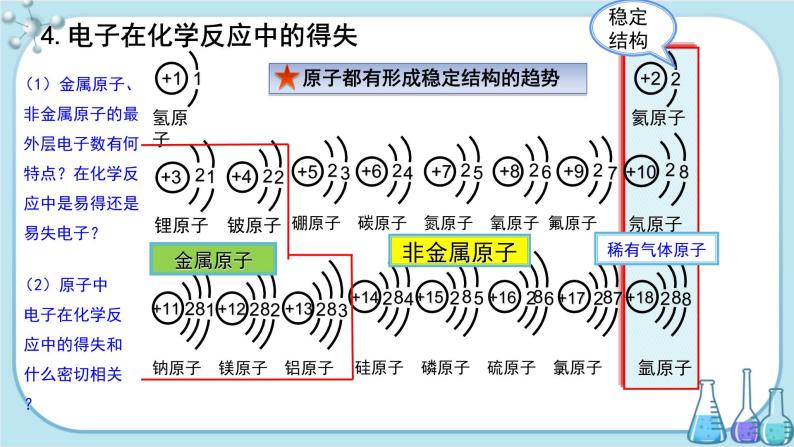
1.原子的结构是怎样的?不同原子中的电子数是否相等?
2.同一原子中的电子能量是否相同?
3.能量不同的电子是如何运动?这种运动叫什么?
讲授新课
三、原子中的电子
图片:原子核外电子的排布
在原子中,电子是体积小、质量轻的一种小粒子。不同的原子含有的电子数目不同。在多电子原子中,核外电子的能量是不同的。能量高的在离核较远的区域运动,能量低的在离核较近的区域运动。
通常把电子在离核远近不同的区域运动称为电子的分层排布。
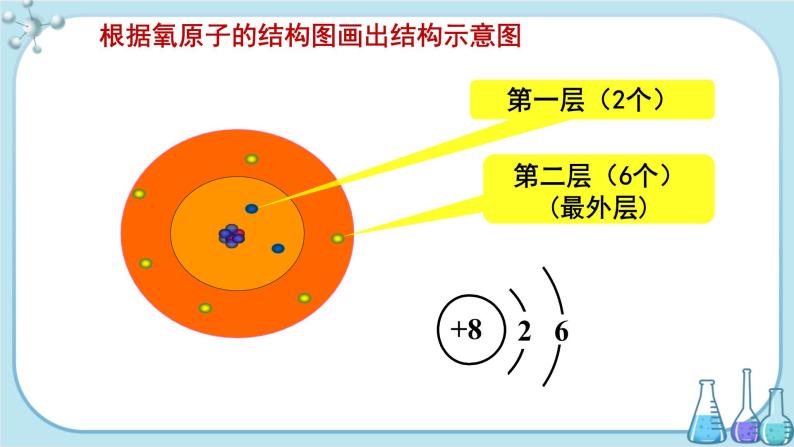
一个碳原子的原子核内有 6 个质子和 6 个中子。核外有 6 个电子,其中有 2 个电子能量相近都较低,另外 4 个电子能量相近且能量稍高。这些电子都同时绕原子核高速运动。根据刚才的理解,请你把碳原子的结构以最简洁的方式画出来。
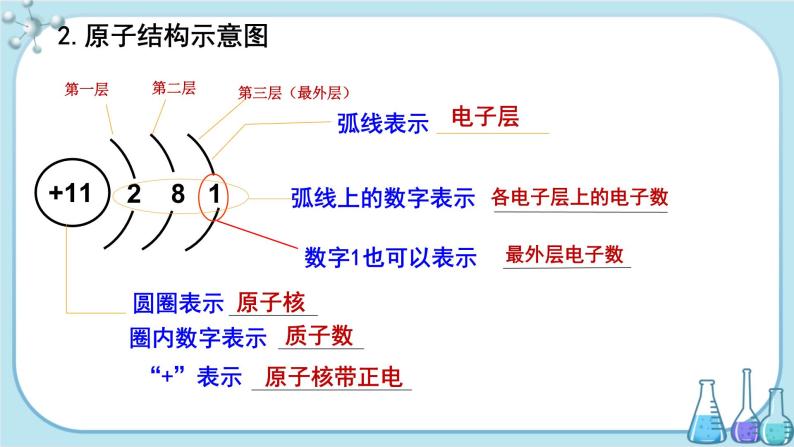
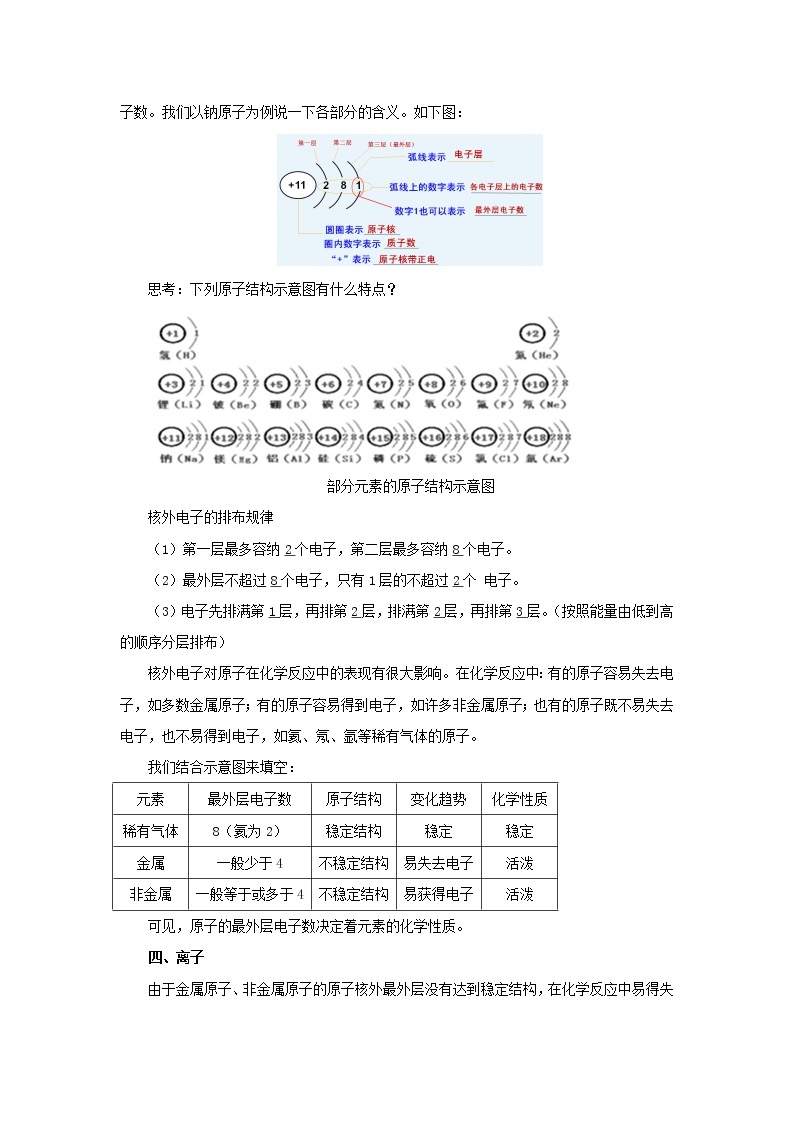
用原子结构示意图可以方便简明地表示原子核外电子的排布。在原子结构示意图中:圆圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上面的数字表示该层的电子数。我们以钠原子为例说一下各部分的含义。如下图:
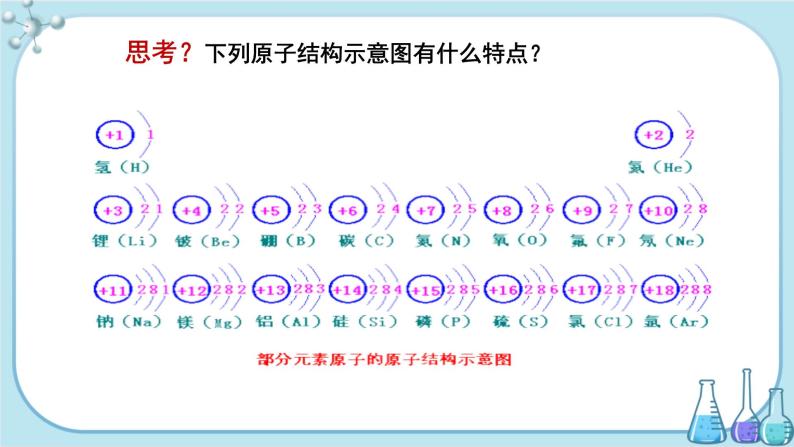
思考:下列原子结构示意图有什么特点?
部分元素的原子结构示意图
核外电子的排布规律
(1)第一层最多容纳2个电子,第二层最多容纳8个电子。
(2)最外层不超过8个电子,只有1层的不超过2个 电子。
(3)电子先排满第1层,再排第2层,排满第2层,再排第3层。(按照能量由低到高的顺序分层排布)
核外电子对原子在化学反应中的表现有很大影响。在化学反应中:有的原子容易失去电子,如多数金属原子;有的原子容易得到电子,如许多非金属原子;也有的原子既不易失去电子,也不易得到电子,如氦、氖、氩等稀有气体的原子。
我们结合示意图来填空:
元素 | 最外层电子数 | 原子结构 | 变化趋势 | 化学性质 |
稀有气体 | 8(氦为2) | 稳定结构 | 稳定 | 稳定 |
金属 | 一般少于4 | 不稳定结构 | 易失去电子 | 活泼 |
非金属 | 一般等于或多于4 | 不稳定结构 | 易获得电子 | 活泼 |
可见,原子的最外层电子数决定着元素的化学性质。
四、离子
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
1.氯化钠的形成
金属钠和氯气反应生成氯化钠,钠原子和氯原子的结构示意图如下,我们从微观角度分析一下氯化钠的形成。
教师总结
阳离子 原子 阴离子
(质子数>电子数)(质子数=电子数)(质子数<电子数)
离子所带电荷数=原子得失电子数
2.离子的定义:带电的原子(或原子团)叫离子。
3.离子的分类
(1)阳离子:带正电的原子(或原子团)叫做阳离子。
①特点:电子数<质子数。
②示例:Na+、K+、Mg2+、Al3+。
(2)阴离子:带负电的原子(或原子团)叫做阴离子。
①特点:电子数>质子数。
②示例:O2-、S2-、 F- 、Cl-。
4.离子化合物
像氯化钠由阴、阳离子靠静电作用而形成的化合物。
5.离子符号的书写
先写元素符号,然后将电荷数标注在元素符号的右上角,数字在前、符号在后,“1”省略不写。离子所带电荷数由该元素原子的最外层电子数决定。
我们以镁离子为例来看一下
教师点拨
熟记常见原子团(根)的符号、名称。
名称: 氢氧根 硝酸根 铵根 碳酸根 硫酸根
符号: OH-
6.构成物质的粒子
构成物质的粒子包括原子、分子、离子。
(1)由原子直接构成的物质:稀有气体(如He、Ne等);金属(如Hg、Fe等);少数固态非金属(如C、Si等)。
(2)由分子构成的物质:双原子气体分子(如H2、O2、N2等);多原子共价化合物(如H2O、CO2、HCl等)。
(3)由离子构成的物质:离子化合物(如NaCl、K2S、CuSO4等)。
教师点拨
离子与原子的区别和联系
(1)区别
①化学性质不同:原子大多不稳定,化学性质活泼;离子结构稳定,化学性质不活泼。
②电性不同:原子不带电,离子带电。
(2)联系
当堂达标
1.辨别下列哪些是原子结构示意图,哪些是离子结构示意图,并能够根据结构示意图写出对应的符号:
答案:对应的符号为Na、Mg、S、Cl、Na+、Mg2+、S2-、Cl-。
2.某离子带3个单位的正电荷,质子数为13,该离子的核外电子数为_____,该离子的名称是______,符号是____,该离子的结构示意图是__________。
答案:10 铝离子 Al3+
3.根据粒子的结构图示意回答:
如果该图表示的是原子,X值为___,该原子的符号是____。
如果该图表示的是带两个单位正电荷的阳离子,X值为___,符号是____。
如果该图表示的是带两个单位负电荷的阴离子,X值为___,符号是____。
答案:10 Ne 12 Mg2+ 8 O2-
板书设计
第二课时 原子中的电子
1.核外电子的运动:分层运动
电子能量:低 高
离核距离:近 远
2.原子结构示意图
氧原子结构示意图
3.核外电子的排布规律
(每层最多排2n2个电子,n—表示电子层数)
(1)第一层最多排 个电子。
(2)第二层最多排 个电子。
(3)第三层最多排 个电子。
(4)最外层最多不超过 个电子。
(5)最外层为 个电子(只有1个电子层,该层上有 个电子)称为稳定结构。
4.元素化学性质与原子的最外层电子数目的关系
5.离子的形成
6.离子符号书写
初中化学鲁教版九年级上册第一节 燃烧与灭火优秀ppt课件: 这是一份初中化学鲁教版九年级上册第一节 燃烧与灭火优秀ppt课件,文件包含第六单元第一节第2课时课件PPTpptx、第六单元第一节第2课时教案含练习docx等2份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
初中化学鲁教版九年级上册第三节 氧气优质ppt课件: 这是一份初中化学鲁教版九年级上册第三节 氧气优质ppt课件,文件包含第四单元第三节第2课时课件PPTpptx、第四单元第三节第2课时教案含练习docx等2份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
鲁教版九年级上册第一节 空气的成分获奖ppt课件: 这是一份鲁教版九年级上册第一节 空气的成分获奖ppt课件,文件包含第四单元第一节第2课时课件PPTppt、第四单元第一节第2课时教案含练习docx等2份课件配套教学资源,其中PPT共16页, 欢迎下载使用。













