





初中化学鲁教版 (五四制)八年级全册第二节 化学反应的表示图片课件ppt
展开化学方程式1.定义:_____________________的式子。2.意义:(1)质的方面:表示_______、生成物和反应条件(2)量的方面:①表示各物质之间的_______②表示各物质粒子间的个数比
【特别提醒】读化学方程式时要注意“+”不能读作“加”而应读作“和”,“===”读作“生成”而不能读作“等于”。【导·思】 “化学方程式中各物质的相对分子质量之比就是化学反应中各物质的质量比”,这种说法是否正确?为什么?_______________________________________________________________提示:不正确。相对分子质量之比不一定是物质的质量比,质量比应为每种物质的相对分子质量乘以前面的化学计量数之比。
【解析】由化学方程式可知各物质化学计量数为H2∶2、O2∶1、H2O∶2,A正确;在点燃的条件下氢气和氧气混合可以发生反应,只混合两种气体不发生反应,B错误;由反应方程式可知,4 g氢气与32 g氧气完全反应,可以生成36 g水,C正确;在反应前后,氢原子和氧原子的数目都没有改变,D正确。
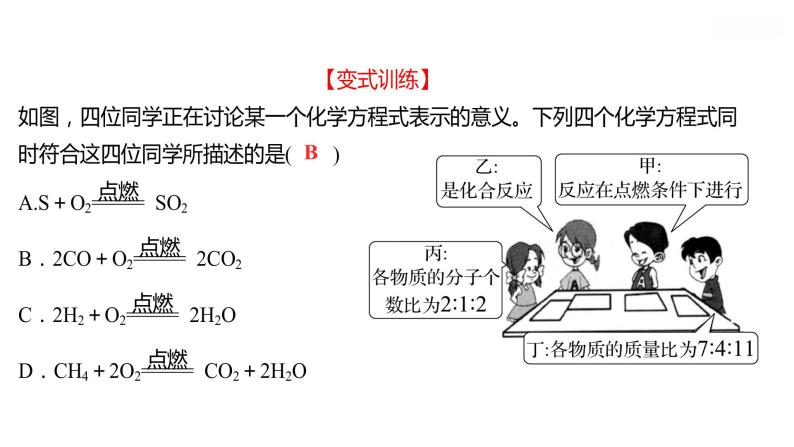
【解析】从给出的图中可以得到如下信息:该反应是化合反应,且反应物与生成物的质量关系是7∶4∶11,分子个数比为2∶1∶2,反应条件为点燃;在A反应中,分子个数比为1∶1∶1;在B反应中,分子个数比、物质质量比、反应条件、反应类型均与题意相符;在C反应中,各物质间的质量比为4∶32∶36=1∶8∶9;在D反应中,反应不是化合反应。
【特别提醒】有关化学方程式意义的两点注意事项1.等号左边为反应物,右边为生成物,等号上方或下方为反应条件2.化学方程式中化学式前的化学计量数表示物质之间的微粒个数比,不是质量比。质量比是化学方程式中各物质的相对分子质量与化学式前化学计量数之积的比
【A层 基础必会】1.(2022·淄博张店区期末)根据化学方程式不能获得该反应的信息是( )A.化学反应的快慢B.化学反应的反应物和生成物C.化学反应发生的条件D.反应物和生成物的质量关系【解析】由化学方程式,无法确定化学反应的快慢;化学方程式“===”左边的是反应物,右边的是生成物;由化学方程式,可以看出反应发生所需要的条件;可以确定反应物和生成物的质量关系。
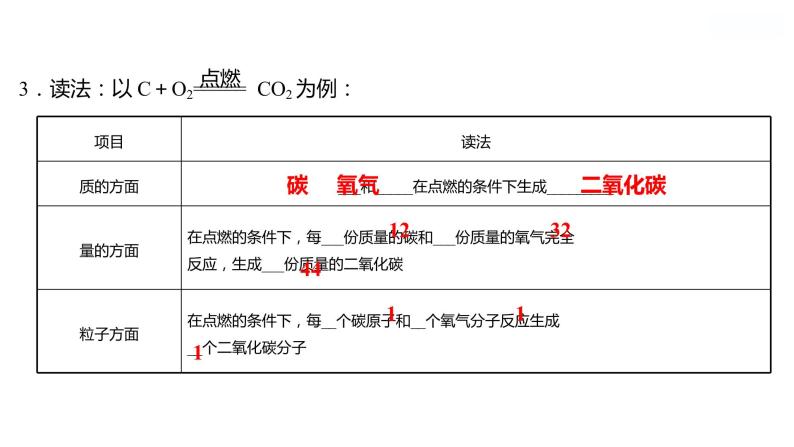
【解析】在化学反应中“+”读作“和”,“===”读作“生成”, A读法错误;物质不能论个数,B读法错误;根据化学方程式可以计算每16份质量的甲烷和64份质量的氧气恰好反应生成44份质量的二氧化碳和36份质量的水, D读法错误。
【解析】A.KMnO4在等号左边,是反应物,故选项说法正确;B.“△”在等号上方,表示反应条件为加热,故选项说法正确;C.K2MnO4在等号右边,是生成物,选项说法正确;D.MnO2是生成物,不是催化剂,故选项说法错误。
【解析】在反应中“+”读作“和”,“===”读作“生成”,故选项A读法错误;从宏观上该反应可读作:点燃条件下,甲烷跟氧气反应生成二氧化碳和水,故选项B读法错误;从微观上,点燃条件下,每1个甲烷分子和2个氧分子生成2个水分子和1个二氧化碳分子,故选项C读法正确;从质量比上,该反应可读作:每16份质量的甲烷和64份质量的氧气在点燃条件下恰好反应生成36份质量的水和44份质量的二氧化碳,故选项D读法错误。
5.在反应4Al+3O2 2Al2O3中,反应物为___________,生成物为_________,反应条件是_________;从反应物、生成物之间的原子、分子个数比来看,每______个铝原子与______个氧分子反应,生成______个氧化铝“分子”,从它们之间的质量比来看,________份质量的Al与_______份质量的O2反应,生成了________份质量的Al2O3。
6.写出下列反应各物质的质量之比(1)2KClO3 2KCl + 3O2↑ ________ ________ _______(2)Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑ ________ _______ ________ _______ _______
【解析】化学反应中各物质质量的计算方法为化学计量数×相对分子质量。(1)KClO3、KCl、O2的质量比为(2×122.5)∶(2×74.5)∶(3×32)=245∶149∶96;(2)Na2CO3、HCl、NaCl、H2O、CO2的质量比为106∶(2×36.5)∶(2×58.5)∶18∶44=106∶73∶117∶18∶44。
【B层 能力进阶】7.铁在氧气中燃烧生成四氧化三铁,在反应中Fe、O2、Fe3O4的质量比为( )A.7∶4∶29 B.3∶2∶1C.21∶8∶29 D.7∶8∶29
【解析】“↓”表示有沉淀生成;化学反应中等号左侧为反应物,右侧为生成物;化学反应中原子种类和数目都不会发生变化;各物质之间的质量比等于物质的相对分子质量与化学式前面的化学计量数的乘积之比,D中是微粒个数比。
Mg与O2反应是金属与气体反应。另外两个是非金属与气体间的反应
【解析】(1)三个反应,都符合“多变一”的特点,都是化合反应。反应中都有氧气参加,故都是氧化反应。反应条件都是点燃。(2)Mg与O2反应是金属与气体反应,另外两个是非金属与气体间的反应等。
12.“宏观和微观相结合”“定性研究和定量研究相结合”是研究化学反应的重要方法。以下是运用上述方法认识红磷燃烧反应的过程,请完成下列问题。(1)写出红磷燃烧的化学方程式_____________________;(2)定性认识,从宏观角度讲,该反应产生了新的物质五氧化二磷;从微观角度讲,该反应生成了新的分子,即___________________;(3)定量认识,从宏观角度讲,_________________________的总质量等于反应后生成的P2O5的质量;从微观角度讲,磷、氧_________的总个数在反应前后保持不变;反应中磷、氧气、五氧化二磷的微粒个数比为___________;(4)红磷燃烧过程中,红磷、氧气、五氧化二磷的质量比为______________。
4P+5O2 2P2O5
初中化学鲁教版 (五四制)八年级全册第二节 化学反应的表示教学课件ppt: 这是一份初中化学鲁教版 (五四制)八年级全册第二节 化学反应的表示教学课件ppt,共17页。PPT课件主要包含了会“说话”的符号,会说“化”的化学符号,元素符号和化学式,说说看,化学方程式,化学反应等内容,欢迎下载使用。
初中化学鲁教版 (五四制)八年级全册第三节 物质组成的表示教课内容ppt课件: 这是一份初中化学鲁教版 (五四制)八年级全册第三节 物质组成的表示教课内容ppt课件,文件包含第1课时化学式及其意义ppt、第四单元第二节物质组成的表示第1课时素材化学式wmv、化学式的意义wmv等3份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
初中鲁教版第二节 化学反应的表示图片课件ppt: 这是一份初中鲁教版第二节 化学反应的表示图片课件ppt,共6页。PPT课件主要包含了不能体现质量守恒定律,表示麻烦,最好的方法是③,化学方程式的定义等内容,欢迎下载使用。













