






初中化学沪教版 (上海)九年级第一学期第一单元 化学的魅力1.3 物质的提纯课文内容课件ppt
展开1、如何理解纯净物和混合物?
1. 混合物——由两种或两种以上物质组成的物质。
例:食盐水;石灰水;海水;碘酒;空气;大理石;盐酸等
2. 纯净物——只含有一种物质。
例:蒸馏水、氧气、二氧化碳、氢氧化钙、碳酸钙、镁、氧化镁等
归纳:混合物没有固定的组成和性质,纯净物有固定的组成和性质, 特别是纯净物有固定的熔点和沸点。
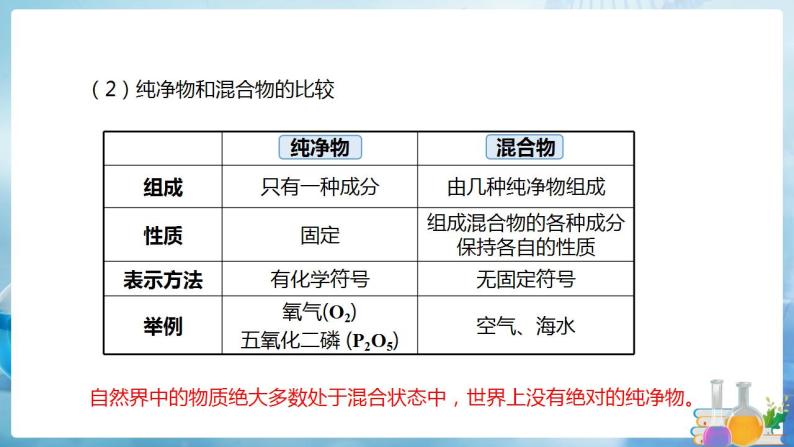
(2)纯净物和混合物的比较
自然界中的物质绝大多数处于混合状态中,世界上没有绝对的纯净物。
物质的纯度(质量分数):混合物中主要成分(或某一成分)的质量百分含量。(含义:每100g某混合物中含有x g某物质)纯度(质量分数)= 某一成分(主要成分)的质量 / 混合物的总质量 x 100%
注意:1. 物质的纯度越高,表示该物质越接近纯净。 例如:24k金的纯度(含金量)为99.99%;硅晶体纯度可达99.999999999%(共11个9)。2.混合物之间没有发生化学反应,保持着各自的性质。因此混合物没有固定的组成和性质。
1、自来水烧开后是否变成纯净水了?
2、喝纯净水好,还是喝矿泉水好?
3、怎样证明买来的纯净水是真的还是假的?
4、怎样鉴别蒸馏水和食盐水?(用多种方法,注意答题的完整性)
练习:判断下列物质是混合物还是纯净物
A 蔗糖______ B 糖水______ C 精盐_______ D 生理盐水______ E 牛奶 _______F 汽水______ G 冷凝水________ H 铁片________ I 氮气______ J 二氧化碳________ K 石灰水________L 熟石灰________
纯净物是一种物质组成的物质,不是一种元素组成的,且一种元素组成的物质也不一定是纯净物。
归纳:纯与不纯是相对的,绝对纯净的物质是没有的。
一般纯度在99%以上的物质就是纯物质。例:纯金(24K金) 纯度99%或99.99% (18K金) 纯度为75%
不纯的物质可以通过物理和化学方法变成纯物质。例:自来水通过蒸馏变成蒸馏水 食盐水通过蒸发得到食盐 氧化铜中混有的铜可通过在空气中加热方法使铜变成氧化铜 铜粉中混有的铁粉可用吸铁石把铁粉吸掉
生活中:农村把稻谷加工成大米时,常用筛子分离大米与糠,提纯成大米;做豆腐常用纱布袋将豆腐渣与豆浆分离提纯豆腐;当铁屑和铜屑混在一起时,可用磁铁分离提纯铁屑等。
纠正:倒数第一句话:得到纯净物改为以提高其纯度
常用的分离和提纯的方法有: (1)物理分离和提纯法: 过滤、结晶、升华、蒸馏、分馏、液化、溶解等。 (2)化学分离和提纯法: 沉淀、置换、加热、分解、洗气等。
(3)本节教材上要求我们重点学习过滤和蒸发
考虑:⑴考虑反应原理以及方法的可行性;⑵考虑除去杂质而不引入新的杂质;⑶考虑操作方法是否简捷;⑷考虑合适的试剂及加入的先后顺序。
化学方法分离与提纯的“五原则”
“五原则”注意十个字:不增、不减、易分、易复、环保。
1.不增:不能引入新的杂质;2.不减:不与被提纯的物质反应使其消耗(可以生成);3.易分离:操作简单,和杂质反应的生成物为沉淀、气体、水等,和主要成分容易分离开来;4.易复原:被提纯物质要容易复原;5.环保:要求所选用的除杂方法,不能产生污染环境的物质。
1、过滤——利用物质的溶解性差异,把不溶于液体的固体和液体分离的一种方法。 原理:让液体通过具有细微孔隙的材料(如滤纸),是不溶性固体截留而除去。 泥水过滤后得到澄清的水(但不纯净)
2、蒸发/蒸馏——沸点不同的两种液体分离或除去溶液中少量难挥发的杂质的一种方法。 把酒精和水的混合物蒸馏后可分别得到酒精和水,海水蒸馏后可得到蒸馏水。
(2)实验仪器及用品:漏斗,滤纸,烧杯,玻璃棒,铁架台(铁圈)。
(1)适用对象:分离固—液(固不溶于液)
(3)操作要点:一贴,二低,三靠
一贴:滤纸紧贴漏斗内壁
二低:滤纸低于漏斗边缘 滤液低于滤纸边缘
三靠:烧杯紧靠玻璃棒 玻璃棒紧靠三层滤纸一侧 漏斗下端尖口紧靠烧杯内壁
过滤的仪器:漏斗铁架台(带铁圈)烧杯玻璃棒(作用:引流)
分离液体或得到纯净的液体
通过蒸发可以把溶于水的固体重新变成固体。
蒸发的四种仪器是:蒸发皿铁架台酒精灯玻璃棒(作用:搅拌)
蒸发操作注意:总量三二,缓热搅拌,余热蒸干1. 蒸发皿中盛放液体的量不超过容积的2/3;2. 加热蒸发时,要用玻璃棒不断搅拌,防止因受热不均局部温度过高引起液滴飞溅;3. 当出现较多固体时,即停止加热,利用余热蒸干,防止固体受热不均四处飞溅;4. 热的蒸发皿可用坩埚钳夹取,放在石棉网上。
通过蒸馏把混在一起的二种液体分离变为纯净液体或者是除去溶在液体中的一些固体.
适用对象:分离液-液、固—液(固溶于液)
特别提醒:1、先通水,再加热2、刚开始收集到的馏分应弃去。3、全程严格控制好温度。
温度计水银球位于蒸馏烧瓶支管口处
溶液体积不超过烧瓶体积的2/3
蒸馏原理:利用各组分沸点不同,将液态混合物分离和提纯的方法。
1、利用互溶液体混合物中各组分沸点不同(通常沸点相差30℃以上),将液态混合物分离和提纯的方法。其过程:将液态物质加热至沸点,使之汽化,然后将蒸汽重新冷凝为液体的操作过程。
氯化钠(泥沙、硫酸钠、 氯化镁 、 氯化钙等)
在实验室,我们是如何除去粗盐中的泥沙的?
1. 实验目的:粗盐中氯化钠的纯度2. 实验仪器和药品:粗盐,水,托盘天平,量筒,烧杯,玻璃棒,药匙,漏斗,铁架台(带铁圈),石棉网,蒸发皿,酒精灯,坩埚钳,胶头滴管,滤纸,火柴3. 实验步骤:称量,溶解,过滤,蒸发,再称量,计算4. 粗盐的纯度(产率)=精盐的质量/粗盐的质量 x100%5. 粗盐提纯中玻璃棒使用了3次:溶解——搅拌,加快溶解;过滤——引流;蒸发——搅拌,防止局部温度过高使液体飞溅。
①一贴:②二低:③三靠:
滤纸边缘低于漏斗边缘,滤液边缘低于滤纸边缘。
向漏斗中倾倒液体时,烧杯的夹嘴应与玻璃棒接触;玻璃棒的底端应和过滤器有三层滤纸处轻轻接触;漏斗颈的末端应与接受器的内壁相接触。
⑴过滤时的“一贴二低三靠”
蒸发——物质的分离和提纯方法之二
⑴适用范围:溶解度随温度变化影响较小的物质而形成的溶液
⑵主要仪器:蒸发皿.玻璃棒.酒精灯.带铁圈的铁架台
①溶质必须不容易分解,不容易被氧化.②加热过程中应该用玻璃棒不断搅拌③接近干燥时停止加热,余热蒸干④停止加热后,不要立即把蒸发皿放在实验台上,应该垫上石棉网
通过上述操作能制得纯净的NaCl吗?
NaCl(泥沙、Na2SO4 、 MgCl2 、 CaCl2)
思考: 加什么试剂? 顺序是什么? 如何操作?
NaCl固体(MgCl2、CaCl2、硫酸盐)
粗盐悬浊液(泥沙、MgCl2、CaCl2、硫酸盐)
NaCl溶液(MgCl2、CaCl2、硫酸盐)
粗盐固体 (泥沙、MgCl2、CaCl2、硫酸盐)
初中化学沪教版 (上海)九年级第一学期1.3 物质的提纯一等奖课件ppt: 这是一份初中化学沪教版 (上海)九年级第一学期1.3 物质的提纯一等奖课件ppt
化学九年级第一学期2.2 神奇的氧气教课内容ppt课件: 这是一份化学九年级第一学期2.2 神奇的氧气教课内容ppt课件,文件包含沪教上海版化学九上222制取氧气课件PPTpptx、加热氯酸钾制取氧气实验mp4等2份课件配套教学资源,其中PPT共33页, 欢迎下载使用。
初中化学沪教版 (上海)九年级第一学期4.2 碳背景图ppt课件: 这是一份初中化学沪教版 (上海)九年级第一学期4.2 碳背景图ppt课件,共35页。PPT课件主要包含了金刚石的用途,刻划玻璃,切割大理石,用石墨做电极,石墨用途,物质的结构,物质的性质,物质的用途,碳原子排列方式不同,正八面体等内容,欢迎下载使用。













