




化学九年级第一学期2.2 神奇的氧气教课内容ppt课件
展开我们知道氧气有许多用途,那么我们如何制取氧气呢?
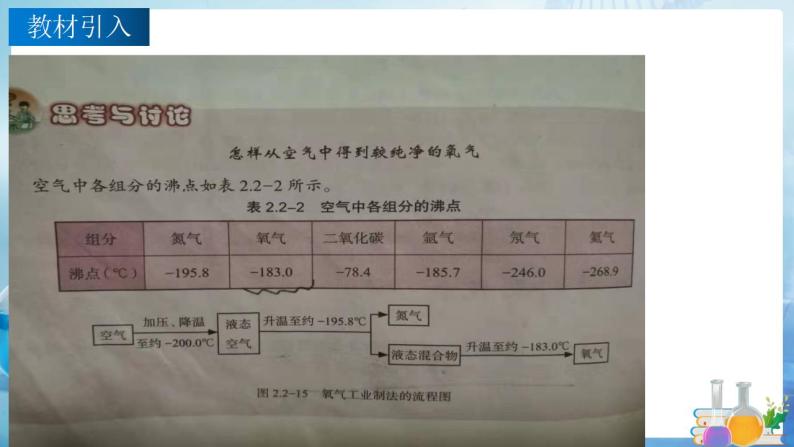
要得到某种物质,应当从富含这种物质或者含有其组成元素的物质去寻找。要得到氧气首先找富含氧气的物质或含有氧元素的物质。
教材解释:1、从富含这种物质中去寻找,其实就是物理法,那么1.3物质的提纯我们学习了很多提纯的方法(可以回忆下有哪些),本节工业上用类似于分馏的方法从空气中分离大量的氧气。2、含有其组成元素的物质去寻找,其实就是化学法(化学反应),我们知道化学反应的微观实质是原子的重新组合。(得含有这种(些)目标元素,才有可能先分解再重新组合成目标产物,不可能无中生有。)
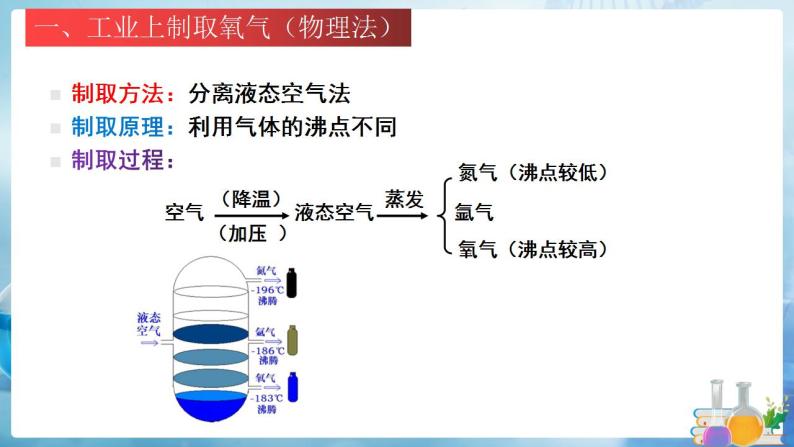
一、工业上制取氧气(物理法)
制取方法:分离液态空气法制取原理:利用气体的沸点不同制取过程:
思考:这种方法制取氧气的优缺点是什么?
1、优点:首先它是工业上的制法,包括后面学习电解水为什么不能在工业上实行,工业上制取二氧化碳等等,都可以掌握这种通用方法。首先,工业上必须考虑成本(价格),其次工业上 必须考虑量的问题(工业上要制取大量目标产物)。优点:1、可以从空气中分离大量氧气;2、成本低。2、缺点:所制取的氧气纯度不高。(至少相比化学法制取低很多)
氯酸钾:白色结晶粉末,可溶于水。
二氧化锰:黑色无定形粉末,难溶于水。
温馨提示:每一种反应物的物理性质、化学性质都要了解清楚,这个粉末状二氧化锰在第四章启普发生器中有个考点,为什么制取用过氧化氢制取氧气不能用启普发生器。
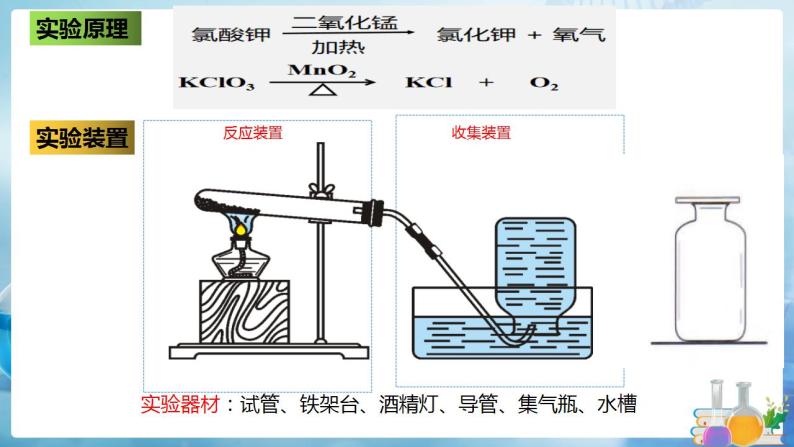
1、将氯酸钾和二氧化锰以质量比3:1的比例均匀混合;2、实验开始时先对固体混合物均匀加热,再用酒精灯外焰对固体混合物集中加热;3、实验结束时先将导管移出水面,再停止加热。
实验器材:试管、铁架台、酒精灯、导管、集气瓶、水槽
依据反应物状态和反应条件
若反应物为固体且反应需要加热,则选用固固加热型。若反应物为固体和液体且反应在常温下即可进行,则选用固液常温型。
加热氯酸钾制取氧气时,因氯酸钾为固体,反应条件为加热,所以选择固固加热型发生装置。
依据气体密度和气体溶解性
将装置导管口的一端伸入水中,再用双手紧握住试管壁,手掌的温度高,使试管中的空气受热膨胀,经导管口排出气泡,手掌离开后导管中形成一段稳定的水柱。这一现象说明了装置不漏气,反之则装置漏气。
1 、查(检查装置气密性)2 、装(把药品装在试管底部)3 、定(把试管固定在铁架台上) 4 、点(点燃酒精灯,先预热、后集中加热)5 、收(收集气体)6 、离(撤离导管)7 、熄(熄灭酒精灯)
可简单归纳为: 茶、 庄、 定、 点、 收、 利、 息
实验室用氯酸钾制取氧气的注意事项
1、要用酒精灯的外焰对准药品部位加热,加热前先对试管进行预热。
2、药品要平铺在试管底部,增大受热面积,便于均匀受热。
3、铁夹要夹在距试管口约1/3处。
4、试管内的导管稍微露出橡皮塞即可,便于气体排出。
5、试管口应略向下倾斜,有些固体试剂受热往往会产生水蒸气,试管口略向下倾斜,防止冷凝水回流到热的试管底部,使试管炸裂。
6、用排水法收集气体时,导管伸到瓶口处即可,当导管口出现连续、均匀的气泡时才可以开始收集(刚开始冒出的气体是受热膨胀的空气,会导致收集的气体不纯)
停止加热时,应先把导管从水槽中撤离出来,再熄灭酒精灯,防止水槽里的水倒流到试管中,冷水与加热后的试管接触,从而导致试管炸裂。
氧气的检验:用带火星木条伸入集气瓶内氧气的验满:用带火星木条放在集气瓶口
【主要成分】过氧化氢 【含量规格】15% 【作用与用途】 本品在分解过程中释放出活泼的新生态氧,可用于养殖池塘的增氧,药性温和,使用方便,无残留且绿色环保。 【用法与用量】 用法:将本品以1000倍水稀释后直接泼洒于养殖池塘中。 用量:每亩水深1米用本品100~150mL,病情严重可加量使用。
过氧化氢分解只产生氧气、水
三、分解过氧化氢制取氧气
实验室中能用过氧化氢制取氧气吗?
取5毫升5%的过氧化氢溶液于试管
怎样知道是否产生了氧气?
伸入带火星的木条进行检验
观察到什么现象?说明了什么?
查阅资料,向其中加入一定量的二氧化锰
看是否产生气泡,伸入带火星的木条。
带火星的木条没有复燃。
常温下,过氧化氢分解缓慢,产生少量氧气。
再伸入带火星的木条进行检验
现象如何?说明了什么?
用过氧化氢溶液制取氧气
1.药品:过氧化氢溶液(无色溶液)、二氧化锰(黑色粉末)
锰酸钾+二氧化锰+氧气
KMnO4 K2MnO4 MnO2 O2
KMnO4 K2MnO4 + MnO2 + O2
教材思考与复习中有个高锰酸钾(紫色)制取氧气的问题
类比氯酸钾制取氧气(固固反应),注意试管口塞一团棉花。
实验室制取氧气的反应原理:
上述三个反应的共同点有哪些?它们属于哪种反应类型?
化合反应与分解反应的特点可以表示如下:
化合反应:A + B → AB
分解反应:AB → A + B
由一种反应物生成两种或两种以上其他物质的反应。
教材要求:二氧化锰在氯酸钾和过氧化氢的分解中起增大反应速率的作用。
在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后没有发生变化的物质叫催化剂。使化学反应加快的催化剂,叫作正催化剂;使化学反应减慢的催化剂,叫作负催化剂。
催化剂的作用是增大反应速率(暂时不考虑负催化剂)。要么某道题具体是填催化作用还是增大反应速率,这个问题留给任课老师们吧。
1.实验室用氯酸钾制氧气的实验中,不需要使用的一组仪器是( )。A.烧杯、玻璃棒 B.大试管、集气瓶C.酒精灯、铁架台 D.导管、单孔塞
2.下列有关催化剂的说法正确的是( )。A.在化学反应后其质量减小B.在化学反应后其化学性质发生了变化C.在化学反应后其质量增加D.催化剂能改变化学反应速率
3.“神州七号”太空舱将利用将航天员呼出的CO2转化为O2,而NiFe2O4的质量和化学性质都不改变,在该过程中NiFe2O4是( )A.反应物B.生成物C.催化剂D.消毒剂
初中化学沪教版 (上海)九年级第一学期第二单元 浩瀚的大气2.2 神奇的氧气教案配套课件ppt: 这是一份初中化学沪教版 (上海)九年级第一学期第二单元 浩瀚的大气2.2 神奇的氧气教案配套课件ppt,文件包含沪教上海版化学九上222制取氧气课件PPTpptx、加热氯酸钾制取氧气实验mp4等2份课件配套教学资源,其中PPT共33页, 欢迎下载使用。
初中化学沪教版 (上海)九年级第一学期2.2 神奇的氧气教案配套ppt课件: 这是一份初中化学沪教版 (上海)九年级第一学期2.2 神奇的氧气教案配套ppt课件,共33页。PPT课件主要包含了情景引入,新课引入,自学导航,一氧气的用途,急救病人,二氧气的利弊,氧气会令钢铁锈蚀,氧气的用途,无味气体,比空气略大等内容,欢迎下载使用。
初中化学沪教版 (上海)九年级第一学期第一单元 化学的魅力1.3 物质的提纯课文内容课件ppt: 这是一份初中化学沪教版 (上海)九年级第一学期第一单元 化学的魅力1.3 物质的提纯课文内容课件ppt,共30页。PPT课件主要包含了物质的纯度,问题讨论,物质的分离和提纯,物质提纯的方法,过滤后一定要洗涤,过滤操作的要点,除去液体得到固体,3主要仪器,4操作要点,操作要点等内容,欢迎下载使用。













