

人教版 (新课标)必修1第一章 从实验学化学综合与测试巩固练习
展开可能用到的相对原子质量:H—1 C—12 N—14 O—16
Na—23 S—32 Cl—35.5 Zn—65
一、选择题(本题包括12小题,每小题4分,共48分,每小题只有1个选项符合题意)
1.电影《闪闪的红星》中,为让被困的红军战士吃上食盐,潘冬子将浸透食盐水的棉袄裹在身上,带进山中……假如潘冬子在实验室中,欲从食盐水中提取出食盐,最好采用的方法是( )
A.过滤
B.萃取
C.蒸发
D.蒸馏
解析:食盐可溶于水,可根据两者的沸点的差异进行分离。
答案:C
2.请你找出适合贴在常用的浓酸、浓碱药品柜上的图标( )
解析:浓酸、浓碱都具有强的腐蚀性。
答案:C
3.除去下列物质中的杂质,所用试剂和方法正确的是( )
解析:A项应用CCl4溶液萃取I2,错误;B项会引入新的杂质KCl,错误;C项CuO能与稀硫酸反应,而Cu不能发生反应,正确;D项CaCO3和CaO都能与盐酸反应,错误。
答案:C
4.下列实验操作正确的是( )
A.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
B.配制溶液定容时,用胶头滴管滴加蒸馏水至溶液凹液面最低点与刻度线相切
C.用分液漏斗分离液体时,先放出下层液体后,再放出上层液体
D.萃取时,将酒精和碘化钾溶液放入分液漏斗中静置
解析:A项会引入NaCl杂质;C项,用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出;D项,酒精和水不分层,所以不能用酒精,也不能用萃取法。
答案:B
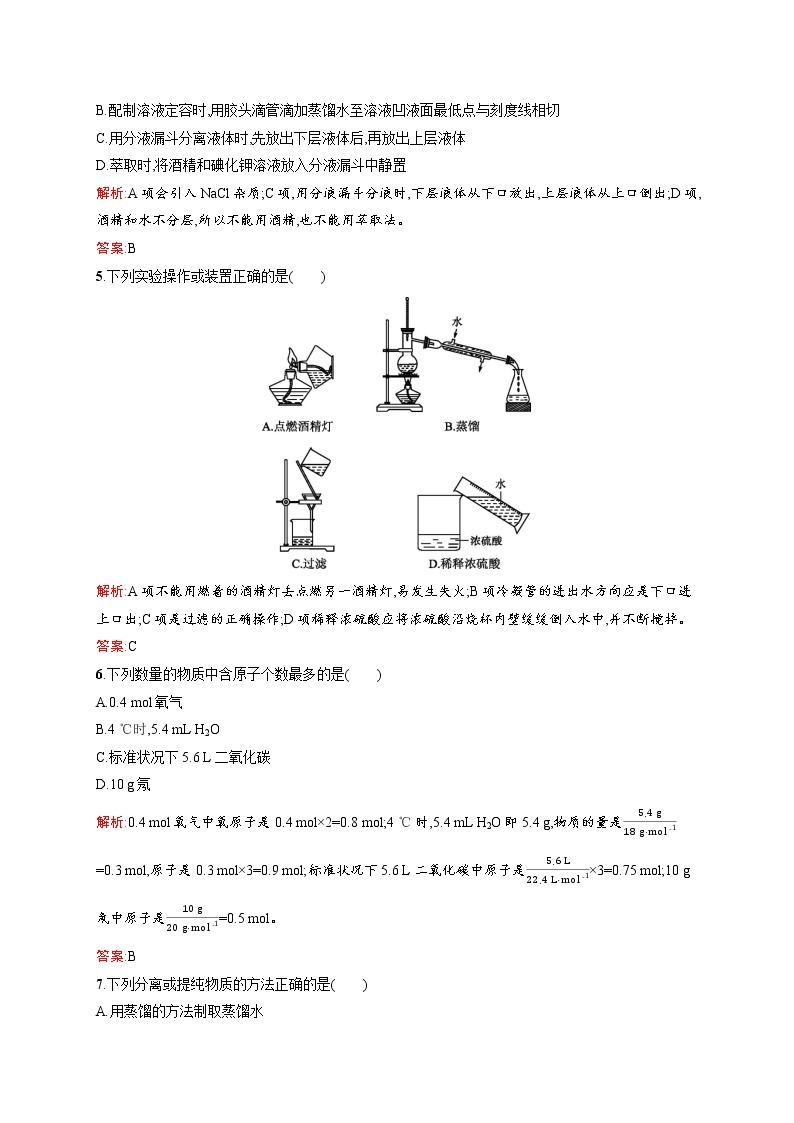
5.下列实验操作或装置正确的是( )
解析:A项不能用燃着的酒精灯去点燃另一酒精灯,易发生失火;B项冷凝管的进出水方向应是下口进上口出;C项是过滤的正确操作;D项稀释浓硫酸应将浓硫酸沿烧杯内壁缓缓倒入水中,并不断搅拌。
答案:C
6.下列数量的物质中含原子个数最多的是( )
A.0.4 ml氧气
B.4 ℃时,5.4 mL H2O
C.标准状况下5.6 L二氧化碳
D.10 g氖
解析:0.4 ml氧气中氧原子是0.4 ml×2=0.8 ml;4 ℃ 时,5.4 mL H2O即5.4 g,物质的量是5.4 g18 g·ml-1=0.3 ml,原子是0.3 ml×3=0.9 ml;标准状况下5.6 L 二氧化碳中原子是5.6 L22.4 L·ml-1×3=0.75 ml;10 g氖中原子是10 g20 g·ml-1=0.5 ml。
答案:B
7.下列分离或提纯物质的方法正确的是( )
A.用蒸馏的方法制取蒸馏水
B.用过滤的方法除去NaCl溶液中含有的少量Na2SO4
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用加热、蒸发的方法可以除去NaCl中CaCl2、MgCl2等杂质
解析:制取蒸馏水可用蒸馏的方法,A正确;NaCl、Na2SO4均溶于水,B错误;BaSO4、BaCO3均难溶于水,C错误;除去NaCl中的MgCl2、CaCl2等杂质,应加入相应的试剂,把Ca2+、Mg2+等除去才行,D错误。
答案:A
8.某溶液经分析,其中只含有Na+、K+、Ca2+、Cl-、NO3-,已知其中Na+、K+、Ca2+、NO3-的浓度均为0.1 ml·L-1,则Cl-的物质的量浓度为( )
A.0.1 ml·L-1
B.0.3 ml·L-1
C.0.2 ml·L-1
D.0.4 ml·L-1
解析:溶液中存在电荷守恒关系。
设Cl-的物质的量浓度为x,由电荷守恒规律得:
c(Na+)+c(K+)+2c(Ca2+)=c(NO3-)+x
0.1 ml·L-1+0.1 ml·L-1+2×0.1 ml·L-1=0.1 ml·L-1+x
解得x=0.3 ml·L-1。
答案:B
9.如图两瓶体积相等的气体,在同温、同压时瓶内气体的关系一定正确的是( )
A.所含原子数相等
B.气体密度相等
C.气体质量相等
D.摩尔质量相等
解析:同温、同压下,两瓶中气体体积相等,则物质的量也相等。N2、O2和NO都是双原子分子,所以原子数也相等。但N2和O2的比例不确定,所以两瓶内的密度、质量和摩尔质量都不一定相等。
答案:A
10.有两种体积相同的某植物的营养液,其配方如下:
对于两种营养液的成分,下列说法中正确的是( )
A.只有n(K+)相同
B.只有n(Cl-)相同
C.完全相同
D.各离子的物质的量完全不同
解析:计算两种营养液中的各种离子的物质的量之和。1号:n(K+)=0.3 ml×1+0.2 ml×2=0.7 ml,n(SO42-)=0.2 ml+0.1 ml=0.3 ml,n(Zn2+)=0.1 ml,n(Cl-)=0.3 ml;2号:n(K+)=0.1 ml×1+0.3 ml×2=0.7 ml,n(SO42-)=0.3 ml,n(Zn2+)=0.1 ml,n(Cl-)=0.1 ml×1+0.1 ml×2=0.3 ml;二者完全相同。
答案:C
11.同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是( )
①密度比为16∶11 ②密度比为11∶16 ③体积比为16∶11 ④体积比为11∶16
A.①③B.①④
C.②③D.②④
解析:同温、同压下等质量的SO2气体和CO2气体的物质的量之比是164∶144=11∶16,则体积比为11∶16,密度之比等于摩尔质量之比,即为16∶11。
答案:B
12.标准状况下,将V L A气体(摩尔质量为M g·ml-1)溶于0.1 L水中,所得溶液密度为ρ g·cm-3,则此溶液的物质的量浓度(ml·L-1)为( )
A.VρMV+2 240
B.1 000VρMV+2 240
C.MV22.4(V+0.1)ρ
D.100VρM(MV+2 240)
解析:该溶液的物质的量浓度c=V22.4V22.4×M+100ρ×1 000 ml·L-1=1 000VρMV+2 240 ml·L-1。
答案:B
二、非选择题(本题包括4小题,共52分)
13.(14分)下面是粗盐提纯的有关操作的叙述,请填空:
(1)称取粗盐5 g。将托盘天平调至平衡后,把两张质量相等的滤纸分别放在两个托盘上,再用镊子夹取5 g砝码放在 盘上,用药匙取用适量粗盐放在 盘上,这时指针如果偏向右边,下步操作是 ,使指针指在标尺中间零点。
(2)用量筒量取10 mL水倒入烧杯中,将称取的粗盐用药匙取出加入水中,边加边搅拌,直至 为止。
(3)过滤混合液时在引流之前往往静置一会儿,其目的是 。若滤液仍然浑浊,应 ,蒸发时,如果蒸发皿中有液滴飞溅,原因是 ,应采取的措施是 。当蒸发皿中出现多量固体时,应 。
(4)用 将固体转移到纸上, 后,回收到指定容器。
解析:固体称量,一般药品需放在滤纸上,特殊药品(如NaOH固体)应放在小烧杯内;称量时,应遵循左物右码的原则;蒸发溶液时,应注意防止液体局部过热,所以应不断搅拌。
答案:(1)右 左 使药匙振动而掉下少量粗盐来加足质量
(2)不再溶解
(3)让杂质沉淀 再过滤一次直至滤液澄清为止 没有用玻璃棒搅拌 用玻璃棒不断搅拌 停止加热
(4)玻璃棒 称量
14.(16分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图所示实验装置,回答下列问题。
(1)写出下列仪器的名称:
① ,② ,④ 。
(2)仪器①~④中,使用时必须检查是否漏水的是 (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是 ,将仪器补充完整后进行的实验操作的名称为 ;②的进水口是 (填“f”或“g”)。
(4)现需配制250 mL 0.2 ml·L-1 NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作:
。
解析:(2)容量瓶需要检查瓶塞是否严密,要求不漏水。(3)利用蒸馏分离液态混合物时,需要利用温度计显示并控制温度;为增加冷凝效果,冷凝器中冷凝水下进上出。(4)向容量瓶中转移液体时,应用玻璃棒引流;配制250 mL溶液应选用250 mL容量瓶。
答案:(1)蒸馏烧瓶 冷凝器 1 000 mL容量瓶 (2)④
(3)温度计 蒸馏 g (4)未用玻璃棒引流,未选用250 mL容量瓶
15.(10分)某学校实验室从化学试剂商店买回18.4 ml·L-1的硫酸。
现用该浓硫酸配制100 mL 1 ml·L-1的稀硫酸。可供选用的仪器有:
①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有 (选填序号),还缺少的仪器有 (写仪器名称)。
(2)配制100 mL 1 ml·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL(保留一位小数)。
量取浓硫酸时应选用 (选填①10 mL、②50 mL、③100 mL)规格的量筒。
(3)实验中造成所配溶液浓度偏高的原因可能是 。
A.容量瓶中原来含有少量蒸馏水
B.未经冷却,立即转移至容量瓶并洗涤烧杯,定容
C.烧杯没有洗涤
D.向容量瓶中加水定容时眼睛一直仰视刻度线
解析:(1)用浓硫酸配制稀硫酸,无需烧瓶、药匙、托盘天平,还缺少100 mL容量瓶、玻璃棒。
(2)根据稀释前后溶液中溶质的物质的量不变可得0.1 L×1 ml·L-1=18.4 ml·L-1×V,V≈0.005 4 L,即5.4 mL,应选用10 mL量筒。
(3)A项无影响;B项未冷却,所加水偏少,浓度偏高;C项,造成溶质减少,浓度偏低;D项,仰视读数,会造成所加水偏多,浓度偏低。
答案:(1)②④⑥ 100 mL容量瓶、玻璃棒
(2)5.4 ①
(3)B
16.(12分)某市售盐酸试剂瓶标签上的部分信息如下:
盐酸
分子式:HCl
相对分子质量:36.5
密度约1.18 g·mL-1
HCl的质量分数:36.5%
(1)该盐酸中HCl的物质的量浓度= ml·L-1。
(2)取该盐酸50 mL加水稀释到500 mL,则稀释后溶液中c(HCl)= ml·L-1。
(3)取稀释后的适量盐酸与足量的锌粒作用,生成0.25 ml氢气,在标准状况下气体的体积是 L。
解析:(1)c(HCl)=
1 L×1 000 mL·L-1×1.18 g·mL-1×36.5%36.5 g·ml-1×1 L
=11.8 ml·L-1。
(2)稀释10倍,溶质不变,浓度必变为原来的110,即1.18 ml·L-1。
(3)V(H2)=0.25 ml×22.4 L·ml-1=5.6 L。
答案:(1)11.8 (2)1.18 (3)5.6
选项
物质
杂质
除杂质所用试剂和方法
A
KCl溶液
I2
加热,升华
B
KNO3
K2SO4
BaCl2溶液,过滤
C
Cu
CuO
稀硫酸,过滤
D
CaCO3
CaO
盐酸,过滤
物质
序号
KCl
K2SO4
ZnSO4
ZnCl2
1
0.3 ml
0.2 ml
0.1 ml
—
2
0.1 ml
0.3 ml
—
0.1 ml
人教版 (新课标)必修1第二章 化学物质及其变化综合与测试练习题: 这是一份人教版 (新课标)必修1第二章 化学物质及其变化综合与测试练习题,共7页。试卷主要包含了5 Mn—55,下列叙述中正确的是,已知,下列离子方程式书写正确的是,下列离子能大量共存的是等内容,欢迎下载使用。
人教版 (新课标)必修1第四章 非金属及其化合物综合与测试精练: 这是一份人教版 (新课标)必修1第四章 非金属及其化合物综合与测试精练,共7页。试卷主要包含了5 Cu—64 Ba—137等内容,欢迎下载使用。
化学必修1第三章 金属及其化合物综合与测试习题: 这是一份化学必修1第三章 金属及其化合物综合与测试习题,共7页。试卷主要包含了5 Fe—56,下列叙述正确的是,下列推理正确的是,200 mL 0,下列实验的现象或表述正确的是,11等内容,欢迎下载使用。













