

湖北省襄阳市第五中学夷陵中学2020届高三下学期联考化学试题
展开襄阳市第五中学、夷陵中学2020届高三下学期联考
理综化学试题
7.一场突如其来的“新冠疫情”让我们暂时不能正常开学。下列说法中正确的是( )
A.垃圾分类清运是防止二次污染的重要一环,废弃口罩属于可回收垃圾
B.为了防止感染“新冠病毒”,坚持每天使用无水酒精杀菌消毒
C.以纯净物聚丙烯为原料生产的熔喷布,在口罩材料中发挥着不可替代的作用
D.中国研制的新冠肺炎疫苗已进入临床试验阶段,抗病毒疫苗需要低温保存
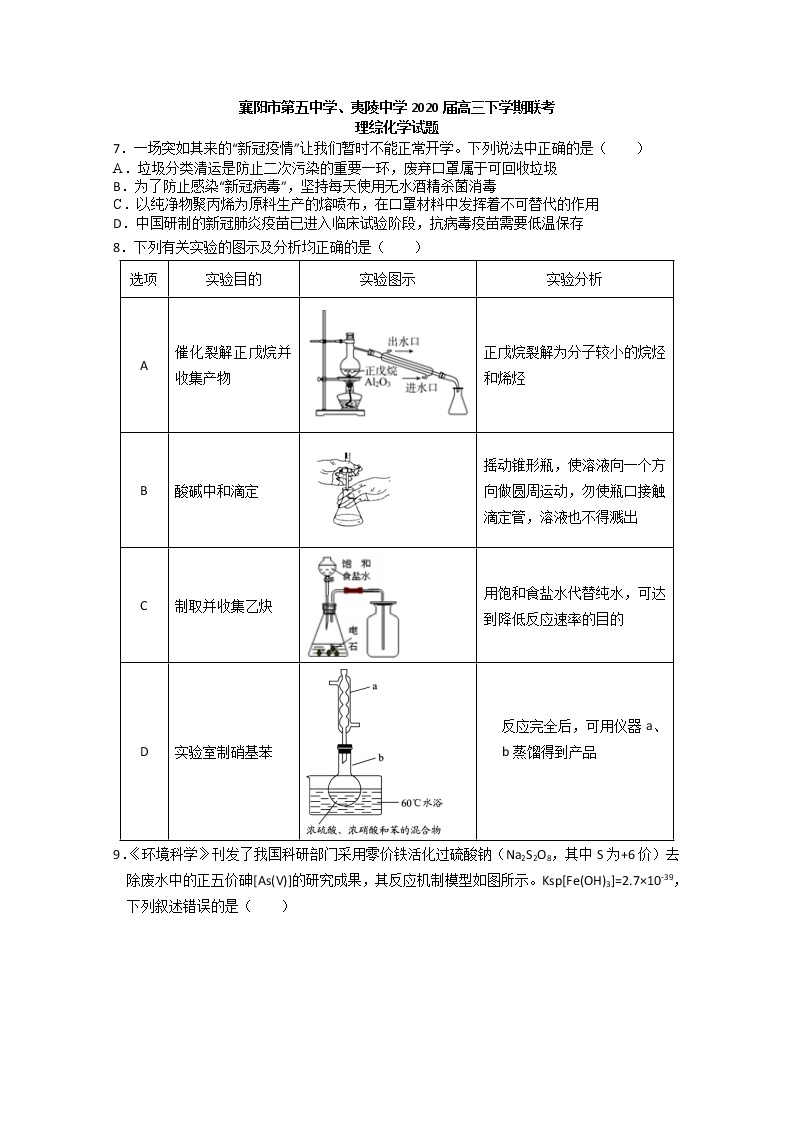
8.下列有关实验的图示及分析均正确的是( )
选项 | 实验目的 | 实验图示 | 实验分析 |
A | 催化裂解正戊烷并收集产物 | 正戊烷裂解为分子较小的烷烃和烯烃 | |
B | 酸碱中和滴定 | 摇动锥形瓶,使溶液向一个方向做圆周运动,勿使瓶口接触滴定管,溶液也不得溅出 | |
C | 制取并收集乙炔 | 用饱和食盐水代替纯水,可达到降低反应速率的目的 | |
D | 实验室制硝基苯 | 反应完全后,可用仪器a、b蒸馏得到产品
|
9.《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠(Na2S2O8,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。Ksp[Fe(OH)3]=2.7×10-39,下列叙述错误的是( )
A.pH越小,越有利于去除废水中的正五价砷
B.1mol过硫酸钠(Na2S2O8)含NA个过氧键
C.碱性条件下,硫酸根自由基发生反应的方程式为:SO4-•+ OH- = SO42-+•OH
D. 室温下,中间产物Fe(OH)3溶于水所得饱和溶液中c(Fe3+)约为2.7×10-18mol·L-1
10.莲花清瘟胶囊对新冠肺炎轻症状患者有显著疗效,其有效成分绿原酸存在如图转化关系,下列有关说法正确的是( )
A.H的分子式为C17H14O4
B.Q中所有碳原子不可能都共面
C.1mol绿原酸与足量NaHCO3溶液反应,最多放出1molCO2
D.H、Q、W均能发生氧化反应、取代反应、显色反应
11.我国某科研团队设计了一种新型能量存储/转化装置(如图所示),闭合K2、断开K1时,制氢并储能。下列说法正确的是( )
A.制氢时,X电极附近pH增大
B.断开K2、闭合K1时,装置中总反应为Zn+2NiOOH+2H2O=Zn(OH)2+2Ni(OH)2
C.断开K2、闭合K1时,K+向Zn电极移动
D.制氢时,每转移0.1NA电子,溶液质量减轻0.1g
12.某新型电池材料结构如图,M、W、X、Y、Z是同周期主族元素,除M外均满足8电子稳定结构,X的最外层电子数是W次外层电子数的3倍,下列说法正确的是( )
A.M的单质可以保存在煤油中
B.原子半径Z>X>Y
C.气态氢化物稳定性X>Y
D.W的最高价氧化物对应的水化物为三元弱酸
13.室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法正确的是( )
A.整个过程中,水的电离程度逐渐增大
B.该温度下H2S的Ka1数量级为10-7
C.曲线y代表继续通入SO2气体后溶液pH的变化
D.a点之后,随SO2气体的通入,的值始终减小
26.二次电池锂离子电池广泛应用于手机和电脑等电子产品中。某常见锂离子电池放电时电池的总反应为:Li1-xCoO2+LixC6=LiCoO2+ C6(x<1)。2018年中国回收了全球可回收锂离子电池总量的69%。但现阶段我国废旧电池回收仍属于劳动密集型产业,效率仍需提高。一种回收该锂离子电池中的锂和钴的流程如下:
已知:① Na2S2O3是一种中等强度的还原剂,遇强酸分解
② Li2CO3溶解度随温度升高而减小
(1) 关于该锂离子电池说法不正确的是
A.锂离子电池中无金属锂,充放电过程中,Li+在两个电极之间往返嵌入和脱嵌
B.集中预处理时,为防止短时间内快速放电引起燃烧甚至爆炸,应先进行放电处理
C.充电时若转移0.01 mol电子,石墨电极将减重0.07g
D.充电时,阳极的电极反应式为LiCoO2-xe-===Li1-xCoO2+xLi+
(2) LiCoO2是一种具有强氧化性的难溶复合金属氧化物,且Co3+在常温、PH=0.5条件下即开始水解。LiCoO2可溶于硫酸得CoSO4。用硫酸酸浸时,需要加入Na2S2O3作助溶剂,从化学反应原理的角度解释原因: ,写出浸出CoSO4的离子反应方程式:
(3) 控制氢离子浓度为4mol/L,反应温度90℃,测得相同时间内离子的浸出率与Na2S2O3溶液的变化关系如图。则酸浸时应选用浓度为 mol/L的Na2S2O3溶液。Na2S2O3溶液浓度增至0.3mol/L时,LiCoO2的浸出率明显下降,可能的原因是 (用化学方程式结合文字说明)
(4) 整个回收工艺中,可循环使用的物质是
(5) 已知15℃左右Li2CO3的Ksp为3.210-2,该温度下Li2CO3的溶解度约为 g。将萃取后的Li2SO4溶液加热至95℃,加入饱和Na2CO3溶液,反应10min, (填操作)得Li2CO3粉末。
27.(14分)亚硝酰硫酸(NOSO4H)纯品为棱形结晶,溶于硫酸,遇水易分解,常用于制染料。SO2和浓硝酸在浓硫酸存在时可制备NOSO4H,反应原理为:SO2 + HNO3 = SO3 + HNO2、SO3 + HNO2 = NOSO4H。
(1)亚硝酰硫酸(NOSO4H)的制备。
①仪器I的名称为______________,打开其旋塞后发现液体不下滴,可能的原因是_________________。
②按气流从左到右的顺序,上述仪器的连接顺序为__________________(填仪器接口字母,部分仪器可重复使用)。
③A中反应的方程式为______________________________________________________。
④B中“冷水”的温度一般控制在20℃,温度不宜过高或过低的原因为____________________________。
(2)亚硝酰硫酸(NOSO4H)纯度的测定。
称取1.500 g产品放入250 mL的碘量瓶中,并加入100.00 mL浓度为0.1000 mol·L-1的KMnO4标准溶液和10 mL 25%的H2SO4,摇匀;用0.5000 mol·L-1的Na2C2O4标准溶液滴定,滴定前读数1.02 mL, 到达滴定终点时读数为31.02 mL。
已知:i:□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
ii:2KMnO4 + 5Na2C2O4 + 8H2SO4 = 2MnSO4 +10CO2↑+ 8H2O
① 完成反应i的化学方程式:
□KMnO4 + □NOSO4H + □______ = □K2SO4 + □MnSO4 + □HNO3 + □H2SO4
② 滴定终点的现象为___________________________________________________。
③ 产品的纯度为__________________。
28.甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知 ①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH= + 93.0kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③甲醇的燃烧热为726.51kJ·mol-1。
要写出表示甲醇燃烧热的热化学方程式,还缺少的热化学方程式为________________。
(2)甲醇可采用煤的气化、液化制取(CO+2H2CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。
①当起始n(H2)/n(CO)=2,经过min达到平衡,0~5min内平均反应速率v(H2)=0.1mol⋅L-1⋅min-1,则该条件下CO的平衡转化率为_____;若其它条件不变,在T2℃(T2>T1)下达到平衡时CO的体积分数可能是____(填标号)
A.<1/4 B.=1/4 C.1/4~1/3 D.=1/3 E.>1/3
②当n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的____点选填“D”、“E”或“F”)。
(3)制甲醇的CO和H2可用天然气来制取:CO2(g)+CH4(g)2CO(g)+2H2(g)。在某一密闭容器中有浓度均为0.1mol·L−1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则该反应的ΔH______(选填“大于”“小于”或“等于”)0。压强p1_______(选填“大于”或“小于”)p2。当压强为p2时,在y点:v(正)__________(选填“大于”“小于”或“等于”)v(逆)。若p2=6Mpa,则T℃时该反应的平衡常数p=_____MPa2(用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
(4)研究表明:CO2和H2在一定条件下也可以合成甲醇,反应方程式为CO2(g)+3H2(g)
CH3OH(g)+H2O(g) [反应Ⅰ]。
①一定条件下,往2L恒容密闭容器中充入2.0mol CO2和4.0mol H2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如下图所示,其中活化能最高的反应所用的催化剂是____(填“A”、“B”或“C”)。
②在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应CO2(g)+H2(g)CO(g)+H2O(g)[反应Ⅱ]。
维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得如下实验数据:
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
注:甲醇的选择性是指发生反应的CO2中转化为甲醇的百分比。
表中数据说明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是_____________________________________________________________________。
35.【化学-选修3:物质结构与性质】(15分)
(1)回答下列问题:
① 处于基态的Ca和Fe原子,下列参数前者小于后者的是_________;
a. 最外层电子数 b. 未成对电子数 c. 第一电离能 d. 原子半径
②有文献表明,迄今为止(至2016年)除氦外,所有其他稀有气体元素都能形成化合物。试简要说明未能制得氦的化合物的理由 _______________________。
(2)H和N可以形成多种化合物。
① 已知联氨(N2H4)的物理性质与水接近,其原因是_____________________;
② 计算表明: N4H62+ 的一种结构如图所示,氢原子只有一种化学环境,氮原子有两种环境,其中的大 π键可表示为_________________。
(3)晶体X只含钠、镁、铅三种元素。在不同的温度和压力下,晶体X呈现不同的晶相。
① γ-X 是立方晶系的晶体。铅为立方最密堆积,其余两种原子有选择的填充铅原子构成的四面体空隙和八面体空隙。在不同的条件下,γ-X 也呈现不同的结构,其晶胞如上图所示。X的化学式为_____________;在(b)型晶胞中,边长为a pm,距离Pb最短的Na有_______个,长度为_______pm(用a表示);Na填充了晶胞中铅原子构成四面体空隙的百分比为________和八面体空隙的百分比为________。已知(a)型晶胞的边长为770 pm,则该型晶体的密度为_________g.cm-3。(只列出计算式)
② α-X是一种六方晶系的晶体,而在α-X中,镁和铅按 1:1 的比例形成类似于石墨的层状结构,钠填在层间。试画出一层α-X 的结构__________。
36.[化学一选修 5:有机化学基础](15分)
化合物G是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:
请回答下列问题:
(1) R的名称是_______________;N中含有的官能团数目是______。
(2) M→N反应过程中K2CO3的作用是____________________________________。
(3) H→G的反应类型是______________。
(4) H的分子式________________。
(5) 写出Q→H的化学方程式:___________________________________。
(6) T与R组成元素种类相同,符合下列条件T的同分异构体有_____种。
①与R具有相同官能团;②分子中含有苯环;③T的相对分子质量比R多14
其中在核磁共振氢谱上有5组峰且峰的面积比为1:1:2:2:2的结构简式有___________。
(7)以1,5-戊二醇() 和苯为原料(其他无机试剂自选)合成,设计合成路线:_________________________________________。








