






华师大版九年级上册2 金属的活动性顺序课堂教学课件ppt
展开取铁钉插入硫酸铜溶液中,观察现象。
同样是金属,铜与铁的化学性质不一样活泼。
第二节 金属的活动性顺序(1)
将镁条、锌粒、铜片分别放入稀盐酸中,现象观察。
最剧烈 较剧烈 不剧烈
用拇指按住盛有锌粒和稀盐酸的试管口,将燃着的火柴接近试管口,松开拇指。
气体燃烧,有轻微的响声
产生的气体为氢气(H2)
镁、锌、铜的金属活动性顺序:
镁 > 锌 > (氢) >铜
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Cu+ HCl - 不反应
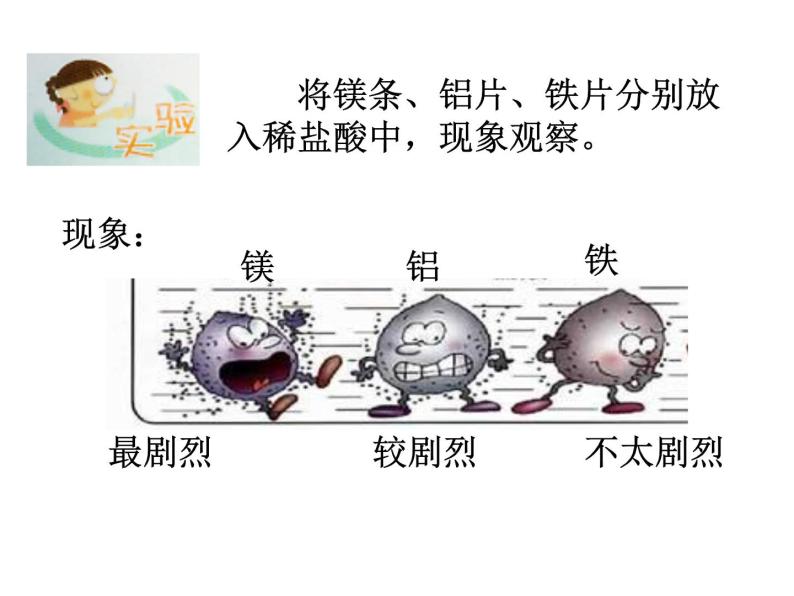
将镁条、铝片、铁片分别放入稀盐酸中,现象观察。
最剧烈 较剧烈 不太剧烈
镁、铝、铁的金属活动性顺序:
2Al+ 6HCl = 2AlCl3 + 3H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑
镁、铝、锌、铁、铜的金属活动性顺序:
镁 > 铝 >锌 >铁>(氢) >铜
将铜丝插入硝酸银溶液中,现象观察。
Cu + 2AgNO3 = Cu(NO3) + 2Ag
铜的化学性质比银活泼,铜可把银从盐溶液中置换出来。
Mg + 2HCl = MgCl2 + H2↑Zn + 2HCl = ZnCl2 + H2↑Mg + H2SO4 = MgSO4 + H2↑Zn + H2SO4 = ZnSO4 + H2↑
像这类由一种单质跟一种化合物起反应生成另一种单质和另一种化合物的反应叫做置换反应。
单质+化合物→新单质+新化合物
说明: 1、在金属活动性顺序表中,越靠前的金属越活泼; 2、前面的金属能后面的金属从它们的盐溶液中置换出来。
说明: 3、排在氢前的金属能将稀盐酸或稀硫酸中的氢置换出来,生成氢气和盐; 4、排在氢后面的金属不能与稀盐酸或稀硫酸发生置换反应。
说明: 5、排在最前面的三种金属K、Ca、Na在常温下就能与水发生剧烈的反应,因此一般不用这三种金属与稀盐酸或稀硫酸置换反应制取氢气,也不用这三种金属来置换溶液中的其他金属。
3、金属活动性与被广泛使用的关系
Fe + CuSO4 = FeSO4 + Cu
不能,因为锡能跟酸反应。Sn + 2HCl = SnCl2 + H2↑
不能,铁能跟波尔多液反应。Fe + CuSO4 = FeSO4 + Cu
1、各金属的化学活动性强弱是不同的;2、常见金属的活动性顺序:
一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,叫做置换反应。
一种新单质和一种新化合物
1、有人利用摄影店的定影液,回收金属银,其中回收方法的反应原理是: Cu+2AgNO3==Cu(NO3)2+2Ag ,则,这个反应属于( )
A 化合反应 B 分解反应C 置换反应 D 复分解反应
2、下列关于金属的叙述与金属活动性顺序无关的是( )A.不用铁制容器配制波尔多液(含有硫酸铜)B.真金不怕火炼C.用稀硫酸识别黄铜(铜锌合金)假冒的黄金指环D.铝制品比铁制品更耐腐蚀
3、根据金属活动性顺序进行分析,下列描述或判断错误的是( )A.在氧气中灼烧时,铁丝要比铜丝反应剧烈B.常温下,金属镁在空气中要比铁容易氧化C.在同一盐酸中反应时,锌片比铁片反应剧烈D.铜活动性不强,故铜不能与硝酸银溶液反应得到金属银
4、有X、Y、Z三种金属,将X、Y、Z分别浸入稀硫酸中,Z溶解,X和Y不溶解;将X浸入Y的硫酸盐溶液中,在X的表面由Y析出。则X、Y、Z的金属活动性由强到弱的顺序为( ) A.Z、Y、X B.Y、Z、X C.Z、X、Y D.Y、X、Z
5、已知甲、乙、丙三种不同的金属,甲在空气中缓慢氧化而腐蚀,乙在空气中加热后仍保持金属光泽,丙需保存在煤油中,以防止氧化,则甲、乙、丙三种金属的活泼性强弱关系为( ) A.甲>乙>丙 B.乙>丙>甲 C.丙>乙>甲 D.丙>甲>乙
6、下列试剂不能用来确定Zn和Cu金属活动性强弱顺序的是( )A.稀H2SO4B.CuSO4溶液C.FeSO4溶液D.ZnSO4溶液
初中科学华师大版九年级上册第3章 金属与盐2 金属的活动性顺序优秀ppt课件: 这是一份初中科学华师大版九年级上册第3章 金属与盐2 金属的活动性顺序优秀ppt课件,文件包含《金属的活动性顺序》课件pptx、《金属的活动性顺序》教案doc、《金属的活动性顺序》练习doc、比较镁锌铁铜分别与稀盐酸稀硫酸的反应flv、铜和硝酸银的置换反应f4v等5份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
初中科学华师大版九年级上册2 金属的活动性顺序一等奖ppt课件: 这是一份初中科学华师大版九年级上册2 金属的活动性顺序一等奖ppt课件,文件包含《金属的活动性顺序》课件pptx、《金属的活动性顺序》教案doc、《金属的活动性顺序》练习doc、比较镁锌铁铜分别与稀盐酸稀硫酸的反应flv、铜和硝酸银的置换反应f4v等5份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
2020-2021学年2 金属的活动性顺序课前预习课件ppt: 这是一份2020-2021学年2 金属的活动性顺序课前预习课件ppt,共12页。PPT课件主要包含了比较快,铜片与硝酸银溶液反应,有银白色物质生成,有银生成,有铜生成,铁与硫酸铜,CuAg,FeCu等内容,欢迎下载使用。













