



广东省雷州市第二中学2023-2024学年高一上学期开学考试化学试题(Word版含答案)
展开B、斩竹槌洗过程中无新物质生成,属于物理变化,故B错误;
C、日晒成干,是水分的蒸发,无新物质生成,属于物理变化,故C错误;
D、捞好的纸膜一张张叠好,用木板压紧,上置重石,将水压出,变化过程中无新物质生成,属于物理变化,故D错误;
故选A。
2.C
【详解】A、该标志是腐蚀品标志,与煤矿或矿井安全无关,不是煤矿或矿井休息室应张贴的警示标志,故选项A不符合题意;
B、该标志是有毒品标志,与煤矿或矿井安全无关,不是煤矿或矿井休息室应张贴的警示标志,故选项B不符合题意;
C、该标志是禁止烟火标志,与煤矿或矿井安全有关,是煤矿或矿井休息室应张贴的警示标志,故选项C符合题意;
D、该标志是国家节约用水标志,与煤矿或矿井安全无关,不是煤矿或矿井休息室应张贴的警示标志,故选项D不符合题意;
故选:C。
3.D
【详解】A、马蹄糕富含糖类,故A错误;
B、油生菜富含维生素,故B错误;
C、蒸肠粉富含糖类,故C错误;
D、牛肉丸富含蛋白质,故D正确。
故选D。
4.C
【详解】A、氧化铁中铁元素为+3价,氧元素为-2价,化合物中各元素正负化合价代数和为0,则氧化铁的化学式为Fe2O3,书写正确;
B、离子符号是在元素符号右上角标出离子所带电荷数及电性。数字在前符号在后,如数字为1则省略不写,镁离子表示为:Mg2+,书写正确;
C、元素符号可以表示一个原子,多个原子在元素符号前加相应数字。2个氢原子:2H,书写错误;
D、化学式可以表示一个分子,多个分子在化学式前加相应数字。3个水分子表示为:3H2O,书写正确。
故选C。
5.D
【详解】A、门捷列夫发现了元素周期律并编制出元素周期表,不符合题意;
B、道尔顿提出了原子学说,不符合题意;
C、拉瓦锡用定量的方法测定了空气的成分,得出空气主要是由氮气和氧气组成,不符合题意;
D、中国药学家屠呦呦因发现青蒿素获得诺贝尔生理医学奖,符合题意。
故选D。
6.D
【详解】A、洗洁精有乳化作用,能乳化油脂,可用于洗涤餐具,故A正确;
B、铝能和空气中的氧气反应生成一层致密的氧化铝薄膜,防止内部的铝进一步反应,故可在铁栏杆刷一层铝粉防锈,故B正确;
C、用水灭火利用的是降低温度至可燃物的着火点以下的原理,故C正确;
D、铁粉生锈是铁和氧气、水共同作用的结果,所以以铁粉为主要成分的食品保鲜剂,是因为铁粉可以吸收袋内的水和氧气,故D错误;
故选D。
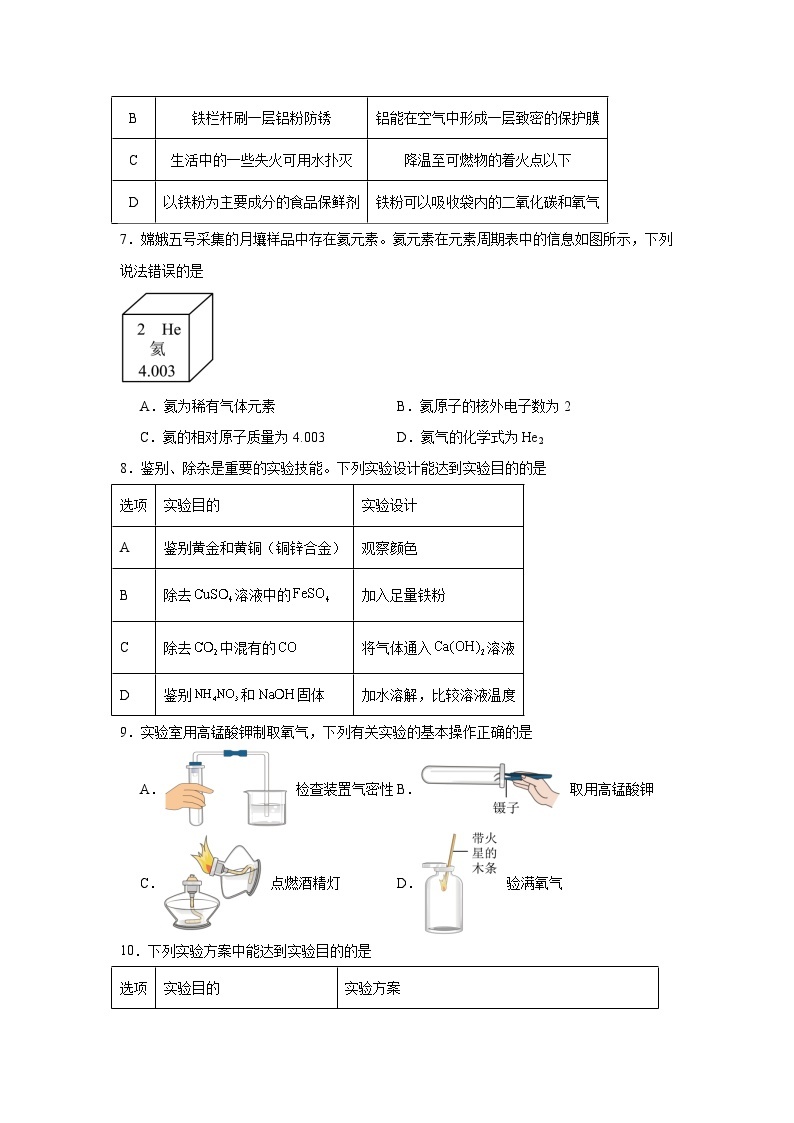
7.D
【详解】A、氦为稀有气体元素,该选项说法正确;
B、元素周期表中左上角的数字表示原子序数,而原子序数=原子的质子数=核外电子数,则氦原子的核外电子数为2,该选项说法正确;
C、元素周期表中,最下方的数字表示相对原子质量,则氦的相对原子质量为4.003,该选项说法正确;
D、氦气为稀有气体,化学式为He,该选项说法错误。
故选D。
8.D
【详解】A、黄金和黄铜均是金黄色的,观察颜色,无法区分,不符合题意;
B、加入足量铁粉,铁和硫酸铜反应生成硫酸亚铁和铜,除去了原物质,不符合题意;
C、将气体通入氢氧化钙溶液,二氧化碳和氢氧化钙反应生成碳酸钙和水,除去了原物质,不符合题意;
D、加水溶解,硝酸铵溶于水吸热,溶液温度降低,氢氧化钠溶于水放出大量的热,溶液温度升高,现象不同,可以区分,符合题意。
故选D。
9.A
【详解】A、检查该装置气密性时,先将导管放入水中,再用手紧握试管,若有气泡冒出,则说明装置气密性良好,该选项操作正确;
B、高锰酸钾为粉末,应将试管倾斜,然后用药匙将药品送至试管底部,该选项操作不正确;
C、禁止用燃着的酒精灯点燃另一只酒精灯,该选项操作不正确;
D、氧气验满时,应将带火星的木条放在集气瓶口,而不是伸入瓶中,该选项操作不正确。
故选A。
10.D
【详解】A、锌与硫酸亚铁反应生成硫酸锌和铁,能除去杂质,但引入新的杂质铁,不符合除杂的原则,故选项不能达到实验目的;
B、氯化钡与硫酸钾反应生成硫酸钡沉淀和氯化钾,能除去杂质,但引入新的杂质氯化钾,不符合除杂的原则,故选项不能达到实验目的;
C、NH4Cl和K2CO3与CaCl2粉末,研磨,均无明显气味,不能鉴别,故选项不能达到实验目的;
D、羊毛主要成分是蛋白质,腈纶属于合成材料,取样灼烧,闻气味,有烧焦羽毛气味的是羊毛,产生特殊气味的是腈纶,可以鉴别,故选项能达到实验目的。
故选D。
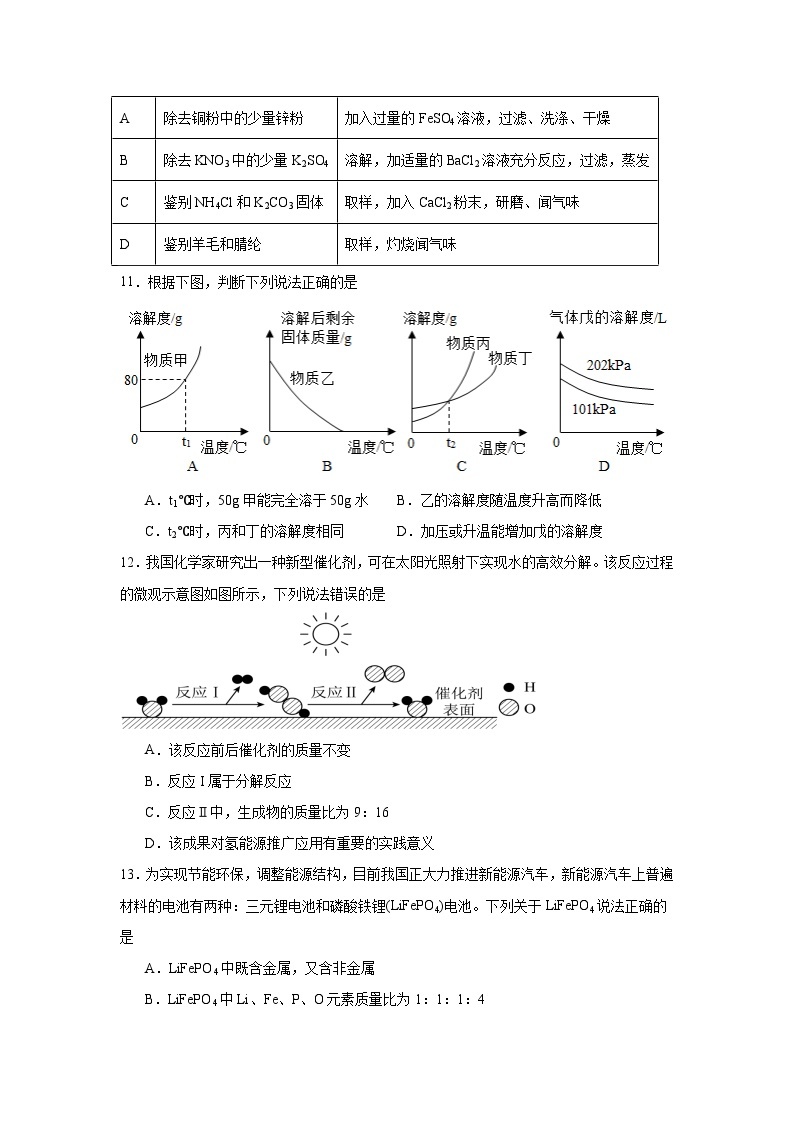
11.C
【详解】A.t1℃时,甲物质的溶解度为80g,也就是100g水中最多能溶解80g物质甲,所以50g甲中只有40g能完全溶于50g水,选项错误。
B.随着温度的升高,溶解后剩余固体的质量在减小,说明溶解的物质变多,所以乙的溶解度随温度升高而升高,选项错误。
C.t2℃时,丙和丁的溶解度相同,正确。
D.压强增大或者温度降低戊的溶解度在升高,所以加压或降温能增加戊的溶解度,选项错误。
故选:C。
12.C
【详解】A、催化剂在反应前后的质量和化学性质不发生改变,不符合题意;
B、由图可知,反应I为水在一定条件下反应成氢气和过氧化氮,该反应有一种反应物和两种生成物,符合“一变多”的特征,属于分解反应,不符合题意;
C、反应II中,该反应可表示为,因此生成物的质量比为(2×18):32=9:8,符合题意;
D、该反应使得水在光照和催化剂的作用下即可分解成氢气和氧气,可以低成本的获取氢能源,对氢能源推广应用有重要的实践意义,不符合题意。
故选:C。
13.C
【分析】磷酸铁锂的化学式为LiFePO4,属于盐,是一种含有多种元素的化合物。
【详解】A、Li、Fe属于金属元素,P、O属于非金属元素,故LiFePO4是由金属元素和非金属元素组成的,不能说LiFePO4中既含金属,又含非金属,A错误;
B、LiFePO4中Li、Fe、P、O元素质量比为(7×1):(56×1):(31×1):(16×4)=7:56:31:64,B错误;
C、若Li为+1价,而P为+5价,O为-2价,根据化合物中正负化合价的代数和为0,则Fe为+2价,C正确;
D、1个LiFePO4中含有7个原子,未说明LiFePO4的个数,D错误。
故选C。
14.B
【详解】A、单质是由同种元素组成的纯净物,故单质只含一种元素,但是含有一种元素的物质不一定是单质,如氧气和臭氧的混合物,由氧元素组成,属于混合物,不符合题意;
B、酸的溶液显酸性,能使紫色石蕊溶液变红,能使紫色石蕊溶液变红的一定是酸性溶液,符合题意;
C、元素是质子数相同的一类原子的总称,故同种元素粒子的质子数一定相同,质子数相同的粒子不一定属于同种元素,如NH3和H2O质子数相同,不属于同种粒子,不符合题意;
D、氢氧化钙显碱性,能与酸性物质反应,可用来改良酸性土壤,氢氧化钠也显碱性,但是氢氧化钠腐蚀性较强,不能用于改良酸性土壤,不符合题意。
故选B。
15.A
【详解】A.加热高锰酸钾制取氧气,分解生成氧气,所以固体质量减小,直至不在生成氧气,固体质量不变,正确;
B.分解等质量等浓度的过氧化氢溶液,二氧化锰仅仅只做催化剂,只会改变反应速率,即减少反应所需时间,不会改变生成氧气的量,选项错误;
C.将等质量的镁片、铁片加入足量稀硫酸中,镁的活性大于铁,所以镁反应所需时间更短,且镁的相对原子质量更小所以产生氢气更多,选项错误;
D.用燃烧红磷的方法测定空气中氧气含量,压强会先增大(因为反应放热)后减小(因为消耗氧气),最终压强比原来低五分之一,选项错误。
故选:A。
16.(7分,除标明分数外,其余每空1分) (1)纯净物
(2) 4/四 10:9 氧元素
(3)(2分)
(4)
【详解】(1)CuSO4属于纯净物;
(2)根据胆矾的化学式,胆矾是4种元素组成的,其中氢、氧原子个数比为(5×2):(5+4)=10:9;铜、硫、氧、氢四种元素的质量比为64:32:(16×9):(1×10)=32:16:72:5,通过对比可知,氧元素的质量最大,则氧元素质量分数最大;
(3)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:;
(4)氧化亚铜中氧元素的化合价为-2价,设氧化亚铜中铜元素的化合价为x,则2x+(-2)=0,解得x=+1,则Cu2O中铜元素的化合价为+1价表示为:。
17.(8分,除标明分数外,其余每空1分)(1)过滤
(2)汞原子之间的间隔随温度的升高而增大(答案合理即可)
(3) 二氧化氯 BD
(4)(2分)
(5) 5.6 bc
【详解】(1)口罩防护的原理是戴在口鼻部位用于过滤进入口鼻的空气,以达到阻挡有害的气体、气味、飞沫、病毒等物质的作用,所以口罩防护相当于化学实验操作中的过滤,故填:过滤。
(2)水银是汞的俗称,汞由汞原子构成,用水银温度计测量体温,是由于温度升高,汞原子之间的间隔随温度的升高而增大,体积增大,汞柱上升,故填:汞原子之间的间隔随温度的升高而增大(答案合理即可)。
(3)氯元素有多种化合价,氯元素的氧化物一般读作几氧化几某,所以ClO2读作二氧化氯。故填:二氧化氯。
A.NaClO由钠、氯、氧元素组成,属于含氯消毒剂,故A错误;
B..过氧化氢(H2O2)由氢元素和氧元素组成,不属于含氯消毒剂,故B正确;
C.氯气(Cl2)由氯元素组成,属于含氯消毒剂,故C错误;
D.过氧乙酸(C2H4O3)由碳、氢、氧三种元素组成,不属于含氯消毒剂,故D正确。
故填:BD。
(4)酒精完全燃烧是酒精与氧气在点燃的条件下反应生成二氧化碳和水,该反应的化学方程式为:,故填:。
(5)①酸雨是pH<5.6的降水,故填:5.6。
②a.CO2 不是空气污染物,也不会形成酸雨,故a错误;
b.SO2 是空气污染物,会形成硫酸型酸雨,故b正确;
c.NO2是空气污染物,会形成硝酸型酸雨,故c正确;
d.CO是空气污染物,但不会形成酸雨,故d错误。
故填:bc。
18.(1)集气瓶(1分)
(2) AF (1分) (2分)
(3) 石灰石或大理石和稀盐酸 (1分) ①(1分)
(4)7.5(1分)
(5)减少氯化钠固体直至指针指向中间(减少固体药品,合理即可)(1分)
(6)ABD(2分)
【详解】(1)b是集气瓶。
(2)氯酸钾制取氧气需要加热,发生装置选择A。氧气密度比空气大可用向上排空气法收集,不易溶于水可用排水法收集,排空气法收集气体较干燥但不纯净,排水法收集气体较纯净但不干燥。所以收集装置选择F。所以发生装置和收集装置是AF。氯酸钾在二氧化锰催化和加热条件下反应生成氯化钾和氧气,化学方程式为。
(3)实验室使用石灰石或大理石和稀盐酸制取二氧化碳。C装置关闭止水夹,当反应停止后固体和液体分离,则液面在多孔隔板下,所以观察到的现象是①。
(4)配制该溶液应称量氯化钠固体50g×15%=7.5g。
(5)称量一定量的固体药品,左物右码,发现指针偏左则药品质量偏大,需要减少氯化钠固体直至指针指向中间。
(6)A、量取水时,俯视读数,读数偏大,水偏少,配制溶液溶质质量分数偏大;
B、称量时所用砝码生锈,量取固体氯化钠质量偏多,配制溶液溶质质量分数偏大;
C、氯化钠固体不纯,氯化钠质量偏少,配制溶液溶质质量分数偏小;
D、将水倒入烧杯时,有少量水溅出,水偏少,配制溶液溶质质量分数偏大;
故选ABD。
19.(1)A(1分)
(2)氢氧化钾溶液与稀硫酸恰好完全反应(1分)
(3)(2分)
(4)实验后溶液中酚酞呈无色,不存在 KOH 碱性物质(1分)
(5)红色固体消失,溶液变为黄色(1分)
(6)反应后生成的 K2SO4也能与 BaCl2反应产生白色沉淀(2分)
(7)BCD(2分)
【详解】(1)由pH变化曲线可知,溶液刚开始pH<7,呈酸性,此时溶液应是H2SO4溶液,随着溶液的加入,溶液pH逐渐增大到7,最后大于7,所以应是将KOH溶液滴入H2SO4溶液中,故选A;
(2)由图2可知,随着反应的进行溶液温度升高,说明酸碱中和反应为放热反应,B点此时温度达到最高值,证明KOH溶液和H2SO4溶液恰好完全反应;
(3)氢氧化钾与硫酸反应生成硫酸钾和水,反应的化学方程式为2KOH+H2SO4=K2SO4+2H2O;
(4)氢氧化钾溶液呈碱性,能够使酚酞变红,根据题目信息,通过图3所示实验,他观察到溶液由红色变成无色,说明此时溶液一定不呈碱性,即反应后溶液中一定不含有氢氧化钾,故可得出猜想三不合理
(5)方案一:根据实验结论溶液中有H2SO4 ,猜想二正确,所以取少量反应后的溶液于试管中, 加入Fe2O3粉末,氧化铁与硫酸反应生成硫酸铁和水,可观察到铁锈减少(或消失),溶液变成黄色;
(6)方案二是不合理的,因为氯化钡与硫酸钾反应也会产生白色沉淀,无法证明H2SO4一定存在;
(7)A、氯化钠与硫酸不反应,不能用来证明硫酸过量,不符合题意;
B、锌与稀硫酸反应生成硫酸锌和氢气,有气泡产生,即可证明有硫酸过量,符合题意;
C、 碳酸钾和稀硫酸反应生成硫酸钾、二氧化碳和水,有气泡产生,即可证明硫酸过量,符合题意;
D、CuO和硫酸反应生成蓝色硫酸铜溶液和水,观察到溶液变蓝,即可证明硫酸过量,符合题意;
故选BCD。
20.(1)(2分)
(2)(5分)解:设参与反应的铁的质量为x
x=16.8g
21g 生锈铁钉中铁单质的质量分数为。
(3) (3分)
【详解】(1)铁钉表面有铁锈,铁锈(主要成分是氧化铁)先与稀硫酸反应生成硫酸铁和水,铁再与稀硫酸反应生成硫酸亚铁和氢气,故ab 段不产生氢气的原因是;
(2)由表格可知,反应生成的氢气的质量为0.6g,利用方程式计算出参与反应的铁的质量,从而求出铁单质的质量分数,解析见答案;
(3)根据表中数据分析可知,每20g稀硫酸完全反应生成0.2g氢气,故第2次加入的20g稀硫酸,只有10g与铁反应生成了氢气,故在30g稀硫酸量的位置开始产生氢气,当加入稀硫酸90g时,铁完全反应生成氢气0.6g,描点画图为。
21.(1)Al2O3+3H2SO4=Al2(SO4)3+3H2O(2分)
(2)硫酸钙/CaSO4(1分)
(3)2x+y=6(1分)
(4)二氧化硫、氧气、水反应生成硫酸(1分)
(5) HCl (1分) (2分)
(6)氧气不易溶于水,若水膜过厚与活性炭接触的氧分子减少(2分)
【详解】(1)氧化铝和硫酸反应生成硫酸铝和水,化学方程式为。
(2)调节pH约为3.6目的是消耗溶液中过量的酸,则过滤Ⅰ后滤液中有硫酸铝和硫酸,硫酸和碳酸钙反应生成微溶于水的硫酸钙、水和二氧化碳,根据制备碱式硫酸铝,而使用的是滤液,所以滤渣中没有铝元素的沉淀,则滤渣Ⅱ的主要成分是硫酸钙。
(3)化合物中各元素正负化合价代数和为0,铝元素为+3价,硫酸根为-2价,氢氧根为-1价,所以(+3)×2+(-2x)+(-1y)=0,2x+y=6;
(4)根据二氧化硫烟气中含有氧气,则经完全热分解放出的SO2量会小于吸收的SO2量,则氧气和二氧化硫会发生反应导致释放的二氧化硫变少。溶液酸性变强,则溶液中氢离子增加,则推测有酸生成,则主要原因是二氧化硫、氧气、水反应生成硫酸,硫酸受热不分解为二氧化硫导致释放二氧化硫减少,且硫酸解离出氢离子,导致溶液酸性变强。
(5)①化学反应前后元素的种类不变及反应前后原子的种类和数目不变,根据H2S、FeCl3转化为X和S、FeCl2,X、FeCl2、O2转化为FeCl3、H2O,可知,X一定含有H、Cl(根据FeCl3和FeCl2中铁、氯原子个数比),是HCl。
该脱硫总反应是H2S和O2反应生成H2O和S,化学方程式为。
(6)要吸附氧化H2S需要氧气,且氧气需要在活性炭表面转化为氧原子后与硫化氢分子反应。则H2S的氧化去除率减小可能与能和活性炭接触的氧分子的多少有关。氧气不易溶于水,所以若水膜过厚与活性炭接触的氧分子减少,导致H2S的氧化去除率减小。
雷州市第二中学2023-2024学年高一下学期开学考试化学试卷(含答案): 这是一份雷州市第二中学2023-2024学年高一下学期开学考试化学试卷(含答案),共16页。试卷主要包含了单选题,填空题,推断题,实验题等内容,欢迎下载使用。
72,广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题: 这是一份72,广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题,共1页。试卷主要包含了225等内容,欢迎下载使用。
72,广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题(1): 这是一份72,广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题(1),共7页。试卷主要包含了《天工开物》中记载,化学让我们的生活更美好,N4分子结构为正四面体,已知CaCO3的Ksp=2等内容,欢迎下载使用。












