






人教版化学必修2 第五章 综合测评(课件PPT)
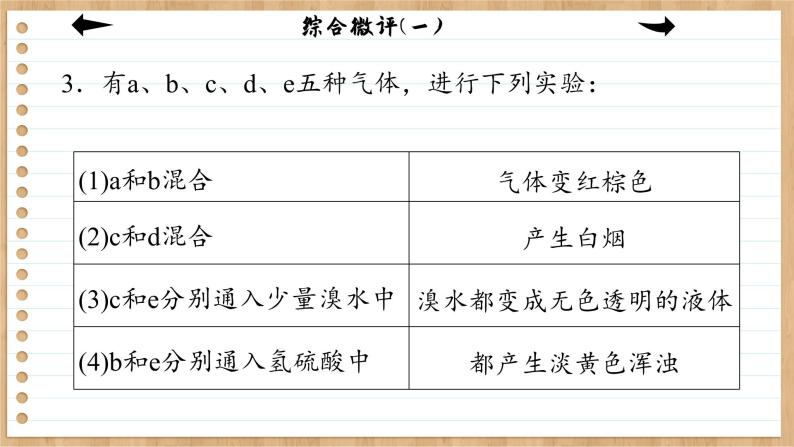
展开第五章 化工生产中的重要非金属元素综合微评(一)测评范围:第五章 满分:100分 时间:90分钟1.化学已经渗透到人类生活的各个方面,下列说法不正确的是 ( )A.在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放量B.“光化学烟雾”“臭氧空洞”的形成都与氮氧化合物有关C.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放D.二氧化碳含量属于空气质量日报中空气污染指数指标D解析:在家用燃煤中加入适量的生石灰,生石灰可与煤燃烧生成的SO2反应生成CaSO3,最终生成CaSO4而固硫,A项正确;氮的氧化物和碳氢化合物引起“光化学烟雾”,氟氯烃和氮的氧化物都会造成“臭氧空洞”,B项正确;使用太阳能等代替化石燃料,减少CO2等温室气体的排放,C项正确;CO2含量不属于空气质量日报中空气污染指数指标,D项错误。2.下列关于物质性质的叙述中正确的是( )A.Cl2能与金属活动性顺序表中的大多数金属反应B.N2是大气的主要成分之一,雷雨时可直接转化为NO2C.硫是黄色、能溶于水的晶体,既有氧化性又有还原性D.硅是应用广泛的半导体材料,常温下化学性质活泼A解析:Cl2具有强氧化性,能与金属活动性顺序表中的大多数金属反应,A正确;雷雨时N2与O2反应可生成NO,而不是NO2,B错误;硫难溶于水,C错误;硅在常温下化学性质不活泼,D错误。3.有a、b、c、d、e五种气体,进行下列实验:a、b、c、d、e依次可能是( )A.O2、NO、HCl、NH3、CO2B.O2、NO、NH3、HCl、SO2C.NO、O2、NH3、HCl、SO2D.HCl、CO2、NH3、H2S、CH4C解析:a和b混合后气体变成红棕色,可知a和b分别为NO、O2中的一种;b通入氢硫酸中产生淡黄色浑浊,则b为O2,a为NO;c和d混合产生白烟,则c和d分别为NH3、HCl中的一种;c通入少量溴水中使溴水变成无色透明液体,则c为NH3,d为HCl;e通入少量溴水中,溴水变成无色透明的液体,e通入氢硫酸中产生淡黄色浑浊,则e为SO2。4.下列有关物质性质与用途具有对应关系的是( )A.Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂B.ClO2具有还原性,可用于自来水的杀菌消毒C.SiO2硬度大,可用于制造光导纤维D.NH3易溶于水,可用作制冷剂A解析:人呼出的CO2可与Na2O2反应生成O2,故可用作呼吸面具供氧剂,A项正确;ClO2具有氧化性,可用于自来水的杀菌消毒,B项错误;SiO2可用于制造光导纤维的原因是其导光性能好,与硬度无对应关系,C项错误;液氨汽化吸收大量的热是其用作制冷剂的原因,D项错误。。5.下列关于SO2和NO2的叙述中,正确的是( )A.SO2可使紫色石蕊溶液褪色B.SO2与水作用生成H2SO4C.可用排水法收集NO2D.实验室可用NaOH溶液处理NO2和SO2废气D解析:SO2的漂白性是有限的,不能使紫色石蕊溶液褪色,A错误;SO2与水作用生成H2SO3,B错误;NO2与水反应:3NO2+H2O===2HNO3+NO,C错误。6.关于非金属元素Si、N、S的叙述中,正确的是( )A.通常情况下,它们的单质均为气体B.它们在自然界中都存在游离态形式C.它们都有对应的含氧酸D.每种元素都只有一种氧化物C解析:A项,Si、S的单质常温下为固体,而N的单质为气体,故不选A;B项,Si在自然界中以化合态存在,故不选B;C项,均为非金属,存在对应的酸性氧化物,则都有对应的含氧酸,故选C;D项,N和S的氧化物有多种,故不选D。7.在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终充满烧瓶,则a和b分别是( )A解析:B选项不能充满;C选项Cl2几乎不溶于饱和食盐水;D选项氮气不溶于盐酸。8.某实验过程如图所示,则图③试管中的现象是( ) A.无明显现象,因稀H2SO4不与铜反应B.铜片溶解,产生无色气体,该气体遇到空气不变色C.铜片溶解,放出红棕色有刺激性气味的气体D.铜片溶解,产生无色气体,该气体在试管口变为红棕色D解析:生成的Cu(NO3)2在H2SO4的酸性条件下相当于又有了HNO3,铜片会继续溶解生成NO。9.下列说法正确的是( )A.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸B.在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应C.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中含SO42-D.将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化A解析:A项,浓硝酸在光照下发生分解生成NO2,NO2溶于浓硝酸中使浓硝酸呈黄色;B项,Cl2氧化I-生成I2,淀粉遇I2变蓝色;C项,溶液中若存在Ag+或SO32-也会产生相同的实验现象;D项,常温时,Cu与浓硫酸不发生反应。10.甲和乙两种物质混合反应(反应可加热),将所得气体通入适量的丙中,丙中不能产生明显化学现象的是( )B 解析:A项,C与浓硫酸在加热条件下反应生成CO2、SO2和H2O,澄清石灰水能与CO2、SO2反应产生CaCO3或CaSO3白色沉淀;B项,MnO2与稀盐酸不反应,加热时也得不到Cl2,所以品红溶液不褪色;C项,浓氨水与碱石灰作用可得NH3,NH3溶于水与AlCl3溶液反应产生Al(OH)3白色沉淀;D项,Cu与浓硝酸反应产生NO2,NO2溶于水生成HNO3和NO,HNO3能将HSO3-氧化为SO42-,从而产生BaSO4白色沉淀。11.下列由相关实验现象所推出的结论正确的是( )A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42-C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应D.分别将充满HCl、NH3的烧瓶倒置于水中,液面均迅速上升,说明二者易溶于水D 解析:A项,Cl2溶于水生成的HClO具有氧化性,能使品红溶液褪色,SO2能使品红溶液褪色体现了SO2的漂白性,错误;B项,溶液中也可能含有SO32-,SO32-与酸化的Ba(NO3)2溶液反应,被其中的H+和NO3-氧化为SO42-,SO42-与Ba2+结合为BaSO4沉淀,错误;C项,铁与硝酸发生的不是置换反应,错误。12.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )解析::A项,铁粉过量,反应生成亚铁离子,加入KSCN溶液,溶液不显红色,正确;B项,Cu和Fe3+发生氧化还原反应Cu+2Fe3+===Cu2++2Fe2+,所以没有黑色沉淀生成,溶液由黄色变为蓝色,错误;C项,向蔗糖中滴加浓硫酸,蔗糖变黑,并放出有刺激性气味的气体,可证明浓硫酸具有脱水性和强氧化性,正确;D项,在金属活动性顺序中铜排在氢的后面,不能与稀硫酸反应,错误。13.类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。以下类推的结论中正确的是( )A.SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色B.盐酸与镁反应生成氢气,故硝酸与镁反应也生成氢气C.SO2能使品红溶液褪色,故CO2也能使品红溶液褪色D.常温下浓硫酸能使铁和铝钝化,故常温下浓硝酸也能使铁和铝钝化D解析:A项中CO2无还原性,不能使酸性KMnO4褪色;B项中金属与HNO3反应不产生H2;C项中CO2无漂白性,不能使品红褪色。14.下列实验目的可以用如图所示装置达到的是( ) A.以MnO2、浓盐酸为原料,制备、干燥、收集Cl2B.以Na2SO3固体、质量分数为70%的浓硫酸为原料,制备、干燥、收集SO2C.以浓氨水、生石灰为原料,制备、干燥、收集NH3D.以Cu、稀硝酸为原料,制备、干燥、收集NOB解析:A项,MnO2与浓盐酸的反应需要加热,不符合题意;C项,NH3是碱性气体,易被浓硫酸吸收,不符合题意;D项,NO不能用排空气法收集,因为2NO+O2===2NO2,不符合题意。15.如图所示是验证气体性质的实验装置,下列有关说法不正确的是 ( ) A.若水槽中是水,试管中是NO2,可观察到试管中液面上升,若再充入适量的O2可使液体充满整个试管B.若水槽中是NaOH溶液,试管中是Cl2,可观察到试管中液面上升C.若水槽中是水并滴有几滴紫色石蕊试液,试管中是SO2,可观察到试管中液面上升,试管中溶液呈无色D.若水槽中是水并滴有几滴酚酞试液,试管中是NH3,可观察到试管中液面上升,试管中溶液呈蓝色解析:二氧化氮与水反应生成硝酸和NO,NO不溶于水,则可观察到试管中液面上升,若再充入适量的O2,会发生反应4NO+3O2+2H2O===4HNO3,当NO与O2的体积比为4∶3时,可使液体充满整个试管,A项正确;氯气与NaOH溶液反应生成NaCl、NaClO和H2O,则可观察到试管中液面上升,B项正确;二氧化硫与水反应生成亚硫酸,亚硫酸能使紫色石蕊试液变红,则可观察到试管中液面上升,试管中溶液呈红色,C项错误;氨气易溶于水,溶液显碱性,能使酚酞试液变红,则可观察到试管中液面上升,试管中溶液呈红色,D项错误。16.(12分)实验室模拟合成氨和氨催化氧化的流程如图:已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。(1)从图中选择制取气体的合适装置:氮气________、氢气________。a b (2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有______________、___________________________。干燥气体控制氢气和氮气的流速(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,________(填“会”或“不会”)发生倒吸,原因是________________________________________________________________________。不会 混合气体中含有大量难溶于水的氮气、氢气(4)用乙装置吸收一段时间氨气后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是_______________________________________,锥形瓶中还可观察到的现象是___________________________。氨的氧化反应是一个放热反应 有红棕色气体产生(5)写出乙装置中氨氧化的化学方程式:___________________________________________________。(6)反应结束后锥形瓶内的溶液中含有的离子为H+、OH-、________、________。NH4+ NO3-17.(12分)A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去):请回答下列问题:(1)若X是强氧化性单质,则A不可能是________(填序号)。a.C b.N2 c.S d.Na e.Mge (2) 若A能使湿润的红色石蕊试纸变蓝色,C为红棕色气体,则A转化为B的化学方程式为______________________________________________________。(3) 若A、B、C三种化合物的水溶液均呈酸性,写出A和B反应的化学方程式:______________________________________________________。2H2S+SO2===3S↓+2H2O(4)若X是金属单质,向B、C的溶液中分别滴加AgNO3溶液和稀硝酸均产生白色沉淀,则B的化学式是________,保存C溶液常加少量的X,其目的是______________________________________________________________________。FeCl3 防止Fe2+被氧化成Fe3+解析:(1)C、N、S均为变价元素,当X为O2时均符合图示转化关系;Na与O2常温下生成Na2O,Na2O在加热条件下与O2反应生成Na2O2,也符合图示转化关系。Mg的化合价只有+2价,不符合图示转化关系。(2)A为NH3,C为NO2,则B为NO。(3)A为H2S,B为SO2,C为SO3。(4)X为变价金属单质Fe,B、C的溶液中均含有Cl-,B为FeCl3,C为FeCl2,A为Cl2。保存FeCl2溶液时需加铁粉防止Fe2+被氧化成Fe3+。18.(12分)某课外活动小组的同学在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了图中的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置略去)。试回答下列问题:(1)上述反应中生成二氧化硫的化学方程式为___________________________________________________。(2)乙同学认为还可能产生氢气的理由是________________________________________________________________________。 随Zn与浓硫酸反应的进行,浓硫酸逐渐变稀,Zn与稀硫酸反应可产生H2 (3) 丙同学在安装好装置后,必须首先进行的一步操作是______________________________________________________________________。检查装置的气密性(4) A中加入的试剂可能是__________,作用是____________;B中加入的试剂可能是________,作用是____________;E中加入的试剂可能是________,作用是______________________________________________________________________________。品红溶液 检验SO2 浓硫酸 吸收水蒸气碱石灰 防止空气中的水蒸气进入装置D中(5)可以证明气体X中含有氢气的实验现象:C中_______________________________________,D中_______________________________________。黑色粉末变成红色 白色粉末变成蓝色 如果去掉装置B,________(填“能”或“不能”)根据D中的现象判断气体X中有氢气,原因是_______________________________________________________________________________。不能 混合气体中含有水蒸气,会干扰对H2的检验解析:本题对Zn与浓硫酸反应的产物进行两种推测,而后设计实验进行验证。设计时既要验证有无SO2生成,又要验证有无H2生成。验证SO2可用品红溶液;验证H2可利用它的还原性,使其通过灼热的CuO,再通过无水硫酸铜检验是否有水生成来推断H2是否存在。同时应注意通入装置C中的气体必须干燥,也要防止空气中水蒸气进入装置D中,以免对H2的检验产生干扰。19.(12分)大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl-、SO32-、SO42-、NO3-等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成三份,进行如下实验:请回答下列问题:(1)根据实验判断该酸雨中肯定不存在的离子是____________,不能确定的离子有______________。SO32-、Ba2+ Na+、Cl-(2)写出第一份试液滴加淀粉KI溶液时发生反应的离子方程式:____________________________________________________。(3)第三份试液滴加NaOH溶液,加热,整个过程中发生了多个反应,写出其中两个反应的离子方程式:________________、____________________________、________________________、________________________________________________。6I-+2NO3-+8H+===2NO↑+3I2+4H2OH++OH-===H2O Al3++3OH-===Al(OH)3↓ Al(OH)3+OH-===AlO2-+2H2O(任写两个)(4)设计实验方案,检验该酸雨中是否存在Cl-:_____________________________________________________________________________________________________________________。(5) 该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是________________________________。 取少量试液滴加足量的Ba(NO3)2溶液,静置,取上层澄清液,加HNO3酸化的AgNO3溶液,若有白色沉淀生成,则证明存在Cl-作催化剂解析:(1)由第一份试液产生的现象知该酸雨中含有NO3-,因酸性条件下SO32-不能与NO3-共存,故试液中没有SO32-;由第二份试液产生的现象知该酸雨中含有SO42-,没有Ba2+;由第三份试液产生的现象知该酸雨中含有Al3+、NH4+。故该酸雨中肯定不存在的离子是SO32-、Ba2+,不能确定的离子有Na+、Cl-。(2)滴加淀粉KI溶液时,I-被氧化为I2,NO3-被还原为NO。(3)第三份试液中OH-分别与H+、Al3+、NH4+、Al(OH)3发生反应。(4)检验Cl-时,需要先用足量的Ba(NO3)2溶液将SO42-除去以排除干扰,然后用HNO3酸化的AgNO3溶液进行检验。(5)通入O2后,2NO+O2===2NO2,NO2+SO2===NO+SO3,喷水后SO3+H2O===H2SO4,故NO起催化作用。20.(12分)某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(图中铁架台等来持仪器均已略去):Ⅰ.实验装置如图甲所示。(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气。写出该反应的化学方程式:_____________________________________________________。(2)当集气瓶中充满红棕色气体时,木条复燃。有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是_______________________________________________________________________________________________________________________________。正确 Cu(NO3)2分解产生的O2的体积分数与空气中O2的体积分数相等,但空气不能使带火星的木条复燃,所以NO2能支持燃烧Ⅱ.实验装置如图乙所示。(3)写出浓硝酸受热分解的化学方程式:____________________________________。(4)实验开始后木条上的火星逐渐熄灭,有的同学提出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是_________________________________________________。不正确 可能是由于产生大量的水蒸气所致解析:Ⅰ.(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,所以该反应的化学方程式是2Cu(NO3)2=====△2CuO+4NO2↑+O2↑。(2) 2Cu(NO3)2=====2CuO+4NO2↑+O2↑,该反应中氧气占总气体体积的五分之一,与空气中氧气的体积分数基本相同,若NO2不支持燃烧,则木条不会复燃,根据实验现象知,二氧化氮支持燃烧,故结论正确。△Ⅱ.(3)浓硝酸具有强挥发性,且不稳定,在加热条件下能分解生成二氧化氮、氧气和水,反应方程式为4HNO3(浓)=====4NO2↑+O2↑+2H2O。(4)该反应的反应条件是加热,加热过程中有水蒸气生成,产生的大量水蒸气阻碍了NO2的助燃,导致NO2不能支持木条燃烧的假象,所以结论不正确。△本课结束This lesson is overTHANKS!









