



- 第七单元 应用广泛的酸碱盐(基础卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版) 试卷 4 次下载
- 第九单元 化学与社会发展(培优卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版) 试卷 2 次下载
- 第九单元 化学与社会发展(基础卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版) 试卷 1 次下载
- 第八单元 食品中的有机化合物(培优卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版) 试卷 2 次下载
- 第八单元 食品中的有机化合物(基础卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版) 试卷 1 次下载
第七单元 应用广泛的酸碱盐(培优卷)——2022-2023学年九年级下册化学单元卷(沪教版全国)(原卷版+解析版)
展开班级 姓名 学号 分数 第七单元 应用广泛的酸碱盐(B卷·能力提升练)
(时间:90分钟,满分:100分)
可能用到的相对原子质量:C-12 H-1 O 16 S-32 Zn-65
第Ⅰ卷 选择题(共40分)
一、选择题(本题共20小题,每小题2分,共40分。)
1.(2022年四川省成都市中考)部分水果及饮料的pH如下:
下列说法正确的是( )
A.西瓜汁显碱性 B.橘子汁中滴入酚酞,溶液变红
C.苏打水显酸性 D.胃酸过多的人应该少饮柠檬水
2.(2022年云南省中考)天宫课堂中,宇航员通过实验呈现了“奥运五环”,实验中使用了指示剂一一溴百里酚蓝,溴百里酚蓝溶液在不同环境中的显色情况如下:
溶液 | 中性溶液 | 碱性溶液 | 酸性溶液 |
颜色 | 绿色 | 蓝色 | 黄色 |
下列溶液能使绿色溴百里酚蓝溶液变为黄色的是( )
A.氯化钠溶液 B.醋酸溶液 C.氢氧化钾溶液 D.碳酸钠溶液
3.(2022年云南省中考)正确的实验操作是实验成功的保证。下列实验操作不正确的是( )
A.振荡试管 B.添加酒精
C.稀释浓硫酸 D.测定溶液的pH
4.(2022黑龙江龙东中考)城市绿化养护移栽的树木需要用到营养液。某品牌营养液的配制是在1000mL水中按照一定比例加入以下几种成分,①KNO3 ②Ca3(PO4)2 ③NH4H2PO4 ④K2SO4。几种成分中属于复合肥的是( )
A. ①② B. ①③ C. ②③ D. ①④
5.(2022江苏苏州中考)向溶液X中加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝。则溶液X中一定含有的微粒是( )
A. Cl- B. C. Ca2+ D.
6.(2022山东日照中考)向氢氧化钠溶液中加入一定量的稀硫酸,取少量反应后的混合液进行下列实验,能证明二者恰好完全中和的是( )
A.滴入几滴酚酞溶液,溶液变红色
B.滴入适量CuCl2溶液,无沉淀生成
C.滴入适量BaCl2溶液和稀硝酸,观察到有白色沉淀
D.测得混合液中Na+与SO42﹣的个数比为2:1
7.(2022年四川省自贡市中考)分类是化学学习和研究的重要方法之一。下列物质分类错误的是( )
A.氧化物:SO2、CuO、KMnO4
B.酸:HCl、H2SO4、HNO3
C.碱:NaOH、Ca(OH)2、NH3•H2O
D.盐:NH4Cl、AgNO3、BaSO4
8.(2022年江西省中考)化学学科核心素养展现了化学课程对学生发展的重要价值,下列示例说法错误的是( )
A.化学观念:酸溶液中都含有H+,所以具有相似的化学性质
B.科学思维:碱能使无色酚酞溶液变红,能使无色酚酞溶液变红的一定是碱
C.科学探究与实践:将火柴梗迅速平放入蜡烛的火焰中约1s后取出,探究火焰哪层温度最高
D.科学态度与责任:可燃性气体遇明火易发生爆炸,加油站要严禁烟火
9.(2022山东东营中考)东营某化工厂产生的污水pH=2,主要污染物是硫酸。现要将污水调节至接近中性,达标后再排放,下列说法不正确的是( )
A.检测:用pH试纸或pH计检测污水的酸碱度
B.原理:处理酸性污水的实质是消耗污水中的氢离子
C.验证:取水样,加入少量氯化钡溶液后出现白色沉淀,证明处理未达标
D.应用:可与造纸厂排放的碱性污水混合,达标后再排放
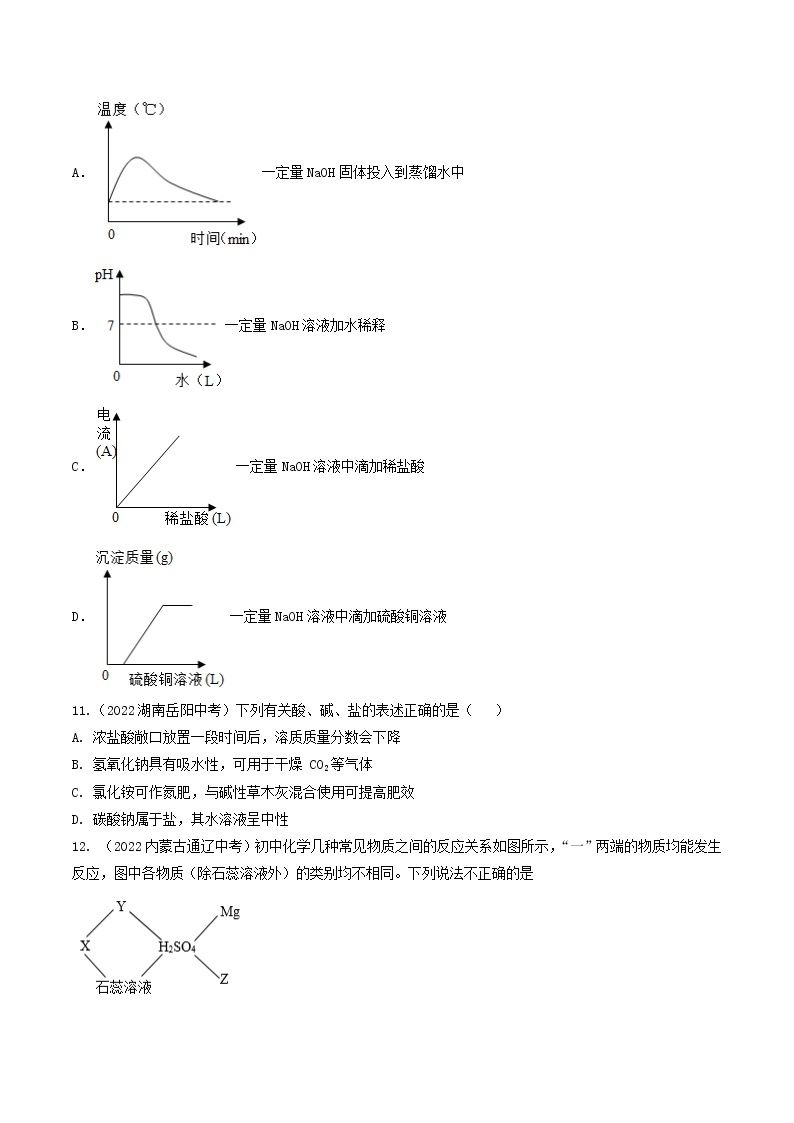
10.(2022年四川省自贡市中考)下列图像与对应的实验操作相符合的是( )
A.一定量NaOH固体投入到蒸馏水中
B.一定量NaOH溶液加水稀释
C.一定量NaOH溶液中滴加稀盐酸
D.一定量NaOH溶液中滴加硫酸铜溶液
11.(2022湖南岳阳中考)下列有关酸、碱、盐的表述正确的是( )
A. 浓盐酸敞口放置一段时间后,溶质质量分数会下降
B. 氢氧化钠具有吸水性,可用于干燥 CO2等气体
C. 氯化铵可作氮肥,与碱性草木灰混合使用可提高肥效
D. 碳酸钠属于盐,其水溶液呈中性
12. (2022内蒙古通辽中考)初中化学几种常见物质之间的反应关系如图所示,“一”两端的物质均能发生反应,图中各物质(除石蕊溶液外)的类别均不相同。下列说法不正确的是
A. X可能是碳酸钠 B. Z与硫酸反应,可能得到黄色溶液
C. X和Y可能是NaOH和Ba(NO3)2 D. Mg与H2SO4发生置换反应
13.(2022山东济宁中考)下列物质间转化仅通过一步化学反应就能实现的是( )
A.CuCuSO4
B.SiO2Na2SiO3
C.KClKNO3
D.BaSO4MgSO4
14.(2022湖南郴州中考)有关酸碱盐的性质和用途,下列说法错误的是( )
A. 氯化钠解离出的阳离子是氯离子,氯离子是胃液中的主要成分,具有促生盐酸、帮助消化和增进食欲的作用
B. 硫酸厂的污水中含有硫酸等物质,可以用熟石灰进行中和处理
C. 盐酸与镁反应中,除生成气体外还会放出热量
D. 碳酸氢钠在医疗上是治疗胃酸过多症的一种药剂
15.(2022湖南常德中考)根据下列证据,运用化学知识进行推理,错误的是( )
| 证据 | 推理 |
A | 把铁丝插入硫酸铜溶液后,在铁丝表面有红色固体出现 | 金属铁比铜活泼 |
B | 居室放置茉莉花,进屋就能闻到扑鼻香气 | 分子在不断运动 |
C | 用pH试纸测得某品牌洗涤剂的pH=12 | 该洗涤剂含NaOH |
D | 打开盛有浓盐酸试剂瓶的瓶塞,瓶口有白雾出现 | 浓盐酸易挥发 |
16.(2022山东临沂中考)下列各组溶液混合后,能发生化学反应且溶液总质量不变的是
A. 氢氧化钠溶液和稀硫酸 B. 硫酸铜溶液和氯化钡溶液
C. 氢氧化钾溶液和氯化钠溶液 D. 碳酸钠溶液和稀盐酸
17.(2022山东威海中考)某工厂生产高锰酸钾(KMnO4)的流程如图所示,下列说法不正确的是( )
A.混合加热室中发生物理变化
B.氧化室中一定有O2参与反应
C.电解室中K2MnO4发生分解反应
D.该过程中可循环利用的物质是KOH
18.(2022年四川省成都市中考)实验小组用图1装置探究稀氢氧化钠溶液与稀盐酸能否反应,测得数据如图2。下列说法正确的是( )
A.烧杯中只能盛放稀氢氧化钠溶液
B.图2不能证明反应是放热反应
C.60s时溶液中溶质只有氯化钠
D.实验证明氢氧化钠与盐酸能反应
19.(2022年江苏省连云港市中考)为探究一瓶久置的NaOH溶液样品是否变质,进行如下实验:
实验一:取少量样品于试管中,滴加1~2滴酚酞溶液,溶液显红色。
实验二:取少量样品于试管中,加入适量稀硫酸,有气泡放出。
实验三:取少量样品于试管中,加入足量的BaCl2溶液,有白色沉淀生成。过滤,向滤液中滴加1~2滴酚酞溶液,溶液显红色。
下列结论正确的是( )
A.实验一说明NaOH溶液没有变质 B.实验二说明NaOH溶液全部变质
C.实验三中生成的沉淀为Ba(OH)2 D.实验三说明NaOH溶液部分变质
20.(2022广西梧州中考)图中甲、乙、丙是三种常见的化合物,相连物质之间均能发生化学反应。下列符合图示要求的是
A. 若甲为CuO,乙、丙可以为H2SO4、H2
B. 若甲为HCl. 乙、丙可以为KOH、FeSO4
C. 若甲为NH4NO3,乙、 丙可以为HCl、Ca(OH)2
D. 若甲为Ba(OH)2, 乙、丙可以为CO2、Na2SO4
第Ⅱ卷 非选择题(共60分)
二、填空简答题(本题共10小题,每空1分,共60分)
21. (3分)(2022北京中考)如下图所示,向井穴板的孔穴1~3中滴加稀盐酸,4~6中滴加无色酚酞溶液。
(1)1中所得溶液的颜色为_______________。
(2)从2、3中任选一个,写出发生反应的化学方程式:_______________。
(3)4、5、6中无明显现象的是_______________(填序号)。
22.(3分)(2022年湖南省衡阳市中考)构建思维导图是一种重要的学习方法。请根据酸和碱的化学性质思维导图,回答下列问题。(“一”表示相连的两类物质之间可以发生化学反应)
(1)请写出图中甲表示的物质类别_______。
(2)酸与碱作用生成盐和水的反应,叫做中和反应。请写出一个中和反应的化学方程式____。
(3)酸和碱能与指示剂反应,而使指示剂显示不同的颜色。如NaOH溶液能使无色酚酞变成___色。
23.(6分)学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)若用Cu(OH)2实现②,会得到 色溶液,该溶液中可能有的溶质是
(填名称)。为验证该物质是否存在,你认为可采用以下哪些物质可用来进行实验验证 。
A碳酸钠溶液B金属铜C酚酞试液D氯化钡溶液E氧化铜粉末
(2)若想实现③,得到浅绿色溶液,可选用的单质是 (填化学式)。
(3)若选用BaCl2溶液实现⑤,这个反应 (填“属于或“不属于”)酸的通性。
(4)在生活中,稀硫酸可以用来除铁锈,反应原理是 (用化学方程式表示)。
24.(6分)(2022年新疆中考)归纳总结是学习化学的重要方法,小明同学用思维导图的形式总结了NaOH的四条化学性质如图甲(即NaOH与四类物质能够发生化学反应)。请回答:
(1)反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是_______。
(2)写出一个符合反应②的化学方程式_______;小红同学将某稀酸溶液逐滴滴入一定量的稀氢氧化钠溶液中,用温度传感器对反应过程中溶液的温度进行实时测定,得到的曲线如图乙,根据图像可以得出该反应是_______(填“吸热”或“放热”)反应。
(3)反应③可以选用的盐是_______,你选择的依据是_______。
A.NaNO3 B.CuSO4 C.NH4NO3 D.KNO3
(4)二氧化碳和一氧化碳都是非金属氧化物,二氧化碳能和氢氧化钠反应,一氧化碳却不能,造成此性质差异的微观原因是_______。
25.(6分)(2022年陕西省中考B卷)学习小组同学用下图所示实验探究完碱的化学性质后,将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。
【反思交流】
(1)小组同学做甲图所示实验时,当溶液恰好由红色变为无色,即停止了滴加稀盐酸,写出发生反应的化学方程式:___________。做乙图所示实验时,看到的现象是___________。
(2)废液呈红色,说明废液显___________性。废液变浑浊,是因为倾倒前丙中的溶液含有___________(填化学式)。
【拓展问题】
使废液变成红色的物质是什么?
【做出猜想】
猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Ca(OH)2
猜想四:NaOH和Na2CO3
你认为以上猜想中,不合理的是猜想___________。
【查阅资料】
CaCl2溶液呈中性。
【验证猜想】
静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成。静置后,发现试管中的上层清液仍为红色,由此证明了猜想___________成立。
26.(11分)(2022年江苏省扬州市中考)为认识酸和碱的性质,某化学学习小组进行了如下实验。
(1)20℃时,配制80g溶质质量分数为10%的NaOH溶液。
①用图中仪器完成实验,还缺少的玻璃仪器是____(填名称),玻璃棒在配制实验中的作用是___。
②配制该溶液需要_______g水。用量筒量取水时,俯视读数会导致所配溶液的溶质质量分数___10%。(填“大于”或“小于”)
(2)向1~5号小试管中分别滴加少量稀盐酸。
①_______中溶液变为红色(填“试管1”或“试管2”)。
②试管3中产生气泡,试管4中无明显现象,由此推断金属活动性Cu比Zn_______(填“强”或“弱”)。
③试管5中生成一种盐和两种氧化物,该反应的化学方程式为_______。
(3)借助传感器对稀NaOH溶液与稀盐酸的中和反应进行研究,实验装置如图,三颈烧瓶中盛放溶液X,用恒压漏斗匀速滴加另一种溶液。
①甲同学用pH传感器测得三颈烧瓶内溶液pH的变化如题图,判断溶液X是_____,实验进行到60s时溶液中的溶质为_____(填化学式)。
②乙同学用温度传感器测得三颈烧瓶内温度变化如图(实验过程中热量散失忽略不计),据此可得出反应过程中_____能量的结论(填“吸收”或“释放”)。
③丙同学提出,通过监测三颈烧瓶内压强变化,也可以推导出乙同学的实验结论,其理由是____。
27.(5分)(2022年四川省遂宁市中考)同学们为提升化学实验操作技能,在实验室练习如下实验:
实验完毕后,小明误将A试管中的物质倒入B试管中,充分振荡后,观察到混合后溶液为无色。小明对该无色溶液的成分产生兴趣并展开探究(温馨提示:本题中番号①~⑤为答题卡上的序号)。
【提出问题】混合后无色溶液的溶质除酚酞外还有什么?
【查阅资料】NaCl溶液、CaCl2溶液显中性。
【猜想与假设】猜想-:NaCl、CaCl2;
猜想二:NaCl、CaCl2、HCl;
猜想三:NaCl、CaCl2、Ca(OH)2;
经分析猜想三错误,其理由是_________。
【设计并进行实验】为了验证其余猜想,小明进行了如下实验:
实验操作 | 实验现象 | 解释与结论 |
取少量混合后的无色溶液于试管中,加入锌粒 | ___________________ | 解释实验现象:__________(用化学方程式表示) 得出实验结论:猜想二正确 |
【反思与拓展】
Ⅰ.有同学提议将上表操作中的锌粒换成另一种药品或用品:________(除金属外),也可得出猜想二正确的实验结论。
Ⅱ.小明误倒后,如果观察到试管底部有白色沉淀,上层清液为红色,则上层清液中一定有的阴离子是_______(填写离子符号)。
28.(9分)(2022年四川省成都市中考)劳动实践课上同学们用草木灰给农作物施肥。课后同学查阅资料,得知草木灰是一种重要的农家肥,碳酸钾含量高。
【提出问题】
如何测定草木灰中碳酸钾的含量?
【查阅资料】
1 常见草木灰钾含量(以碳酸钾表示)如下表:
草木灰种类 | 小灌木灰 | 稻草灰 | 小麦杆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
K2CO3(%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
2 提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(1)表格中钾含量最高的草木灰是____________,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。
(2)图1实验中,用60℃的温水而不用冷水浸洗的原因是________________________。
(3)根据图2,搅拌器转速控制在每分钟____________转,浸取时间为____________分钟,比较适宜。
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
(4)实验中需缓慢滴入稀硫酸,原因是________________________。
(5)装置B的作用是________________________。
【数据与解释】
(6)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为____________%,与表格中数据相比明显偏低,原因可能是____________(填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
【反思与评价】
(7)我国秸秆产量巨大,可作为生物质发电的原料,还可利用其燃烧发电产生的草木灰提取碳酸钾,其优点有______________(写一条)。
29.(8分)(2022年山东省泰安市中考)在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老帅引导下开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
(1)测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将_______(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化
乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是_______(填“放热”或“吸热”)反应。图2中B点表示的含义是_______。
(3)借助于酸碱指示剂
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为_______。
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】
猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH
【进行实验】为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量反应后的溶液于试管中,加入Fe2O3粉末 | _______ | 溶液中有H2SO4猜想二正确 |
方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液 | ②产生白色沉淀 | 溶液中有H2SO4,猜想二正确 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(4)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是_______。
(5)同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号_______。
A.Mg B.CuO C.KCl D.Na2CO3
(6)分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还要考虑_______。
30.(3分)(2022年云南省中考)学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40g。计算。
(1)消耗的NaOH溶液中溶质的质量为___________g:
(2)该硫酸溶液的溶质质量分数_________。(温馨提示:)(2分)









