






人教版化学九年级下册第八单元复习课件
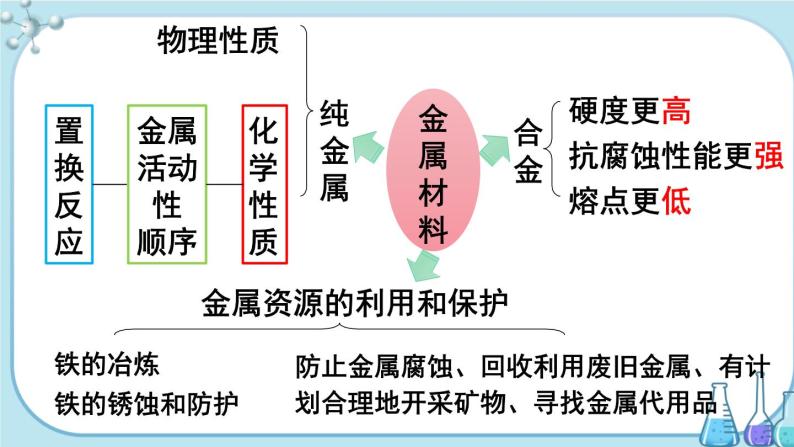
展开第八单元 金属和金属材料小结与复习人教版化学九年级下册纯金属物理性质化学性质金属活动性顺序合金硬度更高抗腐蚀性能更强熔点更低金属资源的利用和保护铁的冶炼防止金属腐蚀、回收利用废旧金属、有计划合理地开采矿物、寻找金属代用品 金属材料置换反应铁的锈蚀和防护考点一 金属材料及其用途1.金属材料包括:__________和________。2.合金(1)定义:在金属中加热熔合某些金属或非金属形成的具有____________的物质。(2)性能:合金的____________比组成它们的纯金属高,_____低,抗腐蚀性能________。纯金属 合金 金属特征 强度和硬度 熔点 强合金在物质分类中属于混合物,且至少含一种金属,合金的用途比纯金属广泛。注意(3)常见的两种铁的合金________:含碳量2%~4.3%的铁合金,硬度大、韧性小。________:含碳量0.03%~2%的铁合金,较硬,韧性佳。其中__________中含有铬、镍,不易生锈,抗腐蚀性能好,常用于制造医疗器械。生铁 钢 不锈钢金属的性质在很大程度上决定了金属的用途,但这不是唯一决定的因素,还需考虑价格、资源、是否美观、使用是否便利,以及废料是否易于回收和对环境的影响等多种因素。3.金属的用途 共性 个性 常温下一般是固态 汞-液态大多呈银白色金属光泽铜-紫红、金-黄、铁粉-黑一般密度较大,熔点较高一般具有良好的导电性、导热性、延展性 考点二 金属的物理性质【练习1】(湖南湘西州中考)下列有关“金属之最”的描述中,属于金属物理性质的是( )A.钙是人体中含量最多的金属元素B.铁是世界年产量最高的金属C.铝是地壳中含量最多的金属 D.银是导电导热性最好的金属【练习2】(辽宁本溪中考)关于金属及合金的说法错误的是( )A.合金中至少含有两种金属元素B.生铁和钢是常见的铁合金C.黄铜的硬度比纯铜的硬度大 D.焊锡的熔点比纯锡的熔点低AD1.金属活动性顺序K Ca Na Fe Sn Pb (H) Pt Au Mg Al Zn Cu Hg Ag金属活动性由强到弱(1)在金属活动性顺序里,金属的位置越靠前,它的活动性就越强,越容易与氧气发生反应;(2)在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢;(3)在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。考点三 金属的化学性质氢前可换氢 前金换后金许多金属都能与氧气反应,但反应的难易和剧烈程度不同。2.金属与氧气反应4Al + 3O2 === 2Al2O33.金属与盐酸、稀硫酸的反应(氢前可换氢)Mg + H2SO4 ===MgSO4 + H2↑Zn + H2SO4 === ZnSO4 + H2↑Fe + H2SO4 === FeSO4 + H2↑Mg + 2HCl ====MgCl2 + H2↑Zn + 2HCl === ZnCl2 + H2↑Fe + 2HCl === FeCl2 + H2↑ 一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应。置换反应:表达式:A+BC==B+AC特征:一换一4.金属与其他金属化合物溶液的反应(前金换后金)Cu+2AgNO3===2Ag+Cu(NO3)22Al+3CuSO4===3Cu+Al2(SO4)3(1)在初中阶段,金属活动性顺序的应用 不涉及K、Ca、Na(2)Fe在这两类置换反应中,都变成亚铁离子(Fe2+)Fe + CuSO4 === FeSO4 + Cu注意【例1】(广东中考)利用盐酸和硝酸银探究铁、 铜、银的金属活动性顺序,下列实验可以不需要进行的是( )A.铁+稀盐酸 B.铜+稀盐酸C.银+稀盐酸 D.铜+硝酸银溶液解题思路:由金属活动性顺序的应用,验证试验的设计思路为:根据三种金属与盐酸反应的情况,可验证铁的活动性比铜、银强;然后利用铜和硝酸银的置换结果,验证铜的活动性比银强。对比四个实验,不做实验C也不影响三种金属活动性的判断。故选CC 【练习3】(新疆中考)如图是探究铁和铜金属活动性的实验,关于此实验说法错误的是( )A.铁丝需要砂纸打磨B.溶液由蓝色变为无色C.金属活动性强弱:Fe>CuD.化学反应方程式为Fe+CuSO4 =Cu+FeSO4 B【例2】(湖北宜昌中考)取一定量的Mg放入Cu(NO3)2和 AgNO3 的混合溶液中,充分反应后过滤,得到固体和滤液。下列说法错误的是( )A.固体中只有Ag时,滤液一定呈蓝色B.固体中有Cu和Ag时,滤液一定呈无色C.固体中一定有Ag,滤液中可能有AgNO3D.固体中可能有Cu,滤液中一定有Mg( NO3) 2解题思路:镁比铜活泼,铜比银活泼,将一定量的镁粉加入AgNO3和Cu(NO3)2的混合溶液中,镁先和AgNO3反应,后和Cu(NO3)2反应。固体中一定有Ag,可能有Cu;滤液中一定有Mg(NO3)2,可能有Cu(NO3)2或Cu(NO3)2、AgNO3。对于选项B,固体中有Cu和Ag时,可能是镁置换了部分Cu(NO3)2,滤液可能呈蓝色,故B错误B【例3】某不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是( ) A.Zn B.Cu C.Mg D.Ag解题思路:本题主要考查对 “有关化学反应方程式计算” 等考点的理解和运用。5.6g铁与足量稀硫酸充分反应生成氢气0.2g,因此铁中混有的金属不可能是铜或银;5.6g锌、镁与足量稀硫酸充分反应生成氢气分别是0.17g、0.47g。由此可知,不纯的铁中,如果含有锌,则生成的氢气小于0.2g,如果含有镁,则生成的氢气大于0.2g。C考点四 铁的冶炼1.一氧化碳还原氧化铁(1)实验装置(如图)(2)实验步骤一氧化碳酒精喷灯早出早退迟到晚归(3)实验现象:红棕色粉末逐渐变为______色,澄清石灰水变________,尾气燃烧产生_______火焰。黑 浑浊 蓝色防爆炸防氧化防倒吸点燃或收集【注意】①先通CO(早出) ②实验完毕后要先撤掉酒精喷灯,继续通入CO(晚归)③CO有毒,要进行尾气处理(1)原料:铁矿石(2)原理: 在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来。(3)主要设备:炼铁高炉2.工业炼铁石灰石焦炭空气Fe2O3 + 3CO ==== 2Fe + 3CO2 高温焦炭:①燃烧提供热量②产生一氧化碳石灰石:将铁矿石中的 SiO2转变为炉渣C + O2=== CO2C + CO2 === 2CO 点燃高温考点五 金属资源的保护1.金属的锈蚀与保护(1)铝在空气中耐腐蚀的原因:_______________________________________________________________________________。(2)铁生锈的条件:铁与空气中的________和________反应生成铁锈(主要成分是Fe2O3)。铁锈疏松易吸水,若不及时除去,会加快铁制品的锈蚀速度。铝在空气中与氧气反应,其表面会生成一层致密的氧化铝薄膜,阻止内部的铝进一步氧化氧气 水蒸气 问题:如何防止铁生锈呢?(3)防锈措施:①________________________,如菜刀用完后擦干挂起来。②__________________________,如:刷漆、涂油、电镀等。③还可以通过添加其他金属或非金属制成合金,如不锈钢。2.保护金属的有效途径 (1)______________________。 (2)______________________。 (3)有计划合理地开采矿物。 (4)寻找金属的代用品。保持金属表面洁净、干燥 金属表面涂上一层保护膜 防止金属腐蚀 回收利用废旧金属 考点六 涉及杂质问题的计算1.化学方程式所表示的物质间的质量关系是__________间的关系。2.当参加反应的物质或生成的物质含有杂质时,要换算成纯物质的质量,再进行计算。3.各物质间的关系______________=含杂质物质的质量×纯度(或含量)纯净物 纯物质的质量 【练习4】(四川巴中中考)用“W”形管进行微型实验,如下图所示。下列说法错误的是( )A.a处红棕色粉末变为黑色B.a处实验结束时先停止通入CO,后停止加热C.b处澄清石灰水变浑浊证明有二氧化碳生成D.可利用点燃的方法进行尾气处理 【练习5】(湖南株洲中考)用1000 t含有氧化铁80%的赤铁矿石,理论上可以炼出含铁97%的生铁的质量约是______。B577.3t易错点归纳1.铁与盐酸、稀硫酸以及某些金属化合物溶液发生置换反应时,生成的是亚铁离子(Fe2+),而不是铁离子(Fe3+)。2.金属与其他金属化合物溶液发生反应:①在金属活动性顺序里,排在前面的金属才能置换出排在后面的金属;②金属化合物必须能溶于水;③金属不能是特别活泼的钾、钙、钠;④描述实验现象时,既要描述金属颜色的变化,还要描述溶液颜色的变化。化学方程式网络构建1.有关铁的反应A的化学式__________ Fe2O3请写出图中所涉及的化学方程式①__________________________②__________________________ __________________________③__________________________④____________________________2.有关锌、铜的反应请写出图中所涉及的化学方程式①__________________________②__________________________ __________________________③④⑤____________________________________________________ __________________,____________________________________________⑥Zn + H2SO4 === ZnSO4 + H2↑Zn + 2HCl === ZnCl2 + H2↑Cu+2AgNO3===2Ag+Cu(NO3)2Zn + CuSO4 ===ZnSO4 + CuCuO + H2 === Cu + H2O2CuO + C === 2Cu + CO2 高温 △CuO + CO === Cu + CO △谢谢观看









