



初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除教课内容课件ppt
展开分离:是通过适当的方法,把混合物中的几种物质分开,每一组分都要保留下来,并恢复到原状态,得到比较纯的物质。
提纯:指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去。
区别:分离得到的是多种纯净物;提纯只得到一种纯净物。
分离和提纯有什么不同?
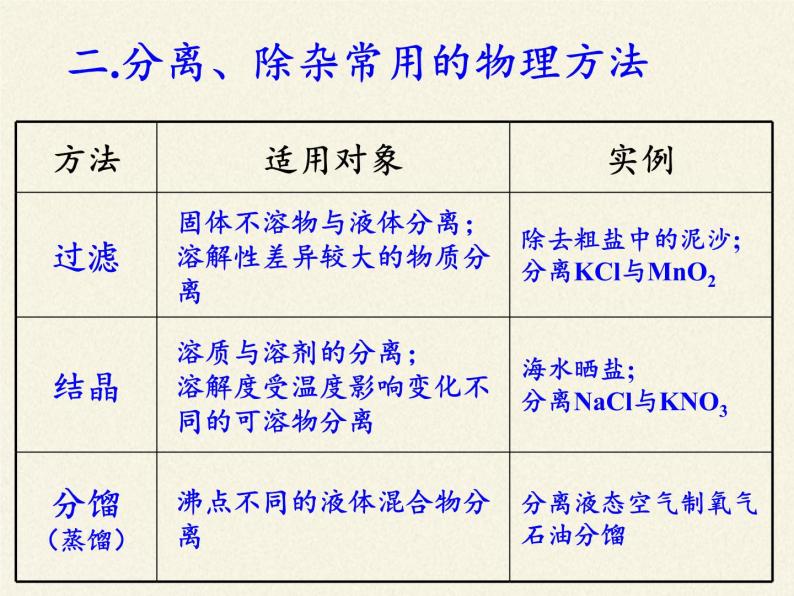
二.分离、除杂常用的物理方法
氯化钾和氯化镁均为白色粉末,如果氯化钾粉末混有少量的氯化镁,可以采用什么方法得到纯净的氯化钾。
思路:除去氯化镁——把Mg2+转换为沉淀——
不增:即最终不能引入新的杂质;
不减:除杂结果不应使所需物质减少;
易分:加入试剂后,使杂质转化为沉淀,气体等与所需物质易于分离。
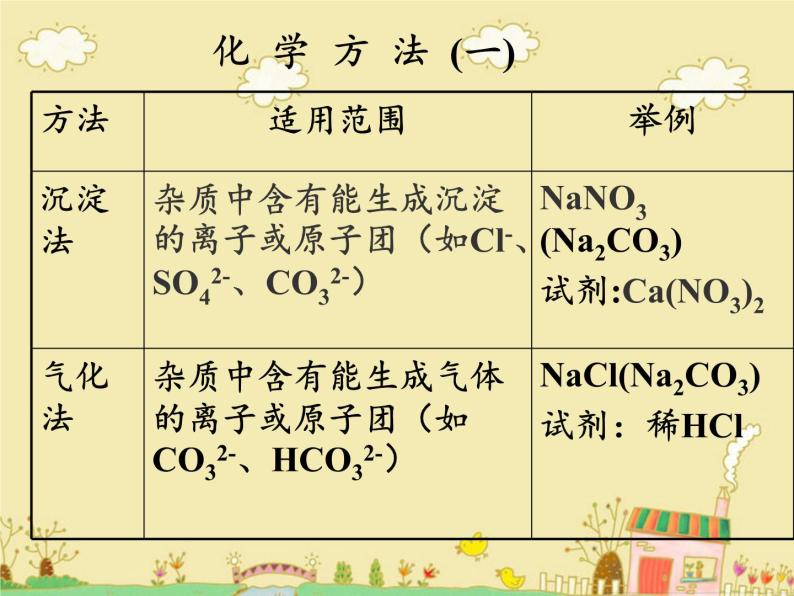
化 学 方 法 (一)
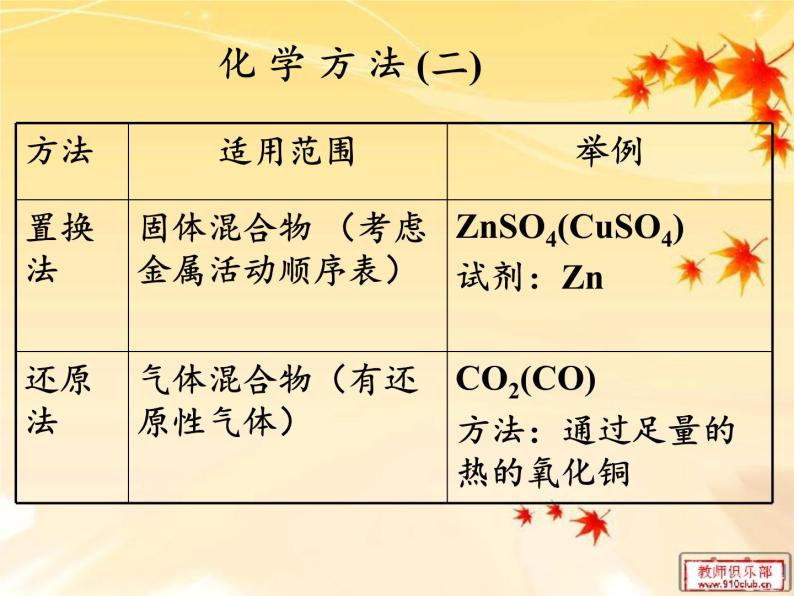
化 学 方 法 (二)
(1)确定杂质离子;(2)选择除杂试剂的离子, 使杂质离子转化为水、气体或沉淀;(3)根据主体成分, 确定除杂试剂的另一离子。
除去下列物质中的杂质的方法(括号内为杂质)⑴NaCl(I2)___ _________________⑵ CuO(C)______ ___________________⑶ Cu(CuO)_ ________________________
通过H2并加热或加过量的稀盐酸过滤
1、 NaCl(NaOH)
Cu2+ Mg2+ Fe3+
2、 NaCl(CuSO4)
3、 FeCl3(KCl)
2、 Fe(OH)3 + 3HCl = FeCl3 + 3H2O
NaCl (Na2CO3) ________________
加入适量的盐酸适量的氯化钙溶液适量的氯化钡溶液
另外,在遇到一些实际问题时,为了充分除去杂质,往往加入过量的试剂,这时后续操作一定要把加入的过量试剂也除去。
1、下列化合物可以用溶解、过滤、蒸发操作来分离的是( )A.CaCO3 CaO B.KCl MnO2 C.KNO3 K2SO4 D.BaSO4 CaCO3
2、氯化钠溶液中混有少量的硫酸钠杂质,除杂质所用的试剂是( )A、Ba(OH)2 B、BaCl2C、Ba(NO3)2 D、BaCO3
3、下列除杂的实验过程都正确的是(括号内为杂质)( )A、MnO2(KCl) 加水溶解、过滤、洗涤、干燥B、NaOH(Na2CO3) 加适量稀HCl,干燥C、CuSO4(FeSO4) 加适量Cu,过滤、洗涤、蒸发D、KCl(K2CO3)加适量Ca(OH)2溶液,过滤、蒸发
4.下列各组物质中,都含有少量的杂质,分别用什么试剂可以将括号内的杂质去(只要求写所加物质的名称或方法及化学方程式)?(1)CO(C02):(2)NaOH[Ca(OH)2].(3)KN03(KCl).(4)NaCl(Na2C03).(5)FeS04(CuS04)
CO2 +2NaOH=Na2CO3+H2O
Na2CO3+ Ca(OH)2=CaCO3↓+2NaOH
AgNO3+ KCl=AgCl↓+KNO3
CaCl2+ Na2C03= CaCO3↓+2NaCl
Fe+CuSO4=FeSO4+Cu.
1. 选择试剂或方法除去下列固体或溶液中所含杂质(括号内为杂质),并写出反应所涉及的化学方程式及所属基本反应类型 ① ZnCl2 溶液(HCl) ; ② NaCl 溶液(CuCl2) ; ③ CuO(Cu) ; ④ Cu(CuO) ; ⑤ MgO [ Mg(OH)2 ] 。
物 理 方 法
固-液分离(固体不溶)
固-固分离(物质和杂质均可溶且溶解度随温度的变化趋势不同)
固-液分离(固体能溶,且溶解度受温度影响不大)
CaCl2(CaCO3) 加水溶解→过滤
NaCl(H2O) 蒸发
KNO3(NaCl) 高温配制KNO3饱和溶液→降温结晶
注意点:“一贴二低三靠”
适用于分离难溶固体与液体组成的混合物(例:提纯粗盐)
(1)蒸发结晶:适用于将可溶性固体从液体中进行分离(例:从食盐水中提纯氯化钠)。为了提高分离效果,还可以进行重结晶。
现有混有少量氯化钾的硝酸钾粉末,请参照图中的溶解度曲线,设计实验方案提纯硝酸钾。
(2)降温结晶:适用于分离溶解度随温度变化有明显差异的固体混合物(例:提纯氯化钾和硝酸钾晶体)。
KCl、KNO3混合物
KNO3(S)、KCl+ KNO3溶液
设计方案:⑴取一定量的水加热到90℃左右,加入固体混合物,搅拌,使固体完全溶解⑵将所得溶液静置、冷却,降低温度到30℃左右,析出硝酸钾晶体⑶过滤得到晶体
练习二、除去氯化钠溶液中混有的少量氯化钙,应加入的试剂是( )
练习三、除去氯化钠溶液中混有的少量碳酸钠,应加入的试剂是( )
练习四 硫酸锌固体中混有少量的CuSO4杂质,应加入的试剂是( )
练习五 CO2中含有CO气体,应选用的试剂( )
练习一:实验室中的硝酸钾固体混有少量氯化钾固体,下列方法可得到纯净的硝酸钾的是( )A、蒸发结晶法 B、过滤C、降温结晶法 D、加入硝酸钠
初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除集体备课课件ppt: 这是一份初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除集体备课课件ppt,共7页。
初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除一等奖ppt课件: 这是一份初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除一等奖ppt课件
初中人教版实验活动8 粗盐中难溶性杂质的去除课文配套ppt课件: 这是一份初中人教版实验活动8 粗盐中难溶性杂质的去除课文配套ppt课件,共11页。PPT课件主要包含了P87-88,一选择实验用品,二实验步骤,三讨论与交流,物质的除杂,本课至此结束,合作愉快等内容,欢迎下载使用。













