

2021-2022学年河北省张家口市宣化第一中学高一下学期4月月考化学试卷含解析
展开2021-2022学年下学期宣化一中高一月考
化学试卷(4月份)
1. “嫦娥五号,成功从月球“挖土,实现了中国首次月球无人采样返回。月壤中富含,下列有关说法正确的是
A. 原子核外有个电子 B. 原子核内有个中子
C. 与互为同位素 D. 电子数为
2. 常温下,将下列金属分别放入水中,反应最剧烈的是
A. B. C. D.
3. 化学与生活密切相关。下列工业生产过程不涉及氧化还原反应的是
A. 用黄铁矿为原料生产硫酸
B. 高温下与反应制高纯硅
C. 用氨为原料生产硝酸
D. 实验室制取氨气
4. 我国科学家制得的超分子纳米管的微观结构如图。下列叙述正确的是
A. 与干冰的物理性质相似
B. 耐腐蚀,不与任何酸反应
C. 用生产光导纤维
D. 超分子纳米管具有导电性
5. 化学在生活中有着广泛的应用。下列对应关系错误的是
选项
化学性质
实际应用
具有漂白性
水溶液吸收蒸气
具有很大的硬度
用作砂纸或砂轮的磨料
具有碱性
修复被酸雨浸湿的土壤
具有还原性
将烟道气中的转化为
A. B. C. D.
6. 如果为第Ⅱ族中某元素的原子序数,则原子序数为的元素位于周期表的
A. 第Ⅲ族或第Ⅲ族 B. 第Ⅳ族
C. 第 族 D. 第族
7. 下列有关化学键的叙述,正确的是
A. 单质分子中一定存在非极性键
B. 共价化合物分子中一定存在极性键
C. 含有共价键的化合物一定是共价化合物
D. 含有离子键的化合物可能是共价化合物
8. 下列离子方程式书写正确的是
A. 与稀硝酸反应:
B. 向碳酸氢钠溶液中滴加少量澄清石灰水:
C. 与溶液反应:
D. 与氨水反应:
9. 下列说法错误的是
A. 生产玻璃和水泥的原料中均有石灰石
B. 陶瓷由黏土高温烧制而成,主要成分是硅酸盐
C. 耐高温的石英玻璃属于硅酸盐材料
D. 在雷雨天,空气中和可反应生成
10. 常温下能盛放在铁制容器中的物质是
A. 浓盐酸 B. 浓硝酸 C. 硫酸铜溶液 D. 稀硫酸
11. 下列关于、、的说法错误的是
A. 气态氢化物的稳定性:
B. 最外层电子数:
C. 原子半径:
D. 电子层数:
12. 下列关于碱金属元素的描述正确的是
A. 在氧化物中均呈价
B. 单质都可以保存在煤油里
C. 单质均可与氧气反应生成多种氧化物
D. 单质与水反应,均漂浮在水面上
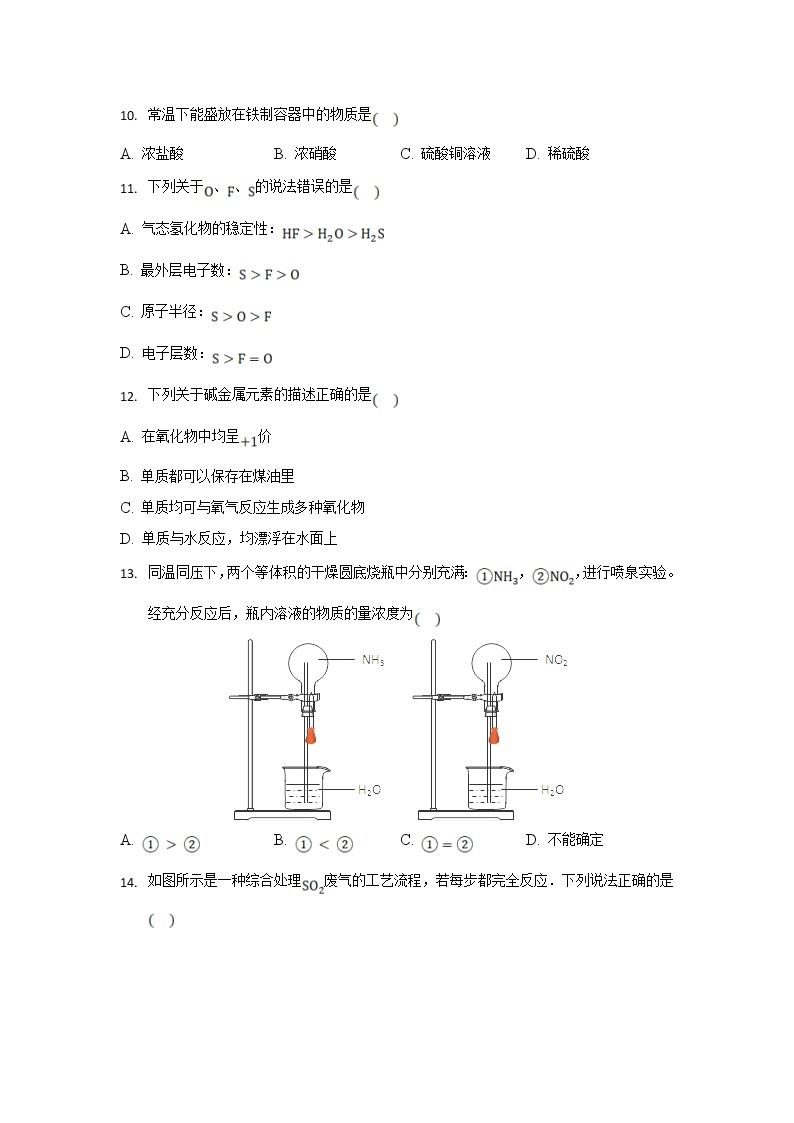
13. 同温同压下,两个等体积的干燥圆底烧瓶中分别充满:,,进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度为
A. B. C. D. 不能确定
14. 如图所示是一种综合处理废气的工艺流程,若每步都完全反应.下列说法正确的是
A. 溶液中发生的反应为
B. 可用酸性高锰酸钾溶液检验溶液中是否含有
C. 由以上流程可推知氧化性:
D. 此工艺的优点之一是物质能循环利用
15. 某课外活动小组在实验室用如图所示装置快速制取氨气并验证氨气的某些性质,同时收集少量纯净的氮气,回答下列问题:
写出用熟石灰和氯化铵反应制氨气的化学方程式:______。
本实验进行一段时间后,观察到加热的硬质玻璃试管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃试管内发生反应的化学方程式:______,这个反应说明氨气具有 ______填标号。
碱性
还原性
氧化性
不稳定性
洗气瓶中盛浓硫酸的作用是 ______。
在最后的出气导管口收集干燥、纯净的氮气,收集方法是 ______填标号。
排空气法
排水法
用气囊收集
装置的作用是 ______。
16. A、、、、、是原子序数依次增大的短周期主族元素,其相关信息如表所示:
元素
相关信息
的原子半径在短周期中最小
A、形成的最简单化合物是一种气体,其水溶液呈碱性
的最外层电子数是内层电子数的倍
常温下,的单质在浓硫酸中会钝化
和处于同一主族
回答下列问题:
的原子结构示意图为 ______,和溴分别与氢形成的化合物,更稳定的是 ______填化学式。
上述六种元素的原子中,半径最大的是 ______填元素符号。
的最高价氧化物对应的水化物的化学式为 ______。
的氢化物与的最高价氧化物对应的水化物反应的离子方程式为 ______。
17. 为验证同主族元素性质的递变规律。某小组用如图所示的装置进行实验夹持仪器已略去装置气密性已检验。
实验过程:
I.打开弹簧夹,打开活塞,滴加浓盐酸。
Ⅱ当装置和装置中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ当装置中溶液由黄色变为棕红色时,关闭活塞。
Ⅳ
已知淀粉遇碘显蓝色。回答下列问题:
碘在元素周期表中的位置为 ______。
该实验利用与浓盐酸反应制取。写出用代替制取的化学方程式:______,装置中湿润的淀粉试纸变蓝说明 ______。
装置的溶液中完全被氧化,则消耗的质量为 ______。
为验证溴元素的非金属性强于碘元素的,过程Ⅳ的操作和现象是 ______。
18. 形成酸雨的原理之一可简示如下:含硫燃气硫酸。
回答下列问题:
物质的化学式是 ______,物质的化学式是 ______。
三个反应中不属于氧化还原反应的是 ______填序号。
中硫元素显价,它可能降低到价,利用这一性质可在工厂的烟道气中通入合适的 ______填氧化剂或还原剂除去,达到减小污染的目的。
从环境保护的角度认为雨水的时,就判定为酸雨。已知,经测定某次雨水中只含硫酸,且浓度为,这次降雨 ______填是或不是酸雨。
你认为减少酸雨的产生可采取的措施是 ______填标号。
A.少用煤作燃料
B.工业废气处理后再排放
C.燃料脱硫
D.把工厂迁移到农村
19. 某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的实验装置。回答下列问题:
某同学拧开分液漏斗下面的活塞后发现浓硫酸开始时能流出,但一会儿就停止下流,请分析原因:______。
加入浓硫酸后,点燃酒精灯,烧瓶中发生反应的化学方程式为______。
反应开始后,观察到、两瓶中溶液均褪色,出现该实验现象分别是由于具有______性和______性。装置的作用是______。
充分反应后,兴趣小组同学发现铜有剩余,其推测烧瓶中是否消耗完,并说明理由:______。
利用石灰乳和硝酸工业的尾气含、反应,既能净化尾气,又能获得应用广泛的,其部分工艺流程如图:
氨的催化氧化是工业制硝酸的基础。写出反应的化学方程式:______。
氨催化氧化制得的经过氧化为,再与水反应得到硝酸。与水反应生成硝酸的反应中,氧化剂与还原剂的物质的量之比为______。已知和的混合气体能被碱液吸收生成亚硝酸盐:,则被溶液完全吸收无气体剩余的离子方程式为 ______。
流程中滤渣可循环使用,滤渣的主要成分是 ______填化学式。
生产中溶液需保持弱碱性。酸性条件下,溶液会发生反应生成、和,该反应的离子方程式为 ______。
2021-2022学年下学期宣化一中高一月考
化学试卷(4月份)答案和解析
1.【答案】
【解析】解:根据分析可知,原子核外有个电子,故A错误;
B.根据分析可知,原子核内有个中子,故B错误;
C.根据分析可知,与互为同位素,故C正确;
D.根据分析可知,核外电子数为,故D错误;
故选:。
月壤中富含,其质子数为,中子数为,质量数为,核外电子数为,是氦元素的一种同位素原子,据此分析作答即可。
本题主要考查原子的过程,属于基本知识的考查,难度不大。
2.【答案】
【解析】解:选项中的金属活泼性,常温下,将金属分别放入水中,反应最剧烈的是,
故选:。
常温下,将金属分别放入水中,发生反应,金属性越强,与水反应越剧烈,据此分析判断。
本题考查了金属性强弱的分析判断,注意金属性强弱的判断依据,题目难度不大。
3.【答案】
【解析】解:用黄铁矿为原料生产硫酸,的化合价发生变化,发生氧化还原反应,故A错误;
B.高温下与反应制高纯硅,氢元素和硅元素的化合价发生变化,发生氧化还原反应,故B错误;
C.用氨为原料生产硝酸,氮元素化合价发生变化,发生氧化还原反应,故C错误;
D.实验室制取氨气,元素化合价未发生变化,不涉及氧化还原反应,故D正确;
故选:。
不涉及氧化还原反应,说明该反应中没有电子转移,其特征是没有元素化合价升降,据此判断。
本题考查氧化还原反应的综合知识,题目难度不大,熟悉物质的性质以及发生的反应过程是解题的关键,试题侧重基础知识的考查,培养了学生的灵活应用能力。
4.【答案】
【解析】解:为共价晶体,干冰为分子晶体,晶体类型不同,其物理性质不同,故A错误;
B.与反应生成和,但和盐酸、硫酸、硝酸等酸都不反应,故B错误;
C.光导纤维的主要成分是二氧化硅,所以用二氧化硅生产光导纤维,故C正确;
D.没有导电性,有导电性,所以超分子纳米管没有导电性,故D错误;
故选:。
A.为共价晶体,干冰为分子晶体;
B.与反应生成;
C.光导纤维的主要成分是二氧化硅;
D.没有导电性。
本题考查二氧化硅的性质,侧重考查基础知识的掌握和灵活运用能力,明确常见物质的晶体类型及性质是解本题关键,题目难度不大。
5.【答案】
【解析】解:水溶液吸收蒸气,利用了二氧化硫的还原性,故A错误;
B.碳化硅为共价晶体,硬度大,可作砂纸或砂轮的磨料,故B正确;
C.具有碱性,依据酸碱中和原理可知氢氧化钙可用于修复被酸雨浸湿的土壤,故C正确;
D.氨气具有还原性,可以与氮的氧化物反应生成氮气,将烟道气中的转化为,故D正确;
故选:。
A.依据二氧化硫的还原性解答;
B.碳化硅为共价晶体,硬度大;
C.依据酸碱中和原理判断;
D.依据氨气的还原性解答。
本题考查物质的组成、性质与用途,把握常见物质的性质与用途等的对应关系为解答的关键,侧重于化学与生产、生活、环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意积累,题目难度不大。
6.【答案】
【解析】解:为第Ⅱ族中某元素的原子序数,若元素处于短周期,Ⅱ族与Ⅲ族相邻,则原子序数为的元素位于周期表的Ⅲ族;若该元素处于长周期,Ⅱ族与Ⅲ族相邻,则原子序数为的元素位于周期表的Ⅲ族,
故选:。
短周期中Ⅱ族与Ⅲ族相邻,长周期中Ⅱ族与Ⅲ族相邻。
本题考查元素周期律表结构,题目比较基础,注意识记族与列的关系,旨在考查学生对基础知识的掌握情况。
7.【答案】
【解析】解:单质分子中可能不存在化学键,如:稀有气体分子中不存在化学键,故A错误;
B.共价化合物中一定是由不同元素组成的,所以一定存在极性键,可能存在非极性键,故B正确;
C.含有共价键的化合物可能是离子化合物,如等,故C错误;
D.只含共价键的化合物是共价化合物,所以共价化合物中一定不含离子键,故D错误;
故选:。
A.单质分子中可能不存在化学键;
B.共价化合物中一定存在极性键,可能存在非极性键;
C.含有共价键的化合物可能是离子化合物;
D.只含共价键的化合物是共价化合物。
本题考查物质和化学键的关系,侧重考查基础知识的掌握和灵活运用能力,明确基本概念内涵是解本题关键,注意规律中的特例,为解答易错点。
8.【答案】
【解析】解:与稀硝酸反应产生的气体是一氧化氮,不会产生氢气,离子反应为,故A错误;
B.二者反应生成碳酸钙、碳酸钠和水,离子方程式为,故B错误;
C.溶于烧碱溶液,反应生成硅酸钠和水,离子反应为,故C正确;
D.与氨水反应,离子方程式:,故D错误,
故选:。
A.与稀硝酸反应产生的气体是一氧化氮;
B.二者反应生成碳酸钙、碳酸钠和水;
C.溶于烧碱溶液,反应生成硅酸钠和水;
D.氨水为弱碱,应保留化学式。
本题综合考查离子方程式的书写,侧重于元素化合物的性质的综合应用,注意物质的化学式、电荷守恒和质量守恒的判断,注意离子反应的先后顺序,题目难度中等.
9.【答案】
【解析】解:生产玻璃的原料是石灰石、纯碱和石英,生成水泥的原料是石灰石和黏土,故A正确;
B.黏土的主要成分是硅酸盐,陶瓷由黏土高温烧制而成,所以陶瓷的主要成分是硅酸盐,故B正确;
C.石英玻璃的主要成分是,不是硅酸盐,故C错误;
D.在雷雨天,空气中和在打雷放电的条件下反应生成,故D正确;
故选:。
A.生产玻璃的原料是石灰石、纯碱和石英,生成水泥的原料是石灰石和黏土;
B.黏土的主要成分是硅酸盐,陶瓷由黏土高温烧制而成;
C.石英玻璃的主要成分是;
D.和在放电的条件下反应生成。
本题主要考查生产玻璃和水泥、陶瓷的原料,石英的成分,的生成条件等,属于基本知识的考查,难度不大。
10.【答案】
【解析】解:、浓盐酸是弱氧化性的酸,能和铁反应生成氢气,故A错误;
B、浓硝酸有强氧化性,能把铁的表面氧化成致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步的反应,故B正确;
C、铁和硫酸铜能发生置换反应,置换出金属铜,故C错误;
D、稀硫酸是弱氧化性的酸,能和铁反应生成氢气,故D错误;
故选B.
A、浓盐酸是弱氧化性的酸,能和铁反应生成氢气;
B、浓硝酸有强氧化性,能把铁的表面氧化成致密的氧化物薄膜而钝化;
C、铁和硫酸铜能发生置换反应,置换出金属铜;
D、稀硫酸是弱氧化性的酸,能和铁反应生成氢气;
本题考查了铁的化学性质,铁、铝都能和浓硫酸、浓硝酸在常温下发生钝化现象,所以可用铁、铝制容器盛放浓硫酸、浓硝酸.
11.【答案】
【解析】解:元素的非金属性越强,则气态氢化物的热稳定性越强,由于非金属性,则气态氢化物的稳定性,故A正确;
B.主族序数最外层电子数,则、、 的最外层电子数分别是、、,即最外层电子数:,故B错误;
C.电子层数越多,则原子半径越大,故原子的半径是最大的;当电子层数相同时,核电荷数越大,则原子半径越小,则原子半径,即原子半径,故C正确;
D.电子层数周期序数,由于处于第三周期,而、处于第二周期,则电子层数:,故D正确;
故选:。
A.元素的非金属性越强,则气态氢化物的热稳定性越强;
B.、、 的最外层电子数分别是、、;
C.电子层数越多,则原子半径越大;当电子层数相同时,核电荷数越大,则原子半径越小;
D.电子层数周期序数。
本题考查了元素非金属性的强弱比较以及电子层数与周期序数、最外层电子数与主族序数之间的关系,难度不大,应注意基础知识的掌握。
12.【答案】
【解析】解:碱金属元素原子最外层个电子,反应中易失去个电子,所以在氧化物中均呈价,故A正确;
B.锂的密度比煤油的密度小,不能保存在煤油中,故B错误;
C.锂与钠反应只生成氧化锂,产物只有一种,故C错误;
D.和密度大于水,沉在水底,故 D错误。
故选:。
A.碱金属元素原子最外层个电子;
B.锂的密度比煤油的密度小;
C.锂与钠反应只生成氧化锂;
D.、、密度小于水,和密度大于水。
本题考查了碱金属的性质,侧重对物理性质的考查,熟悉碱金属的物理性质是解题关键,题目难度不大。
13.【答案】
【解析】
【分析】
本题考查的是物质的量浓度的有关计算,正确求算气体的烧瓶溶液的体积、盛放的烧瓶溶质的物质的量是解本题的关键。
【解答】
在相同条件下,气体摩尔体积相同,烧瓶的容积相同,根据知,氨气、的物质的量之比为:,因能与水反应:,所以各烧瓶中溶质的物质的量之比为:,做喷泉实验时,盛放氨气的烧瓶、含的烧瓶,各烧瓶中溶液的体积分别为:一烧瓶、烧瓶,所以溶液的体积比为:,所以各物质的量浓度之比为:,故C正确。
故选C。
14.【答案】
【解析】
【分析】
本题考查了污染气体二氧化硫的回收利用工艺流程的分析判断,氧化还原反应的规律应用,主要是考查二氧化硫的还原性、三价铁离子的氧化性、二价铁离子的还原性的性质应用,注意反应的产物判断是本题的关键。
【解答】
依据处理二氧化硫气体的工艺流程,各步反应都是完全反应,尾气中的二氧化硫气体,通入酸性硫酸铁溶液中发生氧化还原反应,三价铁离子氧化二氧化硫为硫酸,本身被还原,溶液含有二价铁离子,通入空气会氧化亚铁离子得到含三价铁离子的溶液,溶液可以循环利用。
A.溶液中发生的反应是亚铁离子被氧气氧化为三价铁离子的反应:,故A错误;
B.酸性高锰酸钾与铁离子不能反应,故B错误;
C.由反应可知:、;依据氧化还原反应中氧化剂的氧化性大于氧化产物,所以氧化性,故C错误;
D.过程中生成的硫酸铁溶液可以循环利用,故D正确。
故选D。
15.【答案】 吸收氨气,防止污染空气,并防止空气中的水蒸气进入 验证反应生成了水
【解析】解:熟石灰与氯化铵反应生成氨气、氯化钙和水,由于是浓氨水,故生成的氨气可以逸出,故反应方程式为:,
故答案为:;
加热的硬质玻璃试管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气,说明氧化铜和氨气反应生成铜、氮气和水,反应的化学方程式为:,氨气中的由价升高为价,说明氨气具有还原性,
故答案为:;;
实验中要同时收集少量纯净氮气,故浓硫酸吸收未反应的氨气以及干燥氮气,防止污染空气,并防止空气中的水蒸气进入,
故答案为:吸收氨气,防止污染空气,并防止空气中的水蒸气进入;
、排气法,氮气的密度与空气接近,故此法不可取,故A错误;
B、排水法,题中要求收集干燥的氮气,不符合题意,故B错误;
C、用气囊收集为最好的方法,故C正确,
故答案为:;
装置中的反应要求是干燥的氨气,故利用碱石灰来干燥氨气,水遇无水硫酸铜变蓝,故F的作用是验证水的生成,
故答案为:验证反应生成了水。
熟石灰为氢氧化钙,与氯化铵反应生成氨气和氯化钙;
加热的硬质玻璃试管内黑色氧化铜粉末变为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气,说明氧化铜和氨气反应生成铜、氮气和水;氨气中的化合价升高,体现还原性;
浓硫酸具有吸水性,作用是除杂和干燥;
利用氮气的性质分析,氮气是不溶于水的比空气略轻的气体;
利用碱石灰的吸水作用干燥氨气,利用硫酸铜遇到水变蓝的特征现象判断生成的水。
16.【答案】
【解析】解:由分析可知,为、为、为、为、为、为;
为元素,原子核外有个电子,原子结构示意图为,元素非金属性,故氢化物稳定性,
故答案为:;;
同周期自左而右原子半径减小,同主族自上而下原子半径增大,所有元素中氢原子半径最小,一般电子层越多原子半径越大,上述六种元素的原子半径大小为,
故答案为:;
为元素,其最高价氧化物对应的水化物的化学式为,
故答案为:;
的氢化物为,的最高价氧化物对应的水化物为,二者反应生成硝酸铵,反应的离子方程式为,
故答案为:。
A、、、、、是原子序数依次增大的短周期主族元素,其中的原子半径在短周期中最小,则为元素;、形成的最简单化合物是一种气体,其水溶液呈碱性,则为元素;的最外层电子数是内层电子数的倍,由于最外层电子数不超过,原子只能有个电子层,最外层电子数为,故C为元素;和处于同一主族,则为元素;常温下,的单质在浓硫酸中会钝化,则为;的原子序数大于硫,故F为。
17.【答案】第五周期第Ⅶ族 浓 氯气的氧化性强于碘单质的氧化性 打开活塞,将装置中的少量溶液滴入装置中,关闭活塞,取下装置振荡,静置后层变为紫红色
【解析】解:Ⅰ是卤族元素,在元素周期表中位于第五周期第Ⅶ族,
故答案为:第五周期第Ⅶ族;
与浓盐酸反应制取,化学方程式:浓;淀粉遇到变蓝,装置中湿润的淀粉试纸变蓝,说明的氧化性大于,即氯元素的非金属性强于碘元素,
故答案为:浓;氯气的氧化性强于碘单质的氧化性;
装置中发生反应为:,的溶液中,消耗氯气的物质的量为:,,
故答案为:;
为验证溴的氧化性强于碘,应将中生成的溴加入到盛有溶液的中,若发生置换反应,则静至后层溶液变为紫红色,故操作应为:打开活塞,将装置中的少量溶液滴入装置中,关闭活塞,取下装置振荡,静置后层变为紫红色,
故答案为:打开活塞,将装置中的少量溶液滴入装置中,关闭活塞,取下装置振荡,静置后层变为紫红色。
装置中浓盐酸与高锰酸钾反应放出氯气,氯气遇到湿润的淀粉试纸,试纸变蓝;氯气通入、中发生置换反应生成溴;浸有氢氧化钠的棉花可以吸收多余的氯气等,防止污染;中的溴能够与中的反应置换出碘,据此分析解答。
18.【答案】 还原剂 是
【解析】解:由图可知,物质的化学式是,物质的化学式是,
故答案为:;;
反应中硫元素化合价没有改变,不属于氧化还原反应,
故答案为:;
中硫元素显价,它可能降低到价,表现出氧化性,利用这一性质可在工厂的烟道气中通入合适的还原剂除去,达到减小污染的目的,
故答案为:还原剂;
硫酸浓度为,则氢离子浓度为,,则这次降雨是酸雨,
故答案为:是;
少用煤作燃料,可以减少的排放,进一步减少酸雨的排放,故A正确;
B.工业废气中也含有,处理后再排放,以减少的排放,进一步减少酸雨的排放,故B正确;
C.燃料经过脱硫处理后,以减少的排放,进一步减少酸雨的排放,故C正确;
D.把工厂迁移到农村,并不能以减少的排放,即不能减少酸雨的排放,故D错误;
故答案为:。
由图可知,是二氧化硫,是三氧化硫;
氧化还原反应中必须有元素化合价改变;
中硫元素显价,它可能降低到价,表现出氧化性,可以加入还原剂;
硫酸浓度为,则氢离子浓度为,;
减少的排放,进一步减少酸雨的排放,据此分析作答。
19.【答案】随着反应的进行,圆底烧瓶内压强增大,导致液体不能顺利滴下 浓 漂白 还原 吸收剩余气体,防止污染空气 没有,硫酸浓度变稀,稀硫酸不能与铜反应
【解析】解:由于铜与浓硫酸加热生成二氧化硫气体,随着反应的进行,圆底烧瓶内压强增大,导致液体不能顺利滴下,所以反应停止了,
故答案为:随着反应的进行,圆底烧瓶内压强增大,导致液体不能顺利滴下;
铜和热的浓硫酸反应铜作还原剂,硫酸作氧化剂,生成二氧化硫、硫酸铜和水,反应的化学方程式为:浓,
故答案为:浓;
二氧化硫与品红溶液反应生成不稳定的无色物质,二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫具有还原性,能被氯水氧化,氯水褪色,发生;是酸性氧化物,也是大气污染物,所以用溶液吸收,氢氧化钠和二氧化硫反应生成亚硫酸钠和水,反应的方程式为:,
故答案为:漂白;还原;吸收剩余气体,防止污染空气;
铜和浓硫酸混合加热,随反应的进行,硫酸溶液的浓度降低,变为稀硫酸,与稀硫酸不反应,则反应后有硫酸剩余,
故答案为:没有,硫酸浓度变稀,稀硫酸不能与铜反应。
铜与浓硫酸加热反应生成二氧化硫气体,烧瓶中压强增大,导致气体不能顺利留下;
铜和热的浓硫酸反应生成二氧化硫、硫酸铜和水;
二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫与氯水作用,二氧化硫具有还原性;铜和热的浓硫酸反应,生成的二氧化硫为大气污染物,氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
在加热条件下,只能溶解于浓硫酸,不能溶于稀硫酸。
20.【答案】 :
【解析】解:氨的催化氧化是工业制硝酸的基础,该反应的化学方程式为,
故答案为:;
氨催化氧化制得的经过氧化为,再与水反应得到硝酸,与水反应生成硝酸的反应中,氧化剂与还原剂的物质的量之比为:,已知和的混合气体能被碱液吸收生成亚硝酸盐:,则被溶液完全吸收无气体剩余的离子方程式为,
故答案为::;;
流程中滤渣可循环使用,滤渣的主要成分是,
故答案为:;
生产中溶液需保持弱碱性,酸性条件下,溶液会发生反应生成 、 和,该反应的离子方程式为,
故答案为:。
工业上将与进行催化氧化生成与;
氧化剂是物质所含元素化合价降低的反应物,还原剂是物质所含元素化合价升高的反应物,被溶液完全吸收发生歧化反应生成、、;
流程中滤渣为多余的;
生产中溶液需保持弱碱性,酸性条件下,溶液会发生歧化反应生成 、 和,根据电荷守恒、原子守恒、化合价升降守恒即可写出反应的离子方程式。
河北省张家口市宣化区2022-2023学年高二下学期6月月考化学试卷(Word版含答案): 这是一份河北省张家口市宣化区2022-2023学年高二下学期6月月考化学试卷(Word版含答案),文件包含河北省张家口市宣化区2022-2023学年高二下学期6月月考化学试卷docx、河北省张家口市宣化区2022-2023学年高二下学期6月月考化学答案docx等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
精品解析:河北省张家口市宣化第一中学2022-2023学年高二下学期5月期中化学试题(解析版): 这是一份精品解析:河北省张家口市宣化第一中学2022-2023学年高二下学期5月期中化学试题(解析版),共22页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
河北省张家口市宣化区2021-2022学年高二下学期3月月考化学试卷(含答案): 这是一份河北省张家口市宣化区2021-2022学年高二下学期3月月考化学试卷(含答案),共21页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












