




2020-2021学年第一单元 化学反应速率课文ppt课件
展开考纲要求: 1 知道化学反应速率的概念及定量表示2 了解外界条件对化学反应速率的影响3 能用有效碰撞理论解释外界条件对速率的影响4 学会实验数据的记录与处理
问题1、金属与酸或水反应速率主要取决于什么?
铝与盐酸反应速率取决于什么?
一、反应速率的表示方法
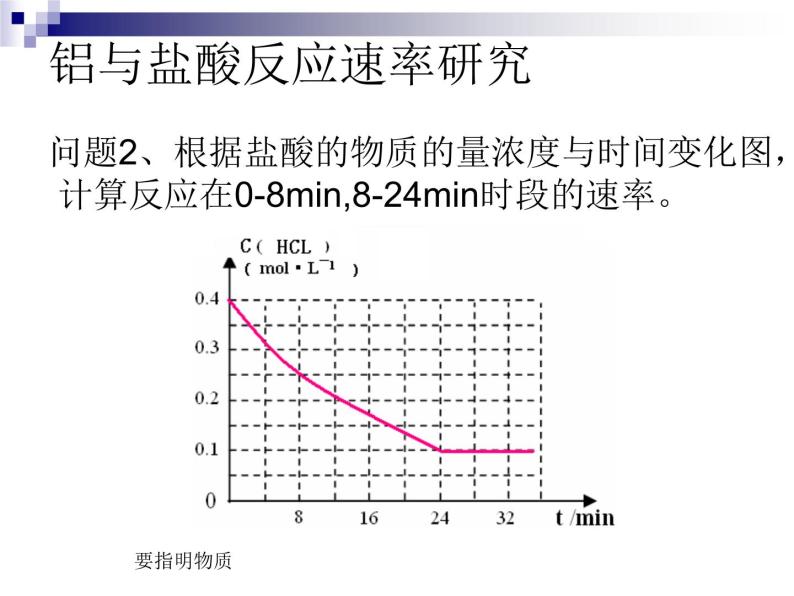
问题2、根据盐酸的物质的量浓度与时间变化图,计算反应在0-8min,8-24min时段的速率。
问题3、以下反应速率中,你认为速率最大的是哪一项。
A、v(HCl) = 0.1 ml·L‑1·min‑1 B、v(AlCl3) = 0.2 ml·L‑1·min‑1 C、v(HCl) = 0.01 ml·L‑1·s‑1
② 同一反应的反应速率可以用不同的物质表示,其数值可能不同,但所表示的意义是相同的。在表示反应速率时,应注明是由哪种物质表示的 。
④ 通常所说的速率是指整个过程中的平均速率而不是瞬时速率,且均为正值。
③ 同一反应中,各物质的反应速率之比等于其化学方程式中的化学计量数之比。
① 固体和纯液体c是常数,化学反应速率一般不用固体或纯液体表示。
⑤对于可逆反应,通常所计算的是正逆反应抵消后的总反应速率。
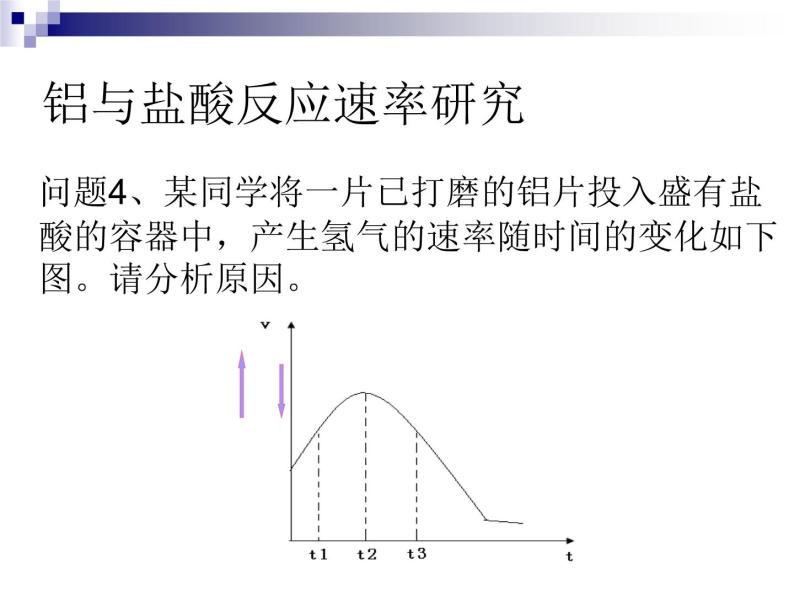
问题4、某同学将一片已打磨的铝片投入盛有盐酸的容器中,产生氢气的速率随时间的变化如下图。请分析原因。
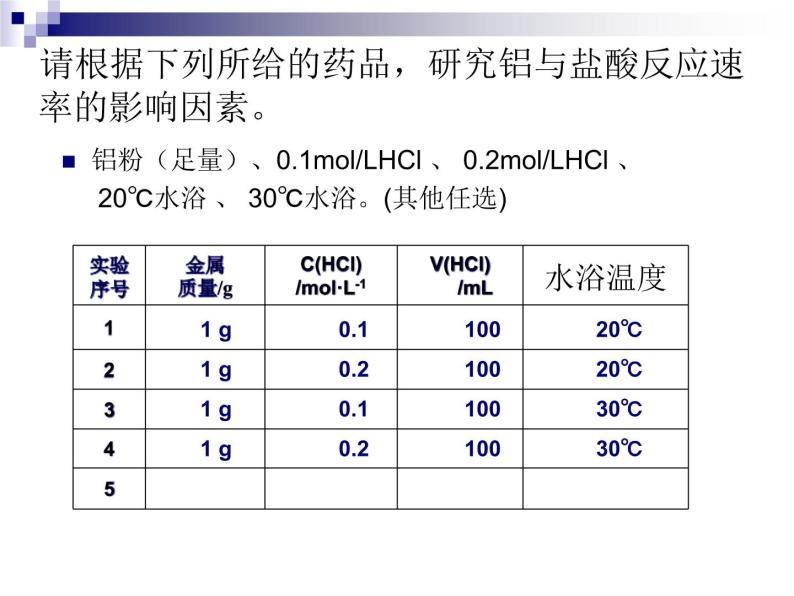
请根据下列所给的药品,研究铝与盐酸反应速 率的影响因素。
铝粉(足量)、0.1ml/LHCl 、 0.2ml/LHCl 、 20℃水浴 、 30℃水浴。(其他任选)
例.实验室用铁片和稀硫酸反应制取氢气,下列措施不能使氢气生成速率增大的是( )A.不用铁片,改用铝片B.改用质量分数为98%的浓硫酸C.加热D.不用铁片,改用铁粉
【高考节选】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为: 2NO+2CO 2CO2+N2。
请在上表空格中填入剩余的实验条件数据。
(5)研究表明:为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
二、反应速率的影响因素
浓度、温度、压强、催化剂等。
一、内因: 物质本身的结构和性质是化学反应速率大小的决定因素。
① 增大浓度② 增大加压
单位体积分子总数增多但活化分子百分数不变
单位体积活化分子数增多
③ 升高温度④ 用催化剂
单位体积分子总数不变但活化分子百分数增大
特别是微型原电池的形成可以加大某些反应速率。
反应物颗粒的大小,溶剂的性质,光、超声波,电磁波等都可能会改变反应速率。
2SO2(g)+O2(g) 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的反应速率B.增大压强,反应速率一定增大C.该反应是放热反应,降低温度将缩短反应达到平衡的时间D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2 内,SO3(g)生成的平均反应速率为v=
下列有关化学反应速率的说法中,正确的是 ( ) A. 100 mL 2 ml/L 的盐酸与锌反应时,加入适量的氯化钠溶 液,生成氢气的速率不变 B. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以 加快产生氢气的速率 C. 二氧化硫的催化氧化是一个放热反应,所以升高温度,反 应速率减慢 D. 汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小 压强,反应速率减慢
一定条件下,可逆反应:N2+3H2 2NH3 △H<0 达到平衡,从t1~t4,依次改变一个条件,对应的v-t曲线如下图所示,试根据曲线变化特征判断依次改变的是哪些条件?
t1 ——( ) t2 ——( )t3 ——( ) t4 ——( )
t5时,在恒温条件下,向混合体系中充入氩气,则反应速率将如何改变?试画出t5后v-t变化图。
苏教版 (2019)选择性必修1第一单元 化学反应速率教案配套ppt课件: 这是一份苏教版 (2019)选择性必修1第一单元 化学反应速率教案配套ppt课件,共48页。PPT课件主要包含了图说考点,基础知识,每一步,反应机理,有效碰撞,活化能,放出的能量,反应热,活化分子数,有效碰撞的次数等内容,欢迎下载使用。
高中化学苏教版 (2019)选择性必修1专题2 化学反应速率与化学平衡第一单元 化学反应速率课堂教学ppt课件: 这是一份高中化学苏教版 (2019)选择性必修1专题2 化学反应速率与化学平衡第一单元 化学反应速率课堂教学ppt课件,共49页。PPT课件主要包含了图说考点,基础知识,molL·s,纯液体,化学物质,颜色深浅,有色物质浓度,答案B,答案D,A⇌B+3C等内容,欢迎下载使用。
苏教版选修4 化学反应原理第一单元 化学反应速率课文配套课件ppt: 这是一份苏教版选修4 化学反应原理第一单元 化学反应速率课文配套课件ppt,共14页。PPT课件主要包含了炸药爆炸,瞬间完成,离子反应,以秒计,食物腐败,以天计,金属锈蚀,以年月计,塑料老化,以年计等内容,欢迎下载使用。













