






高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用课文内容ppt课件
展开第二章 化学与资源开发利用
高考导航考纲要求1.了解海水的综合利用。了解化学科学发展对自然资源利用的作用。2.了解化学在水处理中的应用。
3.了解煤、石油和天然气等综合利用的意义。4.了解化学对废旧物资再生与综合利用的作用。
命题热点1.考查一些技术的处理和运用。2.以实验探究、框图考查金属的制取和海水资源的利用及环保。
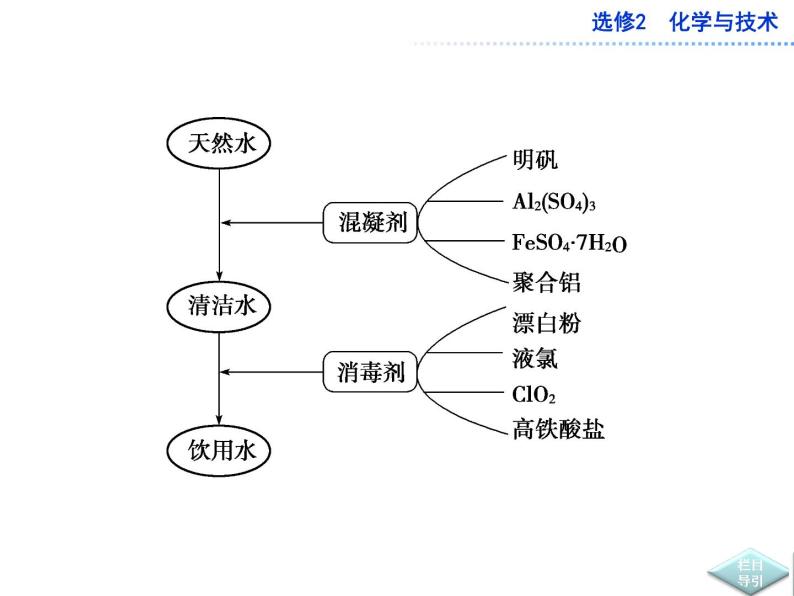
1.水的净化(1)基本流程
2.硬水的软化(1)硬水和软水
(2)硬水的类型暂时硬度——由钙、镁的碳酸氢盐引起的硬度永久硬度——由钙、镁的硫酸盐或氯化物引起的硬度
(3)硬水软化的方法①加热法(只能软化具有暂时硬度的水)其原理是:Ca(HCO3)2 CaCO3↓+CO2↑+H2O,Mg(HCO3)2 MgCO3↓+CO2↑+H2O,
继续煮沸时,MgCO3可转化为更难溶的Mg(OH)2:MgCO3+H2O Mg(OH)2↓+CO2↑。
②药剂法(石灰纯碱法)
③离子交换法利用离子交换反应原理,软化水的质量高。常用离子交换树脂作离子交换剂,其软化硬水和再生的过程如图所示:
3.污水处理(1)基本流程
(2)污水处理的常用方法
(2011·高考山东卷)水处理技术在生产、生活中应用广泛。(1)含有较多________离子的水称为硬水。硬水加热后产生碳酸盐沉淀的离子方程式为_______________________________________________(写出一个即可)。
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应先使硬水通过________(填“RH”或“ROH”)型离子交换树脂,原因是______________________________________________________________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为________。电渗析法净化水时,使离子通过半透膜的推动力是________。(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的________。
(3)通过压力使水分子通过半透膜而获得纯净水的方法称为反渗透法,电渗析法的推动力是电压。(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的电导率(或电阻率).
即时应用1.(2010·高考新课标全国卷)水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。请回答下列问题:(1)天然水中溶解的气体主要有________、________。
(2)天然水在净化处理过程中加入的混凝剂可以是__________________________(填其中任何两种),其净水作用的原理是________________________________________________________________________。
(3)水的净化与软化的区别是________________________________________________________________________________________________________________________________________________。
解析:(1)天然水中溶解的气体主要是空气,空气由N2、O2、CO2、水蒸气等气体组成。(2)混凝剂的作用是净化水,即除去水中悬浮的杂质,能作混凝剂的物质为铁盐或铝盐,其净水原理是应用Al3+(或Fe3+)的水解,
Al3++3H2O=== Al(OH)3(胶体)+3H+, Fe3++3H2O===Fe(OH)3(胶体)+3H+,由于生成的胶体中胶粒有较大的比表面积,可以吸附水中的悬浮物,并且金属氢氧化物形成的胶粒吸附阳离子后带正电荷,破坏天然水中其他带异电的胶体,达到净水的目的。
答案:(1)O2 CO2(或氮气)(2)明矾、硫酸铝、硫酸铁、硫酸亚铁(任填两种) 铝盐或铁盐在水中发生水解生成相应氢氧化物胶体,它可吸附天然水中悬浮物并破坏天然水中的其他带异电的胶体,使其聚沉,达到净化目的
(3)水的净化是用混凝剂(如明矾等)将水中胶体及悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子(4)10°(5)740 1484
1.海水淡化常用方法有蒸馏法、电渗析法等。2.海水中盐的开发和利用
3.海水提溴反应原理Cl2+2NaBr===2NaCl+Br2
3Br2+3Na2CO3===5NaBr+NaBrO3+3CO2↑5NaBr+NaBrO3+3H2SO4===3Br2+3Na2SO4+3H2O
特别提醒(1)通氯气前要将海水酸化,pH为3.5时,氯气的氧化效果最好。(2)用空气或H2O(g)将溴吹出,而不用CCl4萃取,因后者工艺复杂,设备投资大,经济效益低且对环境污染严重.
4.从海水中提取镁单质(1)生产流程及反应原理
(2)化学原理在化工生产中的应用①沉淀溶解平衡原理a.向海水中加入沉淀剂Ca(OH)2,由于c(OH-)增大,Mg(OH)2的溶解度小于Ca(OH)2,则最大程度地将Mg2+转化为Mg(OH)2沉淀。
b.向Mg(OH)2沉淀中加入盐酸,使沉淀溶解平衡右移。②水解平衡原理在MgCl2·6H2O脱水变为MgCl2时,由于MgCl2+2H2O Mg(OH)2+2HCl水解平衡的存在,在HCl气体环境中,增大c(HCl),抑制了MgCl2的
水解,避免了Mg(OH)2的生成。
海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景。回答下列问题:(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但常规蒸馏法也存在较大缺陷,请说明常规蒸馏法淡化海水的最大缺陷:
________________________________________________________________________________________________________________________________________________。
(2)离子交换法也是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式________________________________________________________________________________________________________________________________。
(3)目前从海水中提取溴的常用流程如下(苦卤,海水蒸发结晶分离出食盐的母液):
从反应③后的溶液中分离出单质溴的方法是_______________________________________________________________。(4)海水提镁过程与石灰窑和盐酸厂有着紧密的联系,试说明海水提镁与盐酸厂之间的必然联系:
【解析】 (1)常规蒸馏法淡化海水的最大缺陷是需要使用大量燃煤,因此能耗多、排污量大。(2)聚丙烯酸钠的单体为丙烯酸钠,其结构简式为CH2===CHCOONa。
(3)由流程可知,从反应③后的溶液中分离出单质溴的方法是蒸馏。(4)海水提镁过程与石灰窑和盐酸厂有着紧密的联系,盐酸厂为溶解氢氧化镁提供盐酸,而在电解氯化镁制镁的过程中,可为盐酸厂提供氯气作原料.
【答案】 (1)需要使用大量燃煤,因此能耗多、排污量大(2)CH2===CHCOONa (3)蒸馏(4)盐酸厂为溶解氢氧化镁提供盐酸,在电解氯化镁制镁的过程中,可为盐酸厂提供氯气作原料
即时应用2.(2012·双鸭山高三第一次模拟)工业上对海水资源综合开发利用的部分工艺流程如图所示。
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜均允许通过的分子或离子是________。电解槽中的阳极材料为________。(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、
CaSO4顺序制备?________(填“是”或“否”)。原因是________________________________________________________________________。
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶, 故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是________________________________________________________________________。
解析:(1)电解饱和食盐水用的是阳离子交换膜,而在食盐水中的阳离子只有H+和Na+,电解时,H+在阴极上生成氢气,Na+在外加电场作用下向阴极运动,所以通过离子膜和隔膜的是Na+。由于阳极上发生氧化反应,是溶液中Cl-放电生成Cl2,所以必须
用惰性电极,工业上一般用钛(表面涂有钌氧化物),也可以用石墨电极。(2)在该流程开始时向苦卤中加入硫酸,因CaSO4微溶于水,先形成CaSO4沉淀而将Ca2+除去.若先制取Mg(OH)2,加入的石灰水会有部分与硫酸反应生成CaSO4而使制得的Mg(OH)2不纯净.
(3)CCl4是一种易挥发、有毒的液体,所以此流程中不用CCl4萃取的方法,而是利用溴的挥发性,向得到的含溴水的海水中吹入热空气,使溴挥发出来。与萃取相比,该方法简单、实用、经济、无污染。
答案:(1)阳离子(或Na+) 钛(或石墨)(2)否 如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯(3)四氯化碳萃取法工艺复杂、设备投资大,经济效益低、环境污染严重
特别提醒(1)汽油指含有5~11个碳原子的烃,裂化汽油与直馏汽油不同,裂化汽油中含不饱和烃,能使溴的四氯化碳溶液褪色,而直馏汽油不能。
(2)裂解气中主要含乙烯、丙烯、丁烯等短链气态烃,而液化石油气是石油常压分馏的产物,主要含有丙烷、丁烷及少量戊烷、戊烯和含硫化合物。
3.煤化工和天然气化工的发展——一碳化学一碳化学是指以分子中只含一个碳原子的化合物(如一氧化碳、甲烷、甲醇等)为原料,合成一系列化工原料和燃料的化学。
注意:一组易混淆的概念
(2012·乐山高三第一次模拟)四川有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):
请填写下列空白:(1)已知0.5 ml甲烷和0.5 ml水蒸气在t ℃,p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是:______________________________________________________________。
(2)在合成氨的实际生产过程中,常采取的措施之一是将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气。请应用化学反应速率和化学平衡的观点说明采取该措施的理由:__________________________。
(3)当甲烷合成氨气的转化率为75%时,以5.60×107 L甲烷为原料能够合成________L氨气。(假设体积均在标准状况下测定)(4)已知尿素的结构简式为H2NCONH2,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
①____________________,②____________________。【解析】 (1)书写热化学方程式时要注意反应物的量与反应热的关系,同时还要注意反应物和生成物的状态。
(2)分离氨气目的是减小生成物浓度,使平衡正向移动;增大氮气和氢气浓度既可加快反应速率又可使平衡向正反应方向移动。(3)根据反应关系式可知:CH4 ~ 2NH3 5.60×107L×75% 8.4×107 L
【答案】 (1)CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH(t ℃,p kPa)=+2a kJ/ml(2)增大氮气和氢气的浓度有利于增大反应速率;减小氨气的浓度,增大氮气和氢气的浓度都有利于平衡向正反应方向移动
(3)8.4×107(4)① ②
即时应用3.(2012·西安高三质检)如何从石油中获得更多的轻质燃油一直是化学家探索的课题,将石油分馏得到的重油进行裂化可以获得更多的轻质燃油。资料1:石蜡是含有20~30个碳原子的烷烃的混合物,常温下呈固态。
资料2:石油催化裂化中通常使用Al2O3作催化剂。某研究性学习小组在实验室中模拟石油的催化裂化,装置如图。实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试
管Ⅱ中液体气味,具有汽油的气味。
(1)该装置仪器连接的顺序应遵循的原则为______________________,为保证实验成功,实验前必须进行的操作是__________________________,装置中较长导管的作用是_____________________________________________________________;
(2)试管Ⅱ中少量液体凝结说明_____________________________________________________________;(3)试管Ⅲ中溶液褪色说明_______________________________________________________________;
(4)能否用试管Ⅱ中的液体萃取溴水中的溴,理由是________________________________________________________________________________________________________________________________________________;
(5)写出二十烷裂化得到癸烷和癸烯的化学方程式________________________________________________________________________________________________________________________________________________;
(6)石油裂化的重要意义是________________________________________________________________________________________________________________________________________________。
解析:仪器连接的顺序应遵循从下往上,从左到右的原则,装入药品之前要检验装置的气密性。依据石油分馏工业的分馏塔原理,设置了长导管,其作用除导气外,兼起冷凝气体的作用;依据催化裂化原理,下列反应皆有可能发生:
试管Ⅱ中有液体生成,说明生成了5个碳原子数以上的烃,因为常温常压下,含5个碳原子以上的烃大都呈液体,试管Ⅲ中酸性KMnO4溶液褪色说明生成常温常压下呈气态的5个碳原子以下的烯烃;由于裂化产物中有烯烃生成,易与溴发生加成反应,所以不能用试
管Ⅱ中的液体萃取溴水中的溴;从以上变化可以看出,石油裂化的主要目的是为了获得更多的轻质燃油,特别是提高汽油的产量和质量。
答案:(1)从下往上,从左往右 检验装置的气密性 导气、冷凝气体(2)裂化生成了含5个碳原子以上的烃(3)裂化生成了碳原子数小于5的烯烃(4)不能,因为裂化产物中有烯烃,易与溴发生加成反应,不能用来萃取溴
(5)C20H42A C10H22+C10H20(6)可提高石油产品中轻质燃油特别是汽油的产量和质量
高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用复习ppt课件: 这是一份高中化学人教版 (新课标)选修2 化学与技术课题2 海水的综合利用复习ppt课件,共20页。PPT课件主要包含了获取纯净的水,海水的综合利用,氯碱工业,汽油C5C11,煤油C11C16,柴油C15C18,重油C20以上,减压蒸馏塔,催化裂化,石油气C4以下等内容,欢迎下载使用。
人教版 (新课标)选修2 化学与技术课题2 海水的综合利用图文课件ppt: 这是一份人教版 (新课标)选修2 化学与技术课题2 海水的综合利用图文课件ppt,共21页。PPT课件主要包含了生产中反应条件的控制,生产中的三废处理,能量的充分利用等内容,欢迎下载使用。
人教版 (新课标)选修2 化学与技术课题2 海水的综合利用说课课件ppt: 这是一份人教版 (新课标)选修2 化学与技术课题2 海水的综合利用说课课件ppt,共60页。PPT课件主要包含了Al2SO43,FeSO4,漂白粉,天然水,Mg2+,碳酸氢盐,硫酸盐或氯化物,加热法,污水处理基本流程,蒸馏法等内容,欢迎下载使用。













