人教版 (2019)选择性必修1第一节 反应热综合训练题
展开知识梳理
定义:在101 kPa时,1 ml纯物质完全燃烧生成指定产物时放出的热量,叫做该物质的燃烧热。
(1)可燃物的物质的量必须是1 ml;
(2)可燃物完全燃烧生成的产物必须为稳定的物质,完全燃烧时不同的元素对应的稳定物质:
N→N2(g),C→CO2(g),H→H2O(l)等。
一、单选题
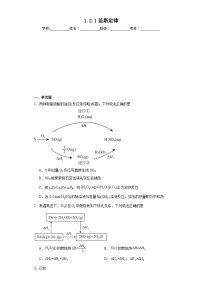
1.下列反应的焓变等于相关可燃物燃烧热的是
A.
B.
C.
D.
2.下列有关反应热说法错误的是
A.测量中和热时,装置中填充碎泡沫塑料的作用是减少热量损失
B.已知: ,则NaOH稀溶液与稀醋酸生成1ml水,放出热量小于57.3kJ
C.已知: ,则1ml (g)和2ml (g)充分反应,放出热量小于akJ
D.表示甲烷燃烧热的热化学方程式:
3.下列依据热化学方程式得出的结论正确的是
A.的燃烧热是,则
B.在、时,完全燃烧生成液态水,放出热量,则表示氢气燃烧热的热化学方程式为:
C.在稀溶液中:;,若将含的浓硫酸与含的溶液混合,放出的热量小于
D.、下,已知热化学方程式:,将和置于密闭容器中充分反应生成,放热
4.下列热化学方程式或离子方程式中,正确的是
A.25℃、101kPa时,碳的燃烧热为-393.5kJ/ml
B.一定条件下,将0.5ml和1.5ml置于密闭的容器中充分反应生成,放热19.3kJ,热化学方程式为:
C.1ml完全燃烧生成放出的热量叫的燃烧热
D.的燃烧热是,分解的热化学方程式为:
5.在25℃、101KPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列表示甲醇燃烧热的热化学方程正确的是
A.CH3OH(l)+O2(g)=CO2(g)+2H2O(l) ΔH=-725.8kJ/ml
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ /ml
C.CH3OH(l)+O2(g)=CO2(g)+2H2O(g) ΔH=+725.8 kJ /ml
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=+1452 kJ /ml
6.下列说法正确的是
A.1mlH2完全燃烧生成H2O(g)放出的热量叫H2的燃烧热
B.25℃、101kPa时,1mlS和2mlS的燃烧热相等
C.已知S(s)+O2(g)=SO3(g) ∆H=-269.8kJ/ml,则硫生成SO3的反应热为269.8kJ/ml
D.25℃、101kPa时,碳的燃烧热为-393.5kJ/ml
7.下列关于燃烧热的说法正确的是
A.燃烧反应放出的热量就是该反应的燃烧热
B.1ml可燃物发生氧化反应所放出的热量就是燃烧热
C.1ml可燃物完全燃烧生成稳定化合物时所放出的热量就是燃烧热
D.101KPa时,1ml纯物质完全燃烧生成指定产物(C元素变为CO2气体、H元素变为液态H2O等)时所放出的热量就是燃烧热
8.下列关于热化学反应的描述中正确的是
A.若盐酸和NaOH溶液反应生成1mlH2O(l)的ΔH为-57.3kJ•ml-1,则CH3COOH溶液和Ba(OH)2溶液反应生成1mlH2O(l)的ΔH也为-57.3kJ•ml-1
B.CO(g)燃烧热是283.0kJ·ml-1,则2CO2(g)=2CO(g)+O2(g)的ΔH=-(2×283.0)kJ•ml-1
C.N2(g)燃烧热是指在101kPa,1mlN2(g)完全生成NO2(g)时所放出的热量
D.同温同压下,4Al(s)+3O2(g)=2Al2O3(s)在常温和点燃条件下的ΔH相同
9.下列对反应热、热化学方程式等有关知识的叙述,正确的是
A.已知热化学方程式:SO2(g)+O2(g)SO3(g) △H=-98.32kJ·ml-1,则在容器中充入2mlSO2和1mlO2充分反应、最终放出的热量为196.64kJ
B.含10gNaOH的稀溶液与足量的稀硫酸完全中和,放出14.35kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ·ml-1
C.已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·ml-1,则氢气的燃烧热为△H=-241.8kJ·ml-1
D.已知石墨转化为金刚石吸热,则石墨比金刚石稳定
10.下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ/ml,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/ml
B.500℃、30MPa下,将0.5mlN2(g)和1.5mlH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)△H=-38.6kJ/ml
C.稀HCl和NaOH溶液反应的中和热△H=-57.3kJ/ml,则稀H2SO4和NaOH溶液反应的中和热△H=2×(-57.3).kJ/ml
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/ml
二、填空题
11.已知下列反应:
① 2C(s)+O2(g)=2CO(g) △H1 = –221 kJ/ml
② CO(g)+1/2O2(g)=CO2 (g) △H2 = –283 kJ/ml
③ 稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H3 = –57.3 kJ/ml
请回答下列问题:
(1)碳(C)的燃烧热为 。已知碳的两种同素异形体的转化如下:C(s,金刚石) = C(s,石墨) △H = –1.9 kJ/ml ,则从能量角度判断:稳定性更大的是 (填名称)
(2)写出能表达反应③意义的一个热化学方程式 ,向2L 0.5ml/L的NaOH溶液中加入稀醋酸,恰好完全反应时的热效应为△H4 ,则△H3 △H4(填“>”,“=”或“<”)
12.回答下列问题:
(1)在25℃、101kPa时,1.00g C6H6(l)燃烧生成CO2和H2O(l)时,放出41.8kJ的热量,表示C6H6(l)燃烧热的热化学方程式为 。
(2)1.00L 1.00ml/LH2SO4溶液与2.00L 1.00ml/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为 。
(3)已知反应CH3-CH3→CH2=CH2(g)+H2(g),有关化学键的键能如下:
通过计算得出该反应的反应热为 。
(4)已知2.0g燃料肼(N2H4)气体完全燃烧生成N2和H2O(g)时,放出33.4kJ的热量,则该反应的热化学方程式为 。
13.(1)氢能源是绿色燃料,可以减少汽车尾气的排放,利用甲醇与水蒸气反应可以制备氢气:CH3OH(g)+H2O(g)===CO2(g)+3H2(g)。下图是该反应的能量变化图:
①通过图中信息可判断反应CH3OH(g)+H2O(g)===CO2(g)+3H2(g)的ΔH 0(选填“>”“=”或“<”)。
②图中途径(Ⅱ)的条件是 ,途径(Ⅰ)的反应热 途径(Ⅱ)的反应热(选填“>”“=”或“<”)。
③在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/ml
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/ml
③H2O(l)===H2O(g) ΔH=+44.0 kJ/ml
写出CO2与NH3合成尿素和液态水的热化学反应方程式 。
14.依据事实,写出下列反应的热化学方程式
(1)已知1g碳粉在氧气中完全燃烧放出的热量是32.8kJ,试写出相关的热化学方程式 .
(2)在25℃、101kPa下,2g甲烷(CH4)燃烧生成CO2和液态水时放热25kJ.则表示甲烷燃烧热的热化学方程式为 .
15.回答问题
(1)反应的则的燃烧热是 。
(2)葡萄糖的燃烧热是,则表示葡萄糖燃烧热的热化学方程式为 。
(3)氢气的燃烧热为,则电解水的热化学方程式为 。
(4)已知中和反应的中和热为。则和盐酸反应表示中和热的热化学方程式为 。
(5)乙硼烷(分子式)在氧气中燃烧,生成固态三氧化二硼和液态水,放出的热量,则其热化学方程式为 。
16.碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
ΔH=88.6kJ/ml
则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热为726.5kJ·ml-1,CH3OH(l)+O2(g)===CO2(g)+2H2(g) ΔH=-akJ·ml-1,则a 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mlCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式: 。
17.在1.01×105Pa时,16g S在足量的氧气中充分燃烧生成二氧化硫,放出148.5KJ的热量,则S的燃烧热为 ;
S燃烧的热化学方程式为 。
18.0.5 ml CH4完全燃烧生成CO2和H2O时,放出445 kJ的热量,写出CH4燃烧热的热化学方程式: 。
19.碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:ΔH=+88.6kJ·ml-1。,则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热ΔH=-726.5kJ·ml-1,CH3OH(l)+O2(g)===CO2(g)+2H2(g)ΔH=-akJ·ml-1,则a 726.5(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mlCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式: 。
(4)根据下表中键能数据估算CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为 。
20.乙炔()气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是: 。则1kg乙炔在氧气中完全燃烧放出多少热 ?
三、实验探究题
21.利用下图装置测定中和热的实验步骤如下:
①用量筒量取50mL 0.25ml/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55ml/L NaOH溶液,测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/ml): 。
(2)倒入NaOH溶液的正确操作是: 。(从下列选项中选出)
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃棒,两个小孔不能开得过大,其原因是 ;反应需要测量温度,每次测量温度后都必须 。
(4)另取50mL HCl(0.1ml•L-1)溶液与50mL NaOH(0.1ml•L-1)溶液在小烧杯中进行中和反应,通过实验并计算可得中和热为54.8kJ/ml,上述实验数值与57.3kJ/ml有偏差,产生此偏差的原因可能是 (填字母序号)。
a、实验装置保温、隔热效果差
b、用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度
c、一次性把NaOH溶液倒入盛有盐酸的小烧杯中
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”或“无影响”)原因为 。
22.Ⅰ.已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·ml-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·ml-1
下列结论中正确的是 。
A.碳的燃烧热等于110.5kJ·ml-1
B.①的反应热为221kJ·ml-1
C.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ·ml-1
D.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.65kJ的热量
Ⅱ.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50mL 0.50ml·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL 0.55ml·L-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)仪器a的名称是 。
(2)反应过程中NaOH溶液的浓度为0.55ml·L-1,不能使用0.50ml·L-1 NaOH的原因是 。
(3)倒入NaOH和盐酸溶液的正确操作是 (填字母)。
A.沿玻璃棒缓慢倒入 B.分三次倒入
C.一次迅速倒入 D.一边搅拌一边一次滴入
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1ml·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为 。
(5)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸所测中和热的数值并不相等,从它们的离子方程式分析,所测中和热的数值并不相等的理由是 。
23.Ⅰ.当今社会,能源的发展已成为全世界共同关注的话题,乙烷、二甲醚的燃烧热较大,可用作燃料。如图1表示乙烷、二甲醚燃烧过程中的能量变化。
请回答下列问题:
(1)a= 。
(2)乙烷的燃烧热为 。
(3)根据题图写出二甲醚完全燃烧时的热化学方程式: 。
Ⅱ.利用如图2装置测定中和热的实验步骤如下:
①用量筒量取50mL0.25ml/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55ml/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(4)大小烧杯中填充泡沫塑料的作用是 。
(5)倒入NaOH溶液的正确操作是 (从下列选出)。
A.一次迅速倒入 B.分三次少量倒入 C.沿玻璃棒缓慢倒入
(6)使硫酸与NaOH溶液混合均匀的正确操作是 。
化学键
C-H
C=C
C-C
H-H
键能E/kJ/ml
414.4
615.3
347.4
435.3
化学键
C—H
C—F
H—F
F—F
键能/(kJ·ml-1)
a
b
c
d
参考答案:
1.C
【分析】燃烧热是指在101 kPa时,1 ml纯物质完全燃烧生成指定产物时所放出的热量。
【详解】A.可燃物的物质的量不是1ml,其不等于燃烧热,A错误;
B.H2O的状态应为液态,B错误;
C.符合燃烧热的定义,热化学方程式中代表燃烧热,C正确;
D.燃烧热是指可燃物与氧气反应,其不等于燃烧热,D错误;
故选C。
2.D
【详解】A.测量中和热时,装置中填充碎泡沫塑料的作用是减少热量损失,使测量更准确,A正确;
B.已知: ,则NaOH稀溶液与稀醋酸生成1ml水,放出热量小于57.3kJ,,因为醋酸电离需要吸收热量,B正确;
C.已知: ,由于该反应放热,则1ml (g)和2ml (g)充分反应致使平衡正向移动,放出更多热量,放出热量小于akJ,C正确;
D. ,由于不是生成液态水,故不能表示甲烷燃烧热的热化学方程式,D错误;
答案选D。
3.A
【详解】A.的燃烧热是,则有:,故,A正确;
B.燃烧热是指1ml纯物质完全燃烧生成稳定的物质所放出的热量,故在、时,完全燃烧生成液态水,放出热量,则表示氢气燃烧热的热化学方程式为:,B错误;
C.在稀溶液中:;,由于浓硫酸稀释过程中将放出大量的热量,则若将含的浓硫酸与含的溶液混合生成1mlH2O,放出的热量大于,C错误;
D.、下,已知热化学方程式:,将和置于密闭容器中充分反应生成,由于该反应为可逆反应,0.5mlN2不能完全反应,则放热小于,D错误;
故答案为:A。
4.D
【详解】A.描述燃烧热时,用正值表示,碳的燃烧热为393.5kJ/ml,故A错误;
B.0.5ml和1.5ml置于密闭的容器中充分反应生成,放热19.3kJ,反应为可逆反应,而热化学方程式中的反应热为完全反应的能量变化,则,故B错误;
C.燃烧热是指1ml可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧必须生成液态水,故C错误;
D.的燃烧热是,为1mlCO燃烧生成二氧化碳的能量变化,则分解的热化学方程式为:,故D正确;
故选:D。
5.A
【详解】甲醇的燃烧热是1ml甲醇燃烧生成二氧化碳和液态水放出的热量,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,则1ml甲醇燃烧生成CO2和液态水时放热22.68kJ×32=725.76 kJ,表示甲醇燃烧热的热化学方程式是CH3OH(l)+O2(g)=CO2(g)+2H2O(l) ΔH=-725.8kJ/ml,故选A。
6.B
【详解】A.燃烧热对产物的要求是稳定状态,对水来说应为H2O(l),A不正确;
B.燃烧热是指1ml可燃物完全燃烧放出的热量,与实验时反应物的用量无关,所以25℃、101kPa时,1mlS和2mlS的燃烧热相等,B正确;
C.从热化学方程式S(s)+O2(g)=SO3(g) ∆H=-269.8kJ/ml可以看出,燃烧为放热反应,∆H小于0,所以硫生成SO3的反应热为-269.8kJ/ml,C不正确;
D.燃烧热都为正值,所以25℃、101kPa时,碳的燃烧热为393.5kJ/ml,D不正确;
故选B。
7.D
【详解】A.可燃物燃烧可以是完全燃烧也可以是不完全燃烧,而燃烧热必须是完全燃烧放出的热量,选项A错误;
B.燃烧热是1ml可燃物燃烧生成稳定氧化物放出的热量,一般H→H2O(l),C→CO2(g),S→SO2(g),选项B错误;
C.燃烧热是1ml可燃物燃烧生成稳定氧化物放出的热量,选项C错误;
D.时,纯物质完全燃烧生成指定产物(C元素变为CO2气体、H元素变为液态H2O等)时所放出的热量就是该物质的燃烧热,选项D正确。
答案选D。
8.D
【详解】A.CH3COOH为弱酸不完全电离,在与NaOH反应过程中会继续电离,电离吸热,则其ΔH不等于-57.3kJ•ml-1,故A错误;
B.燃烧为放热反应,则二氧化碳分解成CO和氧气为吸热反应,ΔH大于0,故B错误;
C.N2(g)性质很稳定,不能在氧气中燃烧,不存在燃烧热,故C错误;
D.ΔH只与反应物和生成物的能量高低有关,与反应条件无关,故D正确;
故选:D。
9.D
【详解】A.反应为可逆反应,进行不完全,放出热量小于196.64kJ,A错误;
B.中和热是在稀溶液中,强酸跟强碱发生中和反应生成1 ml液态水时所释放的热量;故表示中和热的热化学方程式为NaOH(aq)+H2SO4(aq)= Na2SO4(aq)+H2O(l) △H=-57.4kJ·ml-1,B错误;
C.燃烧热是在101 kPa时,1 ml物质完全燃烧生成稳定的氧化物时所放出的热量;反应中生成为气态水,C错误;
D.已知石墨转化为金刚石吸热,则说明石墨能量低于金刚石,故石墨比金刚石稳定,D正确;
故选D。
10.D
【详解】A.甲烷的燃烧热指在为25℃、101kPa时,1ml甲烷完全燃烧生成二氧化碳和液态水所放出的热量,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/ml,故A错误;
B.500℃、30MPa下,将0.5mlN2和1.5mlH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,由于该反应为可逆反应,1mlN2完全反应放热大于38.6kJ,则热化学反应方程式为:N2(g)+3H2(g)2NH3(g) △H<-38.6 kJ/ml,故B错误;
C.稀溶液中,酸跟碱发生中和反应生成1 ml液态水时所放出的热量叫做中和热,则稀H2SO4和NaOH溶液反应的中和热△H=-57.3kJ/ml,故C错误;
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则2mlH2完全燃烧生成液态水,放出571.6热量,反应的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/ml,故D正确;
故选D。
11. 393.5kJ/ml 石墨 HCl(aq)+NaOH(aq)=H2O(l)+NaCl(aq) △H= –57.3 kJ/ml △H3 < △H4
【分析】(1)根据盖斯定律将①+②可得碳燃烧热的热化学方程式,从而可以知道其燃烧热;物质具有能量越高,物质的稳定性越弱;
(2)反应③为稀的强酸溶液与稀的强碱溶液反应生成盐和水的反应;醋酸为弱酸,电离过程需要吸收热量,导致放热热量减少,结合焓变为负值判断。
【详解】(1) ① 2C(s)+O2(g)=2CO(g) △H1 = –221 kJ/ml
② CO(g)+1/2O2(g)=CO2 (g) △H2 = –283 kJ/ml
根据盖斯定律①+②可得:C(s)+O2(g)= CO2 (g) △H= –393.5 kJ/ml;
根据反应C(s,金刚石) = C(s,石墨) △H = –1.9 kJ/ml ,可以知道,该反应为放热反应,说明金刚石的能量高于石墨,则石墨的稳定性更大,
因此,本题正确答案是:393.5kJ/ml;石墨;
(2)稀溶液中H+(aq)+OH-(aq)=H2O(l) △H3 = –57.3 kJ/ml
表示稀的强酸与稀的强碱溶液反应的热化学方程式,如热化学方程式:HCl(aq)+NaOH(aq)=H2O(l)+NaCl(aq) △H= –57.3 kJ/ml;
稀醋酸与氢氧化钠稀溶液恰好反应的中和热为△H4,因为醋酸的电离吸热,则反应中放出热量减少,因为焓变为负值,则△H3>△H4,
因此,本题正确答案是:HCl(aq)+NaOH(aq)=H2O(l)+NaCl(aq) △H= –57.3 kJ/ml;△H3 < △H4。
12. C6H6(l)+O2(g)=6CO2(g)+3H2O(l)△H=-3 260.4 kJ/ml NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+H2O(l)△H=-57.3kJ/ml +125.6kJ/ml N2H4(g)+O2(g)=N2(g)+H2O(g) △H=-33.4kJ/ml
【详解】(1)1.00g C6H6(l)在O2中完全燃烧生成CO2(g)和H2O(l),放出41.8kJ的热量,则1mlC6H6(l)在氧气中完全燃烧放出的热量为41.8×78=3260.4kJ,因此C6H6(l)燃烧热的热化学方程式为C6H6(l)+O2(g)=6CO2(g)+3H2O(l)△H=-3 260.4 kJ/ml;
(2)1.00L 1.00ml/L H2SO4溶液与2.00L 1.00ml/L NaOH溶液完全反应,放出114.6kJ的热量,即生成2ml水放出114.6kJ的热量,则生成1ml水放出的热量为57.3kJ,则中和热的热化学方程式:NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+H2O(l)△H=-57.3kJ/ml;
(3)焓变=反应物总键能-生成物总键能= 6×414.4kJ/ml +347.4kJ/ml -(4×414.4kJ/ml +615.3kJ/ml +435.3kJ/ml)=+125.6kJ/ml;
(4)2.0g燃料肼(N2H4)的物质的量为,所以该反应的热化学方程式为 N2H4(g)+O2(g)=N2(g)+H2O(g) △H=-33.4kJ/ml。
【点睛】在25摄氏度,101 kPa时,1 ml可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热;在稀溶液中,强酸跟强碱发生中和反应生成1 ml液态水时所释放的热量叫做中和热。
13. > 催化剂 = CH3OH(1)+3/2O2(g)===CO2(g)+2H2O(1) ΔH=-725.76 kJ•ml-1 2NH3(g)+CO2(g)===CO(NH2)2(s)+H2O(l) ΔH=-87.0 kJ/ml
【详解】(1)①通过图中信息可知反应物总能量 生成物总能量,因此反应CH3OH(g)+H2O(g)===CO2(g)+3H2(g)的ΔH>0。②图中途径(Ⅱ)的活化能减小,因此条件是使用了催化剂,催化剂改变活化能,不能改变反应热,因此途径(Ⅰ)的反应热等于途径(Ⅱ)的反应热;③在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则1ml甲醇即32g甲醇完全放出的热量是22.68 kJ×32=725.76 kJ,由于在一定条件下,1ml可燃物完全燃烧生成稳定氧化物时所放出的热量是燃烧热,因此表示甲醇燃烧热的热化学方程式为CH3OH(1)+3/2O2(g)===CO2(g)+2H2O(1) ΔH=-725.76 kJ·ml-1。(2)已知:
①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/ml
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/ml
③H2O(l)===H2O(g) ΔH=+44.0 kJ/ml
则根据盖斯定律可知①+②-③即得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)===CO(NH2)2(s)+H2O(l) ΔH=-87.0 kJ/ml。
14.(1)C(s)+O2(g)=CO2(g)△H=﹣393.6 kJ/ml
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣200KJ•ml-1
【详解】(1)1g碳粉在氧气中完全燃烧放出的热量是32.8kJ,12g碳粉在氧气中完全燃烧并放出393.6kJ热量,则热化学方程式为:C(s)+O2(g)=CO2( g)△H=﹣393.6 kJ/ml。
(2)在25℃、101kPa下,2g甲烷燃烧生成CO2和液态水时放热25kJ,则16g甲烷完全燃烧生成二氧化碳和液态水放出的热量为8×25kJ=200kJ,则甲烷燃烧热的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣200kJ•ml﹣1。
15.(1)
(2)C6H12O6(s)+6O2(g) =6CO2(g)+6H2O(l) ΔH=-2 800 kJ·ml-1
(3)
(4)
(5)
【详解】(1)CO的燃烧热是1mlCO燃烧生成二氧化碳气体放出的能量,反应的,则的燃烧热是。
(2)葡萄糖的燃烧热是1ml葡萄糖燃烧生成二氧化碳气体和液态水放出的能量,葡萄糖的燃烧热是,则表示葡萄糖燃烧热的热化学方程式为C6H12O6(s)+6O2(g) =6CO2(g)+6H2O(l) ΔH=-2 800 kJ·ml-1;
(3)氢气的燃烧热为,表示1ml氢气燃烧生成液态水放出285KJ的能量,电解水的热化学方程式为;
(4)中和热是强酸和强碱反应生成1ml水放出的热量,中和反应的中和热为。则和盐酸反应表示中和热的热化学方程式为;
(5)乙硼烷(分子式)在氧气中燃烧,生成固态三氧化二硼和液态水,放出的热量,则1ml乙硼烷燃烧放热2165KJ,其热化学方程式为;
16. M < 2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)ΔH=-290kJ·ml-1
【分析】根据M、N能量高低,判断其稳定性;根据燃烧热的概念,判断a与燃烧热的关系;根据题中信息,写出其热化学方程式;据此解答。
【详解】(1)有机物M经过太阳光光照可转化成N,△H=+88.6kJ•ml-1,该过程是吸热反应,N暗处转化为M,是放热反应,M比N能量低,由能量越低越稳定,说明M稳定;答案为M。
(2)燃烧热是1ml物质完全燃烧生成稳定氧化物放出的热量,甲醇燃烧生成CO2(g)和H2(g)属于不完全燃烧,CH3OH(l)+O2(g)=CO2(g)+2H2(g)△H=-a kJ•ml-1,放出的热量小于燃烧热,故a<726.5;答案为<。
(3)有1ml Cl2参与反应时释放出145kJ热量,2ml氯气反应放热290kJ,反应的热化学方程式为2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•ml-1;答案为2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290kJ•ml-1。
17. 297kJ/ml S(s)+O2(g)===SO2(g) ΔH=-297 kJ·ml-1
【详解】根据题目信息,16g S 的物质的量为0.5ml,放出148.5KJ的热量,则1ml S 燃烧放热297 kJ,所以S的燃烧热为297kJ/ml,S燃烧生成二氧化硫,热化学方程式为S(s)+O2(g)===SO2(g) ΔH=-297 kJ·ml-1,故答案为:297kJ/ml;S(s)+O2(g)===SO2(g) ΔH=-297 kJ·ml-1;
18.CH4 (g)+ O2(g) =CO2(g) + 2H2O(l) △H=-990kJ/ml
【详解】燃烧热指1ml可燃物完全燃烧生成稳定的化合物所放出的热量,故CH4燃烧热的热化学方程式:CH4 (g)+ O2(g) =CO2(g) + 2H2O(l) △H=-990kJ/ml。
19. M < 2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)ΔH=-290kJ·ml-1 4a+4d-4b-4ckJ·ml-1
【分析】根据反应吸放热判断物质能量高低,进而判断物质的稳定性;根据盖斯定律书写热化学反应方程式并计算反应热。
【详解】(1)有机物M经过太阳光光照可转化成N:△H = +88.6kJml-1,该过程是吸热反应,N暗处转化为M,是放热反应,根据反应物的能量越低越稳定,可知M稳定,故答案:M。
(2)燃烧热是1ml物质完全燃烧生成稳定氧化物放出的热量。甲醇燃烧生成CO2(g)和 H2(g)属于不完全燃烧,放出的热量小于燃烧热,故答案为:<。
(3)由1 ml Cl2参与反应时释放出145kJ热量,2 ml氯气反应放热290 kJ,反应的热化学方程式为:2Cl2(g) +2H2O(g) +C(s)═4HCl(g)+CO2(g) △H= -290 kJml-1,故答案为:2Cl2(g) +2H2O(g)+C(s)═4HCl(g)+CO2(g) △H = -290kJml-1。
(4)由CH4(g)+4F2(g)=CF4(g)+4HF(g)反应可知,ΔH=反应物的总键能-生成物的总键能=(4a+4d-4b-4c) kJ ml-1,故答案为:(4a+4d-4b-4c) kJml-1。
20.49982.6kJ
【详解】1kg乙炔的物质的量为,由热化学方程式 可知,38.46ml乙炔完全燃烧放出的热量为38.46ml×=49982.6kJ。
21.(1)NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+H2O(l) △H=-57.3kJ/ml
(2)C
(3) 减少热量散失 用水将温度计上的液体冲掉,并擦干温度计或用蒸馏水清洗干净
(4)ab
(5) 偏小 氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ
【详解】(1)强酸、强碱的中和热数值为57.3kJ/ml,中和热是强酸和强碱的稀溶液完全反应生成1ml水放出的热量,稀硫酸和稀氢氧化钠溶液反应的热化学方程式为:H2SO4(aq)+NaOH(aq)═Na2SO4(aq)+H2O(l)△H=-57.3kJ/ml,故答案为: H2SO4(aq)+NaOH(aq)═Na2SO4(aq)+H2O(l)△H=-57.3kJ/ml;
(2)倒入NaOH溶液时,必须一次迅速的倒入,目的是减少热量的散失,不能分几次倒入NaOH溶液,否则会导致热量散失,影响测定结果;故选:C;
(3)A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃棒,两个小孔不能开得过大,如果孔太大则热量散失增多,引起更大的实验误差,故两孔不能开得过大,其原因是减少热量散失,由于测完酸或者碱的温度计继续测量碱或酸的温度时,沾在温度计上的酸或碱与第二次测量的碱或酸反应,导致溶液局部温度升高,带来实验误差,故反应需要测量温度,每次测量温度后都必须用水将温度计上的液体冲掉,并擦干温度计或用蒸馏水清洗干净,故答案为:减少热量散失;用水将温度计上的液体冲掉,并擦干温度计或用蒸馏水清洗干净;
(4)另取50mL HCl(0.1ml•L-1)溶液与50mL NaOH(0.1ml•L-1)溶液在小烧杯中进行中和反应,通过实验并计算可得中和热为54.8kJ/ml,上述实验数值与57.3kJ/ml有偏差,即使测量结果偏低,据此分析解题:
a、实验装置保温、隔热效果差,导致热量散失,则测量的最高温度偏低,导致测量结果偏低,a符合题意;
b、用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度,导致酸碱中和反应,放出热量,导致测量的HCl的温度偏高,则导致反应前的温度偏高,反应前后温度差偏低,导致测量结果偏低,b符合题意;
c、一次性把NaOH溶液倒入盛有盐酸的小烧杯中,此操作是正确操作,不会带来实验误差,c不合题意;
故答案为:ab;
(5)由于氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ,用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小,故答案为:偏小;氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ;
22. D 环形玻璃搅拌棒 确保盐酸被完全中和 C ΔH1=ΔH2<ΔH3 H2SO4与Ba(OH)2反应生成BaSO4沉淀,沉淀的生成热会影响反应的反应热
【分析】Ⅰ.根据中和热是强酸强碱稀溶液完全反应生成1ml水放出的热量,燃烧热1ml可燃物完全燃烧生成稳定的氧化物放出的热量,结合热化学方程式分析判断;
Ⅱ.中和热的测定实验中需要注意保温,防止热量的散失,影响测定结果的准确性,结合中和热的焓变是负值分析解答。
【详解】Ⅰ.A.由反应①可知,1ml碳燃烧生成CO放出的热量为110.5kJ,CO燃烧生成二氧化碳会继续放出热量,故1ml碳完全燃烧放出的热量大于110.5kJ,所以碳的燃烧热大于110.5kJ•ml-1,即碳的燃烧热△H<-110.5kJ•ml-1,故A错误;
B.反应热包含正负号,①的反应热为-221kJ•ml-1,故B错误;
C.中和热与酸的元数无关,所以稀硫酸与氢氧化钠反应的中和热ΔH=-57.3kJ•ml-1,故C错误;
D.在稀溶液中,酸跟碱发生中和反应生成1ml水时的反应热叫做中和热。20.0gNaOH的物质的量n===0.5ml,与稀盐酸完全中和生成0.5ml水,此时放出热量57.3kJ×= 28.65kJ,故D正确;
故选D;
Ⅱ.(1)根据图示,仪器a是环形玻璃搅拌棒,故答案为:环形玻璃搅拌棒;
(2)为了确保盐酸被完全中和,所用NaOH溶液要稍过量,故答案为:确保盐酸被完全中和;
(3)倒入氢氧化钠溶液时,必须一次迅速的倒入,目的是减少热量的散失,故选C;
(4)中和热是强酸强碱稀溶液完全反应生成1ml水放出的热量,一定量的稀氢氧化钠溶液、稀氢氧化钙溶液和1L 1ml•L-1的稀盐酸恰好完全反应放热57.3kJ;一水合氨是弱电解质,存在电离平衡,电离过程需要吸热,因此稀氨水和1L 1ml•L-1的稀盐酸恰好完全反应放热小于57.3kJ,反应焓变是负值,所以△H1=△H2<△H3,故答案为:△H1=△H2<△H3;
(5)硫酸与Ba(OH)2溶液反应除了生成水外,还生成了BaSO4沉淀,沉淀的生成热会影响反应的反应热,所以不能用Ba(OH)2溶液和硫酸代替NaOH溶液和盐酸测中和热,故答案为:硫酸与Ba(OH)2溶液反应生成BaSO4沉淀,沉淀的生成热会影响反应的反应热。
23.(1)
(2)-1560kJ·ml-1
(3)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-1455kJ·ml-1
(4)保温隔热,减少热量的散失
(5)A
(6)用套在温度计上的环形玻璃棒上下搅动
【详解】(1)由H原子守恒可知6a=2,则a=;
(2)1ml乙烷燃烧生成二氧化碳和液态水放出的热量为520kJ×3=1560kJ,则乙烷的燃烧热为ΔH=-1560kJ•ml-1;
(3)结合状态及焓变可知二甲醚完全燃烧时的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-485kJ•ml-1×3=-1455kJ•ml-1;
(4)中和热测定实验成败的关键是保温工作,在大小烧杯中填充泡沫塑料的作用是减少实验过程中的热量损失;
(5)倒入氢氧化钠溶液时,必须一次迅速的倒入,目的是减少热量的散失,不能分几次倒入氢氧化钠溶液,否则会导致热量散失,影响测定结果,故答案为:A;
(6)使硫酸与NaOH溶液混合均匀的正确操作是用套在温度计上的环形玻璃棒上下搅动。
人教版 (2019)选择性必修1第一节 反应热课时训练: 这是一份人教版 (2019)选择性必修1第一节 反应热课时训练,共21页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第一章 化学反应的热效应第一节 反应热课时训练: 这是一份高中化学人教版 (2019)选择性必修1第一章 化学反应的热效应第一节 反应热课时训练,共21页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第一节 反应热巩固练习: 这是一份高中化学人教版 (2019)选择性必修1第一节 反应热巩固练习,共5页。试卷主要包含了 反应热和焓变, 实验步骤及注意事项, 数据处理等内容,欢迎下载使用。