突破06 有机化学实验专题训练(六)-备战2023年高考化学《有机化学实验》专题突破系列
展开有机化学实验专题训练(六)
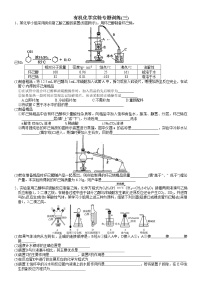
1、苯甲酸甲酯是一种重要的工业原料,某化学小组采用如右图装置,以苯甲酸、甲醇为原料制取苯甲酸甲酯。有关物质的物理性质见下表所示:
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
熔点/℃ | 122.4 | -97 | -12.3 |
沸点/℃ | 249 | 64.3 | 199.6 |
密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
水溶性 | 微溶 | 互溶 | 不溶 |
Ⅰ、合成苯甲酸甲酯粗产品:在圆底烧瓶中加入0.1mol苯甲酸和0.4mol 甲醇,再小心加入 3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品
(1)甲装置的作用是: ;冷却水从 (填“a”或“b”)口进入)
(2)化学小组在实验中用过量的反应物甲醇,其理由是
Ⅱ.粗产品的精制:苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制
(1)试剂1可以是 ,作用是
A.稀硫酸 B.碳酸钠溶液 C. 乙醇
(2)操作2中,收集产品时,控制的温度应在 ℃左右
(3)实验制得的苯甲酸甲酯精品质量为10g,则苯甲酸的转化率为 (结果保留三位有效数字)
(4)本实验制得的苯甲酸甲酯的产量低于理论产量,可能的原因是
A.蒸馏时从100℃开始收集产品 B.甲醇用量多了 C.制备粗品时苯甲酸被蒸出
2、1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2二溴乙烷。其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴。可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。(夹持装置已略去)
有关数据列表如下:
填写下列空白:
(1)A的仪器名称是_________________________
(2)安全瓶B可以防止倒吸,还可以检查实验进行时导管是否发生堵塞。请写出发生堵塞时瓶B中的现象____
________________________________________
(3)A中发生反应的化学方程式为____________________________________________;D中发生反应的化学方程式为____________________________________
(4)在装置C中应加入________(填字母),其目的是吸收反应中可能生成的酸性气体
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)若产物中有少量副产物乙醚,可用_______________(填操作名称)的方法除去
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是________________________________
3、邻苯二甲酸丁基月桂酯是一种淡黄色透明油状液体,密度约0.97g/cm3,常用作聚氯乙烯等树脂的增塑剂。工业上生产原理和工艺流程如下:
有关物质的物理性质见下表:
化合物 | 溶解性 | 熔点 | 沸点 |
邻苯二甲酸酐 | 微溶于冷水、乙醚,易溶于热苯、乙醇、乙酸 | 131.6℃ | 295℃ |
正丁醇 | 微溶于水,溶于乙醇、醚、多数有机溶剂 | -88.9℃ | 117.5℃ |
月桂醇 | 不溶于水,溶于醇、醚 | 24 | 259℃ |
邻苯二甲酸丁基月桂酯 | 不溶于水,溶于多数有机溶剂 | 不祥 | 202~210℃ |
某实验小组的同学模拟工业生产的工艺流程,用右图所示装置制取少量邻苯二甲酸丁基月桂酯,图中夹持和加热装置已略去。主要操作步骤如下:
①向三颈烧瓶内加入30 g 邻苯二甲酸酐、16 g 正丁醇以及少量浓硫酸
②搅拌,升温至105 ℃,持续搅拌反应1小时
③冷却至室温,加入40 g 月桂醇,升温至160 ℃,搅拌、保温至反应结束
④冷却至室温,将反应混合物倒出
⑤通过工艺流程中的操作X,得到粗产品
请回答下列问题:
(1)仪器C的名称___________。冷凝管中冷水应从___________进
(2)步骤③中判断反应已结束的方法是___________
(3)步骤⑤中操作X可除去少量未反应的邻苯二甲酸酐及正丁醇,操作X包括___________
(4)工艺流程中减压蒸馏的目的是___________
(5)实验结果表明步骤②、③产率都比较高,原因是___________
4、冬青油又叫水杨酸甲酯,是一种重要的有机合成原料。某化学小组用水杨酸()和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
Ⅰ、如图,在三颈烧瓶中加入13.8g (0.1mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时
Ⅱ、待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ、将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯9.12g
常用物理常数
名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
请根据以上信息回答下列问题:
(1)仪器A的名称是 ,加入沸石的作用是 ,若加热后发现未加沸石,应采取的正确方法是
(2)制备水杨酸甲酯时,最合适的加热方法是
(3)实验中加入甲苯对合成水杨酸甲酯的作用是
(4)反应结束后,分离出甲醇采用的方法是
(5)实验中加入无水硫酸镁的作用是
(6)本实验的产率为 (保留两位有效数字)
5、实验室制备苯甲酸乙酯的反应装置示意图和有关数据如下:
名称 | 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水中溶解性 |
苯甲酸 | 122 | 1.266 | 249 | 微溶 |
乙醇 | 46 | 0.789 | 78.3 | 溶 |
苯甲酸乙酯 | 150 | 1.045 | 213 | 难溶 |
环己烷 | 84 | 0.779 | 80.8 | 难溶 |
环己烷、乙醇和水可形成共沸物,其混合物沸点为62.1 ℃。
合成反应:向圆底烧瓶中加入6.1 g苯甲酸、20 mL无水乙醇、25 mL环己烷和2片碎瓷片,搅拌后再加入2 mL浓硫酸。按图组装好仪器后,水浴加热回流1.5小时
分离提纯:继续水浴加热蒸出多余乙醇和环己烷,经分水器放出。剩余物质倒入盛有60 mL冷水的烧杯中,依次用碳酸钠、无水氯化钙处理后,再蒸馏纯化,收集210~213 ℃的馏分,得产品5.0 g
回答下列问题:
(1)仪器A的名称为________,冷却水应从________(填“a”或“b”)口流出
(2)加入环己烷的目的为____________________________________________
(3)合成反应中,分水器中会出现分层现象,且下层液体逐渐增多,当下层液体高度距分水器支管约2 cm时开启活塞放出少量下层液体。该操作的目的为_____________________________________________________
(4)实验中加入碳酸钠的目的为____________________________________________;经碳酸钠处理后,若粗产品与水分层不清,可采取的措施为__________________________________________________
(5)在该实验中,圆底烧瓶的容积最适合的是__________
A.50 mL B.100 mL C.200 mL D.300 mL
(6)本实验的产率为____________________
6、苯佐卡因(对氨基苯甲酸乙酯)常用于创面、溃疡面及痔疮的镇痛。在实验室用对氨基苯甲酸()与乙醇反应合成苯佐卡因,有关数据和实验装置图如下:
| 相对分子质量 | 密度(g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
乙醇 | 46 | 0.79 | -114.3 | 78.5 | 与水任意比互溶 |
对氨基苯甲酸 | 137 | 1.374 | 188 | 399.9 | 微溶于水,易溶于乙醇 |
对氨基苯甲酸乙酯 | 165 | 1.039 | 90 | 172 | 难溶于水,易溶于醇、醚类 |
产品合成:在250mL圆底烧瓶中加入8.2g对氨基苯甲酸(0.06mol) 和80mL无水乙醇(约1.4mol),振荡溶解,将烧瓶置于冰水浴并加入10mL浓硫酸,将反应混合物在80℃水浴中加热回流1h,并不时振荡
分离提纯:冷却后将反应物转移到400mL烧杯中,分批加入10%Na2CO3溶液直至pH=9,转移至分液漏斗中,用乙醚(密度0.714g·cm-3) 分两次萃取,并向醚层加入无水硫酸镁,蒸出醚层,冷却结晶,最终得到产物3.3g
(1)仪器A的名称为__________,在合成反应进行之前,圆底烧瓶中还应加入适量的___________
(2) 该合成反应的化学方程式是__________________________
(3)将烧瓶置于冰水浴中的目的是_____________________
(4)分液漏斗使用之前必须进行的操作是____________,乙醚层位于_______(填“上层”或“下层”);分离提纯操作加入无水硫酸镁的作用是_________
(5)合成反应中加入远过量的乙醇目的是_________;分离提纯过程中加入10%Na2CO3溶液的作用是_________
(6)本实验中苯佐卡因的产率为_________(保留3位有效数字)。该反应产率较低的原因是_________
a.浓硫酸具有强氧化性和脱水性,导致副反应多 b.催化剂加入量不足
c.产品难溶于水,易溶于乙醇、乙醚 d.酯化反应是可逆反应
7、某化学小组以苯甲酸为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
Ⅰ、合成苯甲酸甲酯粗产品
在圆底烧瓶中加入9.6ml(密度约为1.27g.ml-1)苯甲酸和20mL甲醇(密度约0.79g·mL﹣1),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品
(1)加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作时
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)浓硫酸的作用是 混合液体时最后加入浓硫酸的理由:
(3)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点最好采用装置 (填“甲”或“乙”或“丙”)
Ⅱ、粗产品的精制
(4)苯甲酸甲酯粗产品中含有少量甲醇、硫酸、苯甲酸和水,现拟用下列流程进行精制,请根据流程图写出操作方法的名称,操作Ⅱ
(5)不能用NaOH溶液代替饱和碳酸钠溶液的原因是
(6)列式计算,苯甲酸甲酯的产率是
8、苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯。苯甲酸乙酯(密度1.05 g·cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等。制备苯甲酸乙酯的过程如下:
制备粗产品:如图所示装置中,于50 mL圆底烧瓶中加入8.0 g苯甲酸(Mr=122)、20 mL乙醇(Mr=46,密度0.79 g·cm-3)、15 mL环己烷、3 mL浓硫酸,摇匀,加沸石。在分水器中加水,接通冷凝水,水浴回流约2 h,反应基本完成。记录体积,继续蒸出多余环己烷和醇(从分水器中放出)
粗产品纯化:加水30 mL,分批加入固体NaHCO3,分液,然后水层用20 mL石油醚分两次萃取。合并有机层,用无水硫酸镁干燥。回收石油醚,加热精馏,收集210~213 ℃馏分
相关数据如下:
沸点(℃,1 atm) | ||||||
苯甲酸 | 苯甲酸乙酯 | 石油醚 | 水 | 乙醇 | 环己烷 | 共沸物(环己烷—水—乙醇) |
249 | 212.6 | 40~80 | 100 | 78.3 | 80.75 | 62.6 |
根据以上信息和装置图回答下述实验室制备有关问题:
(1)写出制备苯甲酸乙酯反应的化学方程式______________________________________,仪器a的名称______________,b口为冷凝水的_____________(填“进水口”或“出水口”)
(2)请说出在本实验中可以采取的能提高苯甲酸乙酯产率的方法________________________(写出任意一种即可)
(3)如何利用实验现象判断反应已基本完成______________________________________
(4)固体NaHCO3的作用__________________________________,加入固体NaHCO3时的实验操作所用到的主要玻璃仪器为______________
(5)经精馏得210~213℃馏分7.0 mL,则实验中苯甲酸乙酯的产率为__________
9、某实验小组探究制取丙烯酸甲酯的最佳实验条件过程中如下所示,回答有关问题:
Ⅰ、实验原理
(1)制备丙烯酸甲酯的化学反应方程式为________________________
Ⅱ、实验步骤
(2)上述反应装置图中存在的一处错误是_________________________
(3)①按题所示组装仪器,加入已实现混合均匀的反应物(其混合的顺序和操作为_________________________
________________________________________),然后加热回流。反应生成的水以共沸物形式蒸馏出来,冷凝后收集于分水器下层,上层有机物积至分水器支管时返回烧瓶,从化学平衡移动原理分子使用分水器的目的___________________________________________________
②充分反应后,冷却,向混合液中加入_________溶液洗至中性
③分液,取______层油状液体,再用无水Na2SO4干燥后蒸馏,收集馏分
Ⅲ、实验条件探究:小组同学经过多次实验,得到如下实验数据
同一反应时间 | 同一反应温度 | ||||
反应温度/℃ | 转化率(%) | 选择性(%) | 反应时间/h | 转化率(%) | 选择(%) |
40 | 77.8 | 100 | 2 | 80.2 | 100 |
60 | 92.3 | 100 | 3 | 87.8 | 100 |
80 | 92.6 | 100 | 4 | 92.3 | 100 |
130 | 94.5 | 88.7 | 6 | 93.0 | 100 |
选择性100%表示反应生成的产物是丙烯酸乙酯和水 | |||||
(4)根据表中数据,该反应的最佳反应条件是_________
A. 120℃,4h B. 80℃,2h C. 60℃,4h D. 40℃,3h
(5)当反应温度达到较高温度后,反应选择性降低的原因可能为_____________________________________
10、苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫
酸的先后顺序是
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至
130 ℃继续反应。在装置中,仪器b的作用是 ;仪器c
的名称是 ,其作用是 ,
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 ,
下列仪器中可用于分离苯乙酸粗品的是
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸的产率
是
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉
淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
【有机化学实验专题训练(六)】答案
1、Ⅰ (1)冷凝回流(2分) b (1分)
(2)该合成反应是可逆反应,甲醇比苯甲酸价廉,且甲醇沸点低,易损失,增加甲醇投料量提高产率或苯甲酸的转化率 (2分)
Ⅱ (1)B (2分) 洗去苯甲酸甲酯中过量的酸(2分)
(2)199.6 (2分)
(3)73.5% (2分)
(4)C (2分)
2、(1)三颈烧瓶 或答圆底烧瓶、三口瓶都可
(2)B中水面会下降,玻璃管中的水柱会上升,甚至溢出
(3)CH3CH2OHCH2=CH2↑+H2O CH2=CH2+Br2→CH2BrCH2Br
(4)c 蒸馏
(5)1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使导管堵塞
3、(1)三颈瓶;A;
(2)分水器中的水不再增加;
(3)先用饱和碳酸钠洗涤、分液,再用蒸馏水洗涤、分液(洗涤、分液);
(4)降低沸点,防止高温下发生副反应,致使产品不纯;
(5)生成的水蒸出冷凝成液态后通过分水器从体系中分离出去,促进反应
(6)2、4、5、2、4、1、4
4、(1)冷凝管 防止暴沸 停止加热,待冷却后加入
(2)水浴加热
(3)加入甲苯易将水蒸出,使平衡向右移动,从而提高反应的产率
(4)蒸馏或水洗分液
(5)除水或干燥
(6)60%
5、(1)球形冷凝管 b
(2)在较低温度下除去产物水,提高产率
(3)确保乙醇和环己烷及时返回反应体系而下层水不会回流到体系中
(4)中和苯甲酸和硫酸 加氯化钠进行盐析
(5)B
(6)66.7%
6、(1)球形冷凝管 沸石(或碎瓷片)
(2)
(3)散热降温,减少副反应,减少乙醇挥发损失
(4)检查是否漏液 上层 干燥吸水
(5)作溶剂,提高对氨基苯甲酸的转化率 中和过量的浓硫酸和调节pH
(6)33.3%(或33.4%) a d
7、(1)防止暴沸; B
(2)催化剂、吸水剂;浓硫酸密度较大,且与苯甲酸和甲醇混合放出大量的热,甲醇易挥发
(3) 乙
(4)蒸馏
(5)苯甲酸甲酯在碱性条件下水解
(6)65%
8、(1)H2O (球形)冷凝管 进水口
(2)加入环己烷形成水—乙醇—环己烷三元共沸物
分离反应过程中生成的水(或加过量乙醇 或使用分水器及时分离生成的水)
(3)加热回流至分水器中水位不再上升
(4)中和硫酸和未反应的苯甲酸 分液漏斗
(5)74.7%
9、(1)CH2=CHCOOH+HOCH3CH2=CHCOOCH3+H2O
(2)冷凝管应从下口进水,上口出水
(3)①先加入丙烯酸,在加入浓硫酸,边加边搅拌,冷却后,再加入甲醇
②将产物水及时从分离体系内分离出来,同时可减少反应物的流失,从而造成平衡正向移动
③饱和Na2CO3溶液 上层
(4)C
(5)发生了副反应。甲醇脱水生成了甲醚,有机物脱水碳化等
10、(1)先加水,再加浓硫酸(1分)
(2)滴加苯乙腈(1分) 球形冷凝管(1分) 回流(或使气化的反应液冷凝)(1分)便于苯乙酸析出(2分)BCE(全选对2分)
(3)重结晶(1分) 95%(1分)
(4)取少量洗涤液、加入稀硝酸、再加AgNO3溶液、无白色混浊出现(2分)
(5)增大苯乙酸溶解度,便于充分反应(2分)
突破10 有机化学实验专题复习讲义(三)-备战2023年高考化学《有机化学实验》专题突破系列: 这是一份突破10 有机化学实验专题复习讲义(三)-备战2023年高考化学《有机化学实验》专题突破系列,共8页。试卷主要包含了教材中五大制备型实验回顾,两大检验性实验,有机物的鉴别常用试剂,有机物的分离与提纯的方法,有机实验的八项注意,熟悉有机物制取中的典型装置图,有机物制备实验题的解题模板等内容,欢迎下载使用。
突破07 有机化学实验专题训练(七)-备战2023年高考化学《有机化学实验》专题突破系列: 这是一份突破07 有机化学实验专题训练(七)-备战2023年高考化学《有机化学实验》专题突破系列,共5页。试卷主要包含了CaO等内容,欢迎下载使用。
突破05 有机化学实验专题训练(五)-备战2023年高考化学《有机化学实验》专题突破系列: 这是一份突破05 有机化学实验专题训练(五)-备战2023年高考化学《有机化学实验》专题突破系列,共8页。试卷主要包含了间溴苯甲醛,是香料,乙酸异戊酯常作为配制香蕉等内容,欢迎下载使用。