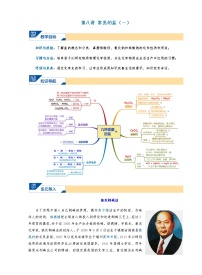
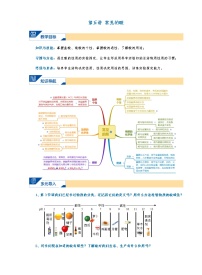
9.常见的盐(二)_2021年浙教版科学准九年级上学期暑假讲义(word,无答案)
展开第九讲 常见的盐(二)
知识与技能:掌握盐的通性,掌握复分解反应的概念和方程式的书写规则,了解不同化肥在农 业上的应用,掌握粗盐提纯的方法;
习惯与方法:通过粗盐的提纯,让学生能够开发思维,培养思考问题的全面性;
思维与素养:通过提纯实验的训练,寻找资源解决问题,培养学生在处理事务上面的思考能力。
1.坦桑尼亚北部有个著名的湖泊——纳特龙湖,被人称作“冥河”。湖边有许多天然形成且保存完好的动物标本,其原因则是湖水中有高浓度的碳酸钠,厨房里常见的碳酸钠为何也有这么大的危险性?
2.从来没干过农业的王大锤承包了一块田种西瓜。为了让西瓜长得更好卖得更多,大锤把购买来的氯化铵、磷酸钙、碳酸钾一股脑地撒到瓜田。接下来的几天,他总能闻到一股浓重的刺激气味,西瓜没过几天也焦枯了。大锤因此赔惨了。他做错了什么?
知识点一、盐的通性
盐的通性
(1)酸+盐 → 新酸+新盐
如:Na2CO3 + 2HCl==== 2NaCl + H2O + CO2↑ CaCO3 + 2HCl==== __________________
BaCl2 + H2SO4===___________________ HCl + AgNO3===_____________________
(2)可溶碱+可溶盐→新碱+新盐
如:Na2CO3 + Ca(OH)2 ==== CaCO3↓+ 2NaOH Na2CO3 + Ba(OH)2 ==== ______________
2NaOH + CuSO4 === __________________ 3NaOH + FeCl3 ==== ________________
(3)可溶盐+可溶盐→新盐1+新盐2
如:NaCl + AgNO3 ==== AgCl↓ + NaNO3 Na2SO4 + BaCl2 ==== ________________
Na2CO3 + CaCl2 ==== _________________ NH4Cl + AgNO3 ==== ________________
(4)金属+可溶盐→新金属+新盐(镁>铝>锌>铁>氢>铜>银)
如:Fe + CuSO4 ==== FeSO4 + Cu
知识点二、复分解反应
(1)复分解反应的概念:所谓复分解反应,即由两种化合物互相交换成分生成另外两种化合 物的反应。
这类反应可表示为:AB+CD=AD+CB。
(2)复分解反应的条件:
①生成物必须有沉淀或水或气体生成,否则不反应。
例1:2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O 能反应,有水生成。
例2:Na2CO3+K2SO4≠K2CO3+Na2SO4 不反应,既没有沉淀物、水生成也没有气体生成。
②除生成物必须满足条件外,反应物也有一定要求的
A.碱与盐反应,反应物必须都可溶。
例3:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH 能反应,因为反应物都可溶,且生成物中有沉淀。
例4:CaCO3+Fe(OH)2≠FeCO3+Ca(OH)2 K2CO3+Cu(OH)2≠2KOH+CuCO3 不反应,虽然好像有沉淀 物生成,但是反应物都不溶或不都溶。
B.盐与盐的反应,反应物必须都可溶.
例7:Na2CO3+CaCl2=CaCO3↓+2NaCl 能反应,因为反应物都可溶,且有沉淀物生成。
例8:BaCO3+ZnSO4≠BaSO4+ZnCO3 CaCO3+2AgCl≠CaCl2 +Ag2 CO3 两个化学方程式,好像都 有沉淀物生成,但两个化学方程式的反应物都不溶或有一种化合物不溶,所以都不反应。
C.常见的酸与盐的反应,这类反应比较复杂,初中阶段只要求记住,碳酸盐与常见的酸都能反 应,其他盐则要求可溶且生成物中要有气体、沉淀或水。
例10: H2SO4+BaCO3=BaSO4↓+H2O+CO2↑ 能反应,生成物,反应物都符合要求。
例11: 2HCl+BaSO4≠H2SO4+BaCl2 H2SO4+2KCl≠2HCl+K2SO4 前一化学反应式中反应物的 BaSO4不溶,所以不反应。后一化学方程式,反应物虽都可溶,但生成物不合要求,因 此也都不反应。
(3)常见酸、碱和盐的溶解性
由于复分解反应能否发生和反应物与生成物的溶解性有很大关系,所以我们需要学会并 牢记常见物质的溶解性。
阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
H+ | / | 溶、挥 | 溶、挥 | 溶 | 溶、挥 |
NH4+ | 溶 | 溶 | 溶 | 溶 | 溶 |
K+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
Mg2+ | 不 | 溶 | 溶 | 溶 | 微 |
Al3+ | 不 | 溶 | 溶 | 溶 | — |
Mn2+ | 不 | 溶 | 溶 | 溶 | 不 |
Zn2+ | 不 | 溶 | 溶 | 溶 | 不 |
Fe3+ | 不 | 溶 | 溶 | 溶 | 不 |
Fe2+ | 不 | 溶 | 溶 | 溶 | — |
Cu2+ | 不 | 溶 | 溶 | 溶 | 不 |
Ag+ | — | 溶 | 不 | 微 | 不 |
速记口诀:
硝酸盐遇水影无踪,碳酸只溶钾钠铵
氯化物不溶氯化银,硫酸盐不溶硫酸钡
碱中只溶钾钠铵钡(钙微溶)
氢氧化钙、硫酸钙、碳酸镁和硫酸银,
微溶于水记清楚,微溶也把沉淀生。
复分解反应的方向:离子间的相互结合,生成沉淀或气体或水。
最终结果是使得溶液中的离子减少。
学以致用:
判断以下物质能否反应,若能反应,写出化学方程式。不能反应的说明原因。
判断方法:第一步——确定反应物的类型,反应物是否满足溶解性要求;
第二部——“换换看”,看能否生成气体、沉淀或水。
①CuO+Ba(OH)2 ______________________ ②SO2+ HNO3 _______________________
③2Fe(OH)3+3MgCl2 ______________________ ④Na2CO3+CaCl2 ______________________
⑤BaCO3+2HCl ______________________ ⑥Ba(OH)2+H2SO4 _____________________
⑦NaOH+BaCl2 ______________________ ⑧2NaCl+Cu(NO3)2 _____________________
⑨AgNO3+ BaCl2 ______________________ ⑩KCl + MgSO4 ______________________
⑪FeCl3+NaOH ______________________ ⑫NH4Cl+ZnSO4 ______________________
⑬NaCl+Cu(OH)2 ______________________ ⑭CaCO3+NaCl ______________________
⑮NH4Cl+NaOH ______________________
互动讨论:
赵刚学习复分解反应后,对王强说:“复分解反应就是有酸、碱、盐参加的反应”。王强说:“对,有气体、沉淀或水生成的反应也一定是复分解反应”。他俩说得对吗?若不同意,请你各举一个例子推翻他们的观点。
知识点三、盐和化肥
1 .常见的化肥:
(1)氮肥(铵盐为主,还包括硝酸盐和尿素CO(NH2)2)
作用:能促使农作物的茎叶生长茂盛,含有组成叶绿素的重要元素
(2)磷肥(主要是磷酸盐)
作用:促进农作物要系发达,增强吸收养分和抗寒抗旱能力,促进作物穗数增多,籽粒饱 满等。
(3)钾肥
作用:促进农作物生长旺盛,茎杆粗壮,增强抗病虫害能力,促进糖和淀粉的生成。
(4)复合肥(含N、P、K元素中的两种或三种,如KNO3、KH2PO4、NH4H2PO4)
作用:具有氮肥、磷肥、钾肥的多种功能
2 .铵根(NH4+)离子的检验
取样品,加适量熟石灰研磨(或加入氢氧化钠溶液微热),有刺激性气味(氨味)气体产生,用湿润的红色石蕊试纸检验,试纸变蓝,则样品中有NH4+。
如:2NH4Cl + Ca(OH)2 === CaCl2 + 2NH3↑ + 2H2O
互动讨论:以上知识说明铵态氮肥不能和哪类物质存放在一起或者共同使用?你现在能解释王大锤的瓜苗为什么都枯死了吗?
知识点四、粗盐的提纯二
在八年级上学期学习过用溶解、过滤、蒸发结晶的方法对粗盐进行提纯,但是只能除去不溶性的杂质,在得到的盐中还有可溶性的杂质,如氯化镁、氯化钙、硫酸钠等。如何设计实验除去这些可溶性的杂质呢?
除杂的原则:“不增”、“不减”、“易分离”
想除去NaCl中的MgCl2可以用 想除去NaCl中的CaCl2可以用
想除去NaCl中的Na2CO3可以用
讨论:为了除恶务尽,在这个过程中要注意什么?可能引发其他的什么问题?怎样解决呢?
精熟讲授① 化肥对提高农作物的产量有重要作用。下列有关化肥的说法,不正确的是( )
A.长期使用化肥会导致土壤板结,故提倡农家肥与化肥综合施用
B.草木灰是一种农家肥,可以促进植物茎秆强壮
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
高效演练1-1 小明家的芹菜茎杆细弱,施肥可免其倒伏,他应施加的化肥是( )
A.KOH B.Ca3(PO4)2
C.KNO3 D.CO(NH2)2
精熟讲授② 对于反应,下列分析中正确的是( )
A.X可能是酸 B.X和Y的相对分子质量之差为18
C.X可能是或 D.Y可能是或
高效演练2-1 常温下,下列各组物质中,Y既能与X反应又能与Z反应的是(排除法)( )
A.①③ B.②③ C.①④ D.②④
精熟讲授③ 下表是某活动设计的4个实验方案,其中方案一、方案二都合理的是( )
高效演练3-1 小金完成了图示实验①②③,下列判断正确的是( )
A.实验①中石灰水有剩余 B.实验③中所得溶液中可能含有Ca(OH)2
C.实验③中没有明显现象 D.实验③所得溶液中一定含CaCl2和NaCl
精熟讲授① 现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加碳酸钠溶液质量为a~cg时,溶液中发生反应为
B.滴加碳酸钠溶液质量至bg时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至cg时,溶液呈中性
高效演练1-1 某固体可能含有NH4+、Cu2+、Na+、Cl﹣、CO32﹣、SO42﹣中的几种离子,取等质量的两份该固体进行如下实验(不考虑盐类的水解及水的电离);下列说法正确的是( )
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生0.51gNH3(标准状况)。
A.该固体中一定含有NH4+、CO32﹣、SO42﹣、Na+ B.该固体中一定没有Cu2+、Cl﹣、Na+
C.该固体中只含有NH4+、CO32﹣、SO42﹣、Cl﹣ D.根据以上实验,无法确定该固体中有Na+
高效演练1-2 某固体可能由MgC12、NaOH、BaC12、Na2SO4中的一种或多种组成。取少量该固体与烧杯中,向烧杯中加入足量水搅拌后,观察到有白色不溶物存在;再向烧杯中滴加酸溶液。根据加酸过程中观察到的现象绘制如图图像,结合图像判断下列说法合理的是( )
A.白色不溶物可能为Mg(OH)2或BaSO4
B.原固体中可能含有三种溶质
C.加水后得到的液体中可能含有OH-
D.酸溶液一定不是稀H2SO4
高效演练1-3 用10g10%的硫酸和10g10%的氢氧化钠溶液混合后,向混合溶液中加入下列物质,能发生反应的是( )
①CuSO4 ②BaCl2 ③MgSO4 ④FeCl3
A.② B.①②③④ C.①② D.①②③
精熟讲授② 尿素[化学式为 CO(NH2)2]是常用的化肥,下图为制取尿素的反应微观示意图。
(1)向土壤中施加尿素,对农作物生长所起的主要作用是_____(填选项字母)。
A.增强抗寒抗旱能力 B.使枝叶浓绿茂盛 C.增强抗倒伏能力
(2)写出A和B在一定条件下反应生成C和D的化学方程式_______________________。
高效演练2-1 小明家是种植蔬菜的专业户,他学习了化学后知道:施用适量氮肥可以使种植的蔬菜叶色浓绿。
(1)下列属于氮肥的是__________(填字母序号)。
A.碳酸氢铵(NH4HCO3) B.硫酸钾(K2SO4) C.磷矿粉[Ca3(PO4)2]
(2)氯化铵(NH4Cl)与氢氧化钠溶液混合加热,生成了氯化钠、水和有刺激性气味的氨气(NH3), 该反应可以用于铵态氮肥的检验,请写出该反应的化学方程式:______________________。 因此,铵态氮肥不能和__________物质混合使用,否则会降低肥效。
精熟讲授③ 通过海水晒制可得粗盐,粗盐中除外,还含有、、以及泥沙等杂质。以下是一种由粗盐制备精盐的实验方案流程图:
分析该流程图,回答下列问题:
(1)试剂X为______(填写化学式)。
(2)加适量溶液的目的是______。
(3)选择除杂的试剂不能用KOH代替溶液,理由是______。
高效演练3-1盐化工是一项重点产业,绿色应用是化工生产的发展方向。为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。回答下列问题:
(1)实验I中加入试剂A除去的杂质是__________;
(2)实验Ⅱ中加入的试剂B是__________溶液:
(3)滤液②中除Na+和Cl-外,还含有的离子是__________(填离子符号);
(4)实验Ⅲ中发生中和反应的化学方程式是__________________________________________。
精熟讲授① 高效演练3-1 研究性学习:探究实验室中久置的NaOH的变质程度
研究方案:先称取13.3g的NaOH样品(杂质为),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生在CO2的质量测定Na2CO3的质量。从而进一步确定样品中NaOH的变质程度。
解决方案:实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。填写下表:(计算结果保留小数点后一位)
Na2CO3的质量/g | ________________________________________ |
变质NaOH的质量/g | ________________________________________ |
NaOH的变质程度(用质量分数表示) | ________________________________________ |
注:变质程度是指变质的NaOH质量占未变质时NaOH的总质量的质量分数。
继续探究:求实验过程中与NaOH反应所用盐酸的质量。
发现问题:根据“与NaOH反应所用盐酸的质量”,对照图像,你发现了什么问题?
高效演练1-1 我国西北地区有很多咸水湖,其中最大的是柴达木盆地的察尔汗盐池。某盐湖附 近的农民通过“冬天捞碱,豆天晒盐”获得大量湖盐。小伟取该湖盐样品进行探究:
(提出问题)该湖盐样品的成分是什么?
(查阅资料)冬天捞碱的“碱”指Na2CO3,夏天晒盐的“盐”指NaCl。
(猜想与假设)猜想一:Na2CO3猜想二:NaCl 猜想三:Na2CO3和NaCl。
(实验探究)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | 猜想_____不成立 |
实验二 | 向实验一所得的溶液中加入适量的_____ | ______________________ | 猜想三成立 |
(拓展延伸)为了进一步确定该湖盐样品中Na2CO3的质量分数,小伟再取该湖盐样品20.00g 做了如图所示的补充实验。
(1)把表格中三处横线处填写完整
(2)反应结束之后继续通入空气的目的是_____________________。
(3)E装置的作用是_____________。
(4)实验结束后测得D装置增重0.88g,则湖盐样品中Na2CO3的质量分数为______%
质量的块状CaCO3和粉末状Na2CO3,分别与足量等质量分数的盐酸充分反应。根据 实验测定:其中粉末状Na2CO3与盐酸反应产生CO2的质量随反应时间变化如图所示。请在图中画出块状CaCO3与盐酸反应产生CO2的质量随反应时间变化大致曲线,并用科学原理加以解释。
14.表格型化学计算_2021年浙教版科学准九年级上学期暑假讲义(word,无答案): 这是一份14.表格型化学计算_2021年浙教版科学准九年级上学期暑假讲义(word,无答案),共10页。学案主要包含了有关化学方程式计算的要点归纳,表格型化学计算等内容,欢迎下载使用。
7.常见的碱(二)_2021年浙教版科学准九年级上学期暑假讲义(word,无答案): 这是一份7.常见的碱(二)_2021年浙教版科学准九年级上学期暑假讲义(word,无答案),共11页。学案主要包含了氢氧化钠,氢氧化钙,氢氧化钠变质探究等内容,欢迎下载使用。
11.离子鉴定_2021年浙教版科学准九年级上学期暑假讲义(word,无答案): 这是一份11.离子鉴定_2021年浙教版科学准九年级上学期暑假讲义(word,无答案),共11页。学案主要包含了常见的离子检验方法,混合溶液中常见离子的检验,混合物成分的分步检验和测定等内容,欢迎下载使用。