


高中化学人教版 (新课标)选修5 有机化学基础第二章 烃和卤代烃综合与测试同步练习题
展开1.掌握各类烃的结构与性质。
2.掌握卤代烃在有机合成中的应用。
【考点归纳】
考点一 烃的结构与性质
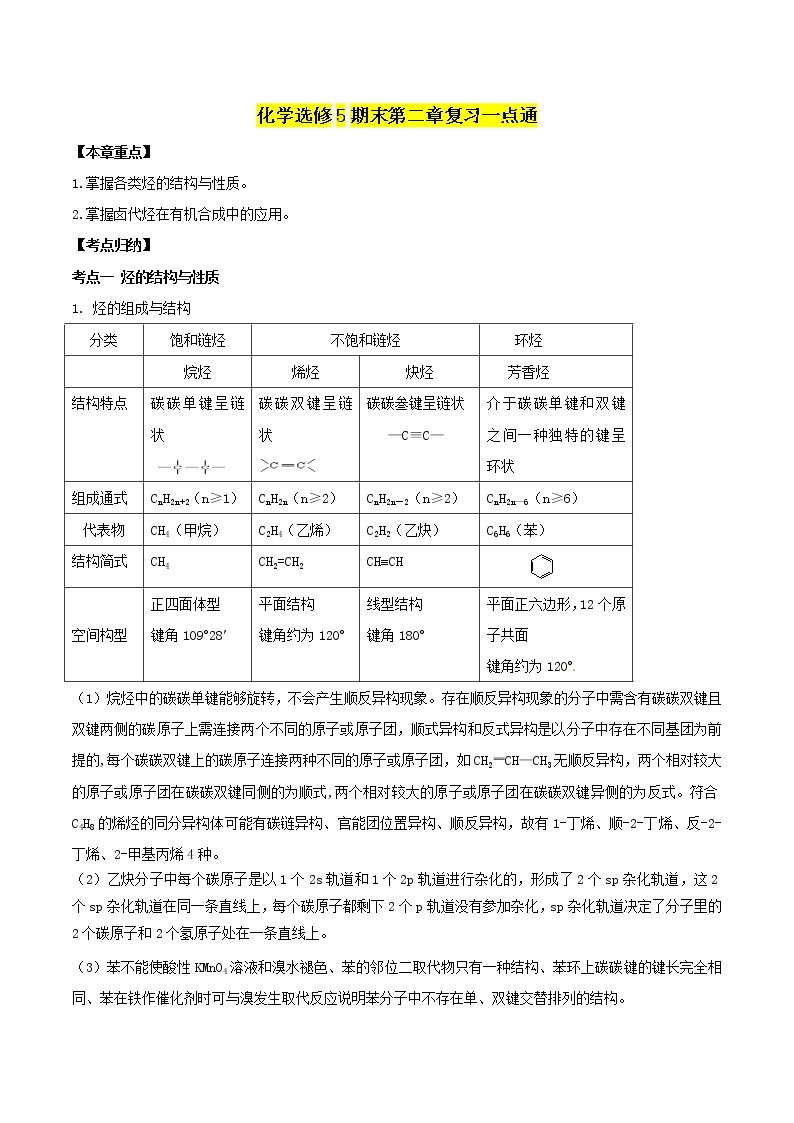
1. 烃的组成与结构
(1)烷烃中的碳碳单键能够旋转,不会产生顺反异构现象。存在顺反异构现象的分子中需含有碳碳双键且双键两侧的碳原子上需连接两个不同的原子或原子团,顺式异构和反式异构是以分子中存在不同基团为前提的,每个碳碳双键上的碳原子连接两种不同的原子或原子团,如CH2CH—CH3无顺反异构,两个相对较大的原子或原子团在碳碳双键同侧的为顺式,两个相对较大的原子或原子团在碳碳双键异侧的为反式。符合C4H8的烯烃的同分异构体可能有碳链异构、官能团位置异构、顺反异构,故有1-丁烯、顺-2-丁烯、反-2-丁烯、2-甲基丙烯4种。
(2)乙炔分子中每个碳原子是以1个2s轨道和1个2p轨道进行杂化的,形成了2个sp杂化轨道,这2个sp杂化轨道在同一条直线上,每个碳原子都剩下2个p轨道没有参加杂化,sp杂化轨道决定了分子里的2个碳原子和2个氢原子处在一条直线上。
(3)苯不能使酸性KMnO4溶液和溴水褪色、苯的邻位二取代物只有一种结构、苯环上碳碳键的键长完全相同、苯在铁作催化剂时可与溴发生取代反应说明苯分子中不存在单、双键交替排列的结构。
(4)因苯的结构的特殊性,判断因取代基位置不同而形成的同分异构体时,通常采用“对称轴”法,即在被取代的主体结构中,找出对称轴,取代基只能在对称轴的一侧,或是在对称轴上而不能越过对称轴(针对一元取代物而言)。例如,二甲苯的对称轴如下(虚线表示):邻二甲苯 (小圆圈表示能被取代的位置),间二甲苯,对二甲苯。因此,邻、间、对3种二甲苯苯环上的一元取代物共有6种。甲苯苯环上共有5个氢原子可被取代,一氯代物有3种,可利用换元法推知四氯代物也有3种。
2. 脂肪烃的物理性质
(1)所有的烃都不溶于水而易溶于苯、乙醚等有机溶剂,其密度比水小。
(2)分子里碳原子数≤4的脂肪烃在常温常压下都是气体,其他脂肪烃在常温常压下是液体或固体(新戊烷除外),随着分子中碳原子数的增加,常温下脂肪烃的状态也由气态逐渐过渡到液态或固态。
(3)烃类的熔、沸点一般较低,其变化规律如下:组成与结构相似的物质(同系物),相对分子质量越大,其熔、沸点越高;相对分子质量相近或相同的物质(如同分异构体),支链越多,其熔、沸点越低;组成与结构不相似的物质,当相对分子质量相同或相近时,分子的极性越大,其熔、沸点越高。
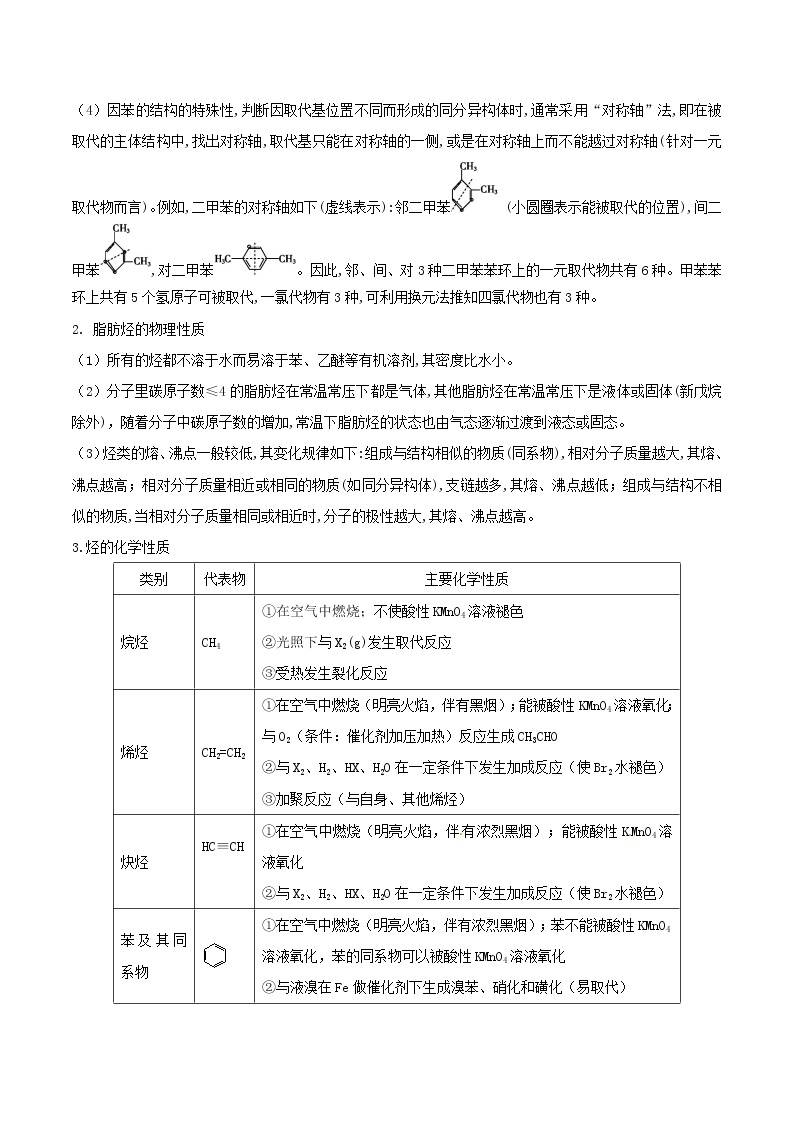
3.烃的化学性质
(1)乙烯能使溴水褪色是因为与溴水发生了加成反应:+Br2CH2BrCH2Br;使酸性高锰酸钾溶液褪色是因为发生了氧化还原反应;除去乙烷中混有的乙烯能用溴水,但不能用酸性高锰酸钾溶液除去乙烷中混有的乙烯,因为乙烯会被酸性高锰酸钾溶液氧化成二氧化碳气体,从而产生新的杂质。
(2)鉴别烷烃和烯烃可用溴的四氯化碳溶液(或溴水)或酸性高锰酸钾溶液进行鉴别,能使二者褪色的为烯烃,不能使二者褪色的为烷烃。
(3)乙炔分子里碳碳三键是由1个σ键和2个π键构成的。乙炔的π键也易发生断裂,故易发生加成反应和氧化反应。学科-网
(4)烷烃和苯均能与卤素单质发生取代反应,相同点是都与纯卤素单质反应,不与卤素单质水溶液反应;不同点是烷烃与卤素单质在光照条件下发生取代反应,苯需要Fe(实质为卤化铁)作催化剂。
3. 加成反应与取代反应的比较
【考点练习】
1.下列说法中错误的是 ( )
A.无论是乙烯的加成反应,还是乙烯使酸性KMnO4溶液褪色,都与其分子内含有碳碳双键有关
B.无论使用溴的四氯化碳溶液还是酸性KMnO4溶液,都可以鉴别乙烯和乙烷
C.等质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.乙烯的化学性质比乙烷的化学性质活泼
2. 有机物的结构可用“键线式”表示,如CH3—CH===CH—CH3可简写为。有机物X的键线式为。下列说法不正确的是( )
A.X的化学式C8H8[来源:Z*xx*k.Cm]
B.有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为
C.X能使KMnO4酸性溶液褪色
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种
3.下列有机物分子中,可形成顺反异构的是( )
A.CH2===CHCH3 B.CH2===CHCH2CH3 C.CH3CH===C(CH3)2 D.CH3CH===CHCl
4.下列有关叙述正确的是( )
A.按系统命名法,化合物的名称是2,3,5,5-四甲基-4,4-二乙基己烷
B.四联苯的一氯代物有5种
C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键
D.间二甲苯的结构简式为
5.下列关于有机物的说法错误的是( )。
①和的实验式相同②和C6H6含碳量相同③丁二烯和丁烯为同系物④正戊烷、异戊烷、新戊烷的沸点逐渐降低⑤标准状况下,11.2 L戊烷所含的分子数为0.5NA(NA为阿伏加德罗常数的值)⑥能够快速、微量、精确地测定有机物相对分子质量的物理方法是核磁共振氢谱法
A.①②⑥ B.②③④ C.②④⑥ D.③⑤⑥
6.蒽()与苯炔()反应生成化合物X(立体对称图形),如图所示:
(1)蒽与X都属于 (填字母,下同)。
a.环烃 b.烃 c.不饱和烃
(2)苯炔的分子式为 ,苯炔不具有的性质是 。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列属于苯的同系物的是 。
A.B.C.D.
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能因发生加成反应而使溴水褪色,还能使酸性高锰酸钾溶液褪色的是 。
A.B.C6H14 C.D.
7.(1)苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑。
回答下列问题:
①试管A中发生反应的化学方程式为 。
②试管C中四氯化碳的作用是 。反应开始后,观察D和E两试管,看到的现象为 。写出E中发生反应的离子方程式: 。
③反应2~3 min后,在B中的NaOH溶液里可观察到的现象是 。
④在上述整套装置中,具有防倒吸作用的仪器有 (填字母)。
(2)实验室制备硝基苯的主要步骤如下:
a.配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c.在55~60 ℃下发生反应,直至反应停止;
d.除去混合酸后,粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后再用蒸馏水洗涤;
e.将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。
①制备硝基苯的反应类型是 。
②配制一定比例的浓H2SO4和浓HNO3的混合酸时,操作的注意事项是 。
③步骤d中洗涤、分离粗硝基苯应使用的仪器是 。
④步骤d中粗产品用5%的NaOH溶液洗涤的目的是 。
8.下图是8种有机化合物的转化关系:
请回答下列问题:
(1)根据系统命名法,化合物A的名称是 。
(2)上述转化中,①是 (填反应类型,下同)反应,③是 反应。
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式: 。
(4)C1的结构简式是 ;F1的结构简式是 。F1和F2互为 。
(5)上述8种化合物中,属于二烯烃的是 ,二烯烃的通式是 。
(6)若将反应④中的条件改为NaOH的水溶液,请写出由D生成E的化学方程式: 。
考点二 卤代烃的结构与性质
1.卤代烃的结构与性质
2. 卤代烃的消去反应和水解反应比较
3. 卤代烃中卤素原子的检验方法
(1)实验原理:R—X+H2Oeq \(――→,\s\up7(NaOH),\s\d5(△))R—OH+HX;HX+NaOH===NaX+H2O;HNO3+NaOH===NaNO3+H2O;AgNO3+NaX===AgX↓+NaNO3。根据沉淀(AgX)的颜色(白色、浅黄色、黄色)可确定相应卤素(氯、溴、碘)种类。
(2)实验操作:取少量卤代烃加入试管中,加入NaOH溶液,加热(是为了加快水解速率),冷却,加入稀硝酸酸化(一是为了中和过量的NaOH,防止NaOH与AgNO3反应干扰实验;二是检验生成的沉淀是否溶于稀硝酸),加入AgNO3溶液,即R—Xeq \(――→,\s\up7(加NaOH水溶液),\s\d5(△))R—OH、NaXeq \(――→,\s\up7(加稀硝酸酸化),\s\d5(中和过量的NaOH))R—OH、NaXeq \(――→,\s\up7(加AgNO3溶液),\s\d5( ))eq \b\lc\{\rc\ (\a\vs4\al\c1(若产生白色沉淀,卤素原子为氯原子,若产生浅黄色沉淀,卤素原子为溴原子,若产生黄色沉淀,卤素原子为碘原子))
4. 卤代烃在有机合成中的作用
(1)卤素原子引入的途径
(2)卤代烃在有机合成中的应用:卤代烃是一种重要的有机合成试剂。由于卤代烃发生水解(或取代)反应可以生成醇,发生消去反应可以生成烯烃、炔烃等,继续可合成许多有机物,因此卤代烃在有机合成和有机推断中起着桥梁作用。
应用最多的是卤代烃先转化为烯烃,烯烃和卤素单质加成生成二元卤代烃,再合成二元醇、二元醛、二元酸等。[来源:学.科.网]
【考点练习】
1.下列关于卤代烃的说法不正确的是 ( )
A.在溴乙烷(CH3CH2Br)分子中,溴元素的存在形式为溴原子
B.在卤代烃中,卤素原子与碳原子形成共价键
C.聚四氟乙烯(塑料王)为高分子化合物,不属于卤代烃
D.卤代烃比相应的烷烃的沸点高
2. 有两种有机物Q()与P(),下列有关它们的说法中正确的是( )
A.二者在核磁共振氢谱中均只出现两个峰且峰面积之比为3∶2
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种,P的一溴代物有2种
3.欲证明某一卤代烃为溴代烃,甲、乙两同学设计了如下方案。甲同学:取少量卤代烃,加入NaOH的水溶液,加热,冷却后加入AgNO3溶液,若有淡黄色沉淀生成,则为溴代烃。乙同学:取少量卤代烃,加入NaOH的乙醇溶液,加热,冷却后,用硝酸酸化,加入AgNO3溶液,若有淡黄色沉淀生成,则为溴代烃。关于甲、乙两位同学的实验评价正确的是( )
A.甲同学的方案可行
B.乙同学的方案可行
C.甲、乙两位同学的方案都有局限性
D.甲、乙两位同学的实验所涉及的卤代烃的性质一样
4.下列有机物检验方法正确的是 ( )
A.取少量卤代烃加NaOH水溶液共热,冷却,再加AgNO3溶液检验卤素原子存在
B.用KMnO4酸性溶液检验溴乙烷与NaOH醇溶液共热后的产物是否是乙烯
C.用溴水鉴别乙烯与乙炔
D.不能只用NaOH水溶液来鉴别一氯乙烷和三氯乙烷
5.下列化学反应的产物中,存在同分异构体的是( )
A.CH3CH2CH2Br在碱性溶液中水解
B.甲苯在催化剂作用下与Cl2发生取代反应
C.与NaOH的醇溶液共热反应
D.在催化剂存在下与H2完全加成
6.溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__气体。继续滴加至液溴滴完。装置d的作用是____;
(2)液溴滴完后,经过下列步骤分离提纯:①向a中加入10 mL水,然后过滤除去未反应的铁屑;②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是_______________________;③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是__________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必需的是___________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是______(填入正确选项前的字母)。
A.25 mL B.50 mL C.250 mL D.500 mL
7.有以下一系列反应,终产物为草酸:
已知B的相对分子质量比A大79。
(1)请推测用字母代表的化合物的结构式:C是______ ,F是________。
(2)①B→C的反应类型是_________;②C→D的化学方程式是________________。
8. 烷烃A只可能有三种一氯取代产物B、C和D。C的结构简式是:,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下图所示。
请回答:
(1)A的结构简式是 。
(2)H的结构简式是 。
(3)B转变为F的反应属于 反应(填反应类型名称)。
(4)B转变为E的反应属于 反应(填反应类型名称)。
(5)1.16gH与足量NaHCO3作用,标装饰品下可得CO2的体积是 mL。
分类
饱和链烃
不饱和链烃
环烃
烷烃
烯烃
炔烃
芳香烃
结构特点
碳碳单键呈链状
碳碳双键呈链状
碳碳叁键呈链状
—C≡C—
介于碳碳单键和双键之间一种独特的键呈环状
组成通式
CnH2n+2(n≥1)
CnH2n(n≥2)
CnH2n-2(n≥2)
CnH2n—6(n≥6)
代表物
CH4(甲烷)
C2H4(乙烯)
C2H2(乙炔)
C6H6(苯)
结构简式
CH4
CH2=CH2
CHCH
空间构型
正四面体型
键角10928
平面结构
键角约为120
线型结构
键角180
平面正六边形,12个原子共面
键角约为120
类别
代表物
主要化学性质
烷烃
CH4
①在空气中燃烧;不使酸性KMnO4溶液褪色
②光照下与X2(g)发生取代反应
③受热发生裂化反应
烯烃
CH2=CH2
①在空气中燃烧(明亮火焰,伴有黑烟);能被酸性KMnO4溶液氧化;与O2(条件:催化剂加压加热)反应生成CH3CHO
②与X2、H2、HX、H2O在一定条件下发生加成反应(使Br2水褪色)
③加聚反应(与自身、其他烯烃)
炔烃
HC≡CH[来源:学。科。网Z。X。X。K]
①在空气中燃烧(明亮火焰,伴有浓烈黑烟);能被酸性KMnO4溶液氧化
②与X2、H2、HX、H2O在一定条件下发生加成反应(使Br2水褪色)
苯及其同系物
①在空气中燃烧(明亮火焰,伴有浓烈黑烟);苯不能被酸性KMnO4溶液氧化,苯的同系物可以被酸性KMnO4溶液氧化
②与液溴在Fe做催化剂下生成溴苯、硝化和磺化(易取代)
③与H2(Ni作催化剂)加成生成环己烷(难加成)
名称
比较
取代反应
加成反应
概念
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应
反应前后分子数目
一般相等
减少
反应特点
反应常常分步发生,多步反应共同进行
有时只有一种加成方式,有时有多种加成方式
结构特点
卤素原子是卤代烃的官能团。C—X之间的共用电子对偏向X,形成一个极性较强的共价键,分子中C—X键易断裂
物理性质
常温下大多数呈液态或固态;不溶于水,可溶于乙醚、苯、环己烷等大多数有机溶剂;沸点高于相应的烃,且随着烃基中碳原子数的增加而升高;密度大于相应的烃,随分子中碳原子数增多而减小,随分子中卤素原子数的增多而增大
化学性质
①取代反应:C2H5Br+NaOHC2H5OH+NaBr
②消去反应:CH3CH2CH2Br+KOHCH3—CH==CH2+KBr+H2O
消去反应
水解反应
反应条件
NaOH醇溶液、加热
NaOH水溶液、加热
反应实质
失去HX分子,形成不饱和键
—X被—OH取代
键的变化
C—X键断裂,形成C—OH键
卤代烃的要求
含有两个或两个以上的碳原子,如CH3Br不能反应;与卤原子相连的碳原子相邻的碳原子上有氢原子,如
、(CH3)3CCH2Br都不能反应,而CH3—CH2—Cl可以;直接连接在苯环上的卤原子不能消去。如不能反应
含有—X的卤代烃绝大多数都可以水解
反应特点
有机物碳骨架不变,官能团由—X变为或—C≡C—
有机物碳骨架不变,官能团由—X变为—OH
主要产物
烯烃或炔烃
醇
取代反应
CH2===CH—CH3+Cl2eq \(――→,\s\up7(500~600 ℃),\s\d5( ))CH2===CH—CH2Cl+HCl
加成反应
CH2===CH—CH3+Br2―→CH2BrCHBrCH3
CH2===CH—CH3+HBr―→CH2BrCH2CH3
CH2===CH—CH3+HBr―→CH3CHBrCH3
CH≡CH+Br2―→CHBr===CHBr
CHBr===CHBr+Br2―→CHBr2CHBr2
CH≡CH+HCleq \(――→,\s\up7(催化剂),\s\d5( ))CH2===CHCl
苯
溴
溴苯
密度/g·cm-3
0.88
3.10
1.50
沸点/℃
80
59
156
水中溶解度
微溶
微溶
微溶
高中化学选修五第二章综合能力检测题及答案解析: 这是一份高中化学选修五第二章综合能力检测题及答案解析,共16页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
高中化学选修五第四、五章综合能力检测题及答案解析: 这是一份高中化学选修五第四、五章综合能力检测题及答案解析,共16页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
高中化学选修五第三章综合能力检测题及答案解析: 这是一份高中化学选修五第三章综合能力检测题及答案解析,共15页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。