
2021年初中科学二轮复习专题24:金属 (含解析)
展开1.向一定质量的AgNO3和Cu(NO)2的混合溶液中不断加入铁粉,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程,下列说法错误的是( )
A. 向a点溶液中滴加稀盐酸,有白色沉淀 B. bd段是铁粉与Cu(NO)2溶液反应
C. d点溶液中的溶质是Fe(NO)3 D. 在e点时,能得到3种固体
2.下列图像能正确表示对应变化关系的是( )
A. 图甲表示水通电分解产生的气体质量m与反应时间t的关系
B. 图乙表示两份完全相同的双氧水在有无MnO2的情况下,产生的O2质量m与反应时间t的关系
C. 图丙表示往锌中加入足量的稀H2SO4 , 产生的H2质量m与反应时间t的关系
D. 图丁表示往稀盐酸和CuCl2混合液中滴人NaOH溶液,产生的沉淀质量m2与NaOH溶液质量m1的关系
3. 下列实验方案不合理的是( )
A. 用观察颜色的方法鉴别磷矿粉和硝酸钾
B. 用植物的花瓣制作指示剂,检验溶液的酸碱性
C. 用水鉴别NH4NO3、Na0H、NaCl三种固体
D. 用FeSO4溶液、Cu和Ag比较Fe、Cu和Ag的金属活动性
4.对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂不可行的是( )
A. Fe、Ag、CuSO4溶液 B. Fe、Cu、稀盐酸、AgNO3溶液
C. Cu、Ag、FeSO4溶液 D. Cu、FeSO4溶液、AgNO3溶液
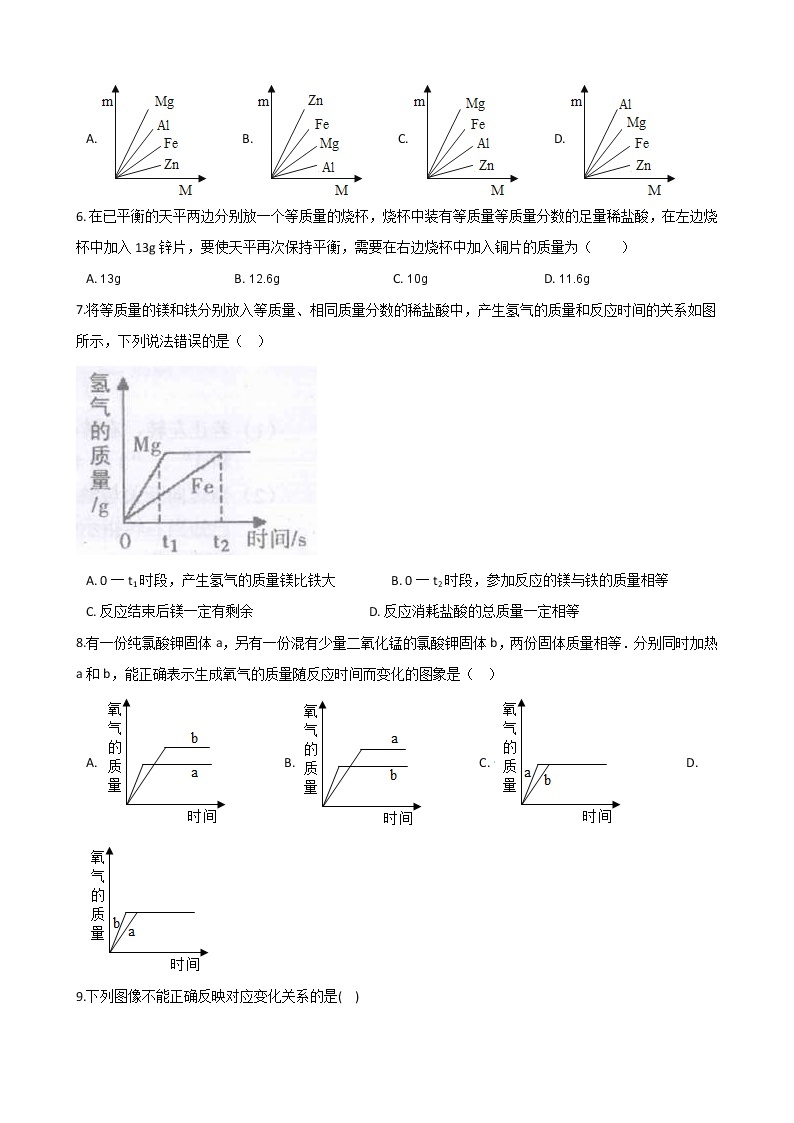
5.下图表示Fe、Zn、Mg、Al分别跟稀盐酸反应制取氢气的质量(m)与所用的金属质量(M)之间的关系图,其中正确的是( )
A. B. C. D.
6. 在已平衡的天平两边分别放一个等质量的烧杯,烧杯中装有等质量等质量分数的足量稀盐酸,在左边烧杯中加入13g锌片,要使天平再次保持平衡,需要在右边烧杯中加入铜片的质量为( )
A. 13g B. 12.6g C. 10g D. 11.6g
7.将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量和反应时间的关系如图所示,下列说法错误的是( )
A. 0一t1时段,产生氢气的质量镁比铁大 B. 0一t2时段,参加反应的镁与铁的质量相等
C. 反应结束后镁一定有剩余 D. 反应消耗盐酸的总质量一定相等
8.有一份纯氯酸钾固体a,另有一份混有少量二氧化锰的氯酸钾固体b,两份固体质量相等.分别同时加热a和b,能正确表示生成氧气的质量随反应时间而变化的图象是( )
A. B. C. D.
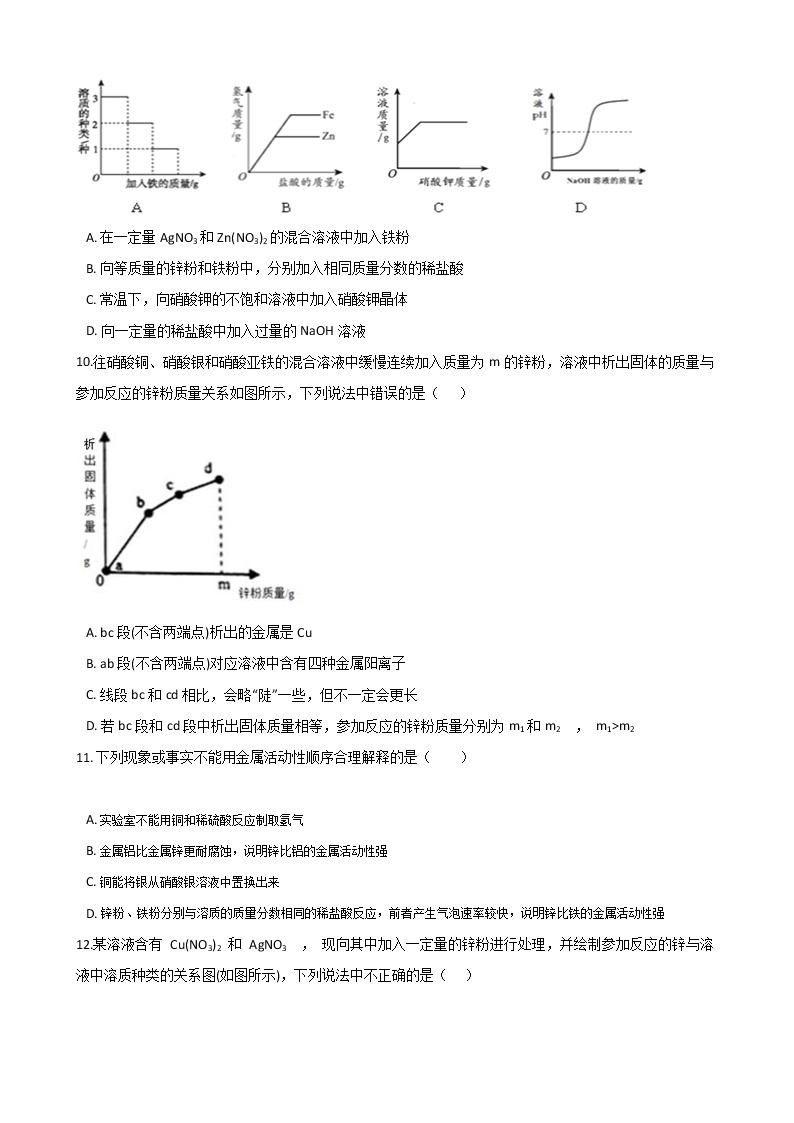
9.下列图像不能正确反映对应变化关系的是( )
A. 在一定量AgNO3和Zn(NO3)2的混合溶液中加入铁粉
B. 向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
C. 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
D. 向一定量的稀盐酸中加入过量的NaOH溶液
10.往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中错误的是( )
A. bc段(不含两端点)析出的金属是Cu
B. ab段(不含两端点)对应溶液中含有四种金属阳离子
C. 线段bc和cd相比,会略“陡”一些,但不一定会更长
D. 若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2 , m1>m2
11. 下列现象或事实不能用金属活动性顺序合理解释的是( )
A. 实验室不能用铜和稀硫酸反应制取氢气
B. 金属铝比金属锌更耐腐蚀,说明锌比铝的金属活动性强
C. 铜能将银从硝酸银溶液中置换出来
D. 锌粉、铁粉分别与溶质的质量分数相同的稀盐酸反应,前者产生气泡速率较快,说明锌比铁的金属活动性强
12.某溶液含有 Cu(NO3)2 和 AgNO3 , 现向其中加入一定量的锌粉进行处理,并绘制参加反应的锌与溶液中溶质种类的关系图(如图所示),下列说法中不正确的是( )
A. Cu 的活动性比 Ag 强,只用盐酸无法探究两者活动性强弱
B. 当溶质种类为1种时,金属单质种类可能为2种
C. c~d 间(不含两点)的溶液中金属离子为 Zn2+、Cu2+
D. 从 m1 变化到 m2 时,溶液中硝酸铜的质量分数不变
13.下列图像不能正确反映对应变化关系的是( )
A. 在一定量AgNO3和Zn(NO)2的混合溶液中加入铁粉
B. 向等质量的锌粉和铁粉中,分别加入相同质量分数的稀盐酸
C. 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体
D. 向一定量的稀盐酸中加入过量的NaOH溶液
14.某科学兴趣小组的小应同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液。实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示:加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示,下列说法正确的是( )
A. 图1中b→c段表示生产气体过程
B. 图1中b点的值为106
C. 图1中c点时,溶液中的溶质有两种
D. 图1中→a段反应过程中溶液的pH变化情况可用图2中d→h段表示
15.将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中。待充分反应后过滤,再在滤渣中加入稀盐酸,没有气体产生,则在滤液中( )
A. 只有硝酸锌和水 B. 如果没有硝酸铜,一定没有硝酸银
C. 一定没有硝酸银 D. 一定有硝酸银和硝酸亚铁
16.将一定质量的铁粉加入含AgNO3和Zn(NO3)2两种溶质的溶液中,反应结束后过滤,分别向滤液和滤渣中加入稀盐酸,均无明显现象,下列对滤渣和滤液的说明中,不正确的是( )
A. 滤渣的成分只有银 B. 滤液中的溶质是Zn(NO3)2、Fe (NO3)2
C. 滤渣的成分可能是银、锌的混合物 D. 所得滤液的质量小于反应前原溶液的质量
17.某化学小组在一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉充分反应后过滤,得到溶液甲和固体乙,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2
②固体乙中一定含有Ag,可能含有Cu和Zn ③若溶液甲是蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2 ④向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2。上述四种说法正确的个数为( )
A. 1个 B. 2个 C. 3个 D. 4个
18. 下列对课本中的图表、数据的使用,叙述不正确的是( )
A. 根据金属活动性顺序表,判断金属能否与稀盐酸、稀硫酸反应产生氢气
B. 根据元素周期表,可以查找元素原子核内中子的数目
C. 根据“酸、碱和盐溶解性表”,判断复分解反应能否发生
D. 根据物质的溶解度曲线图,可确定该物质在某一温度时的溶解度
19. 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
A. 乙、甲、丙 B. 乙、丙、甲 C. 丙、甲、乙 D. 丙、乙、甲
20.现有铁、氧化铁、稀硫酸、氢氧化钙溶液、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“一”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系)。下列判断合理的是( )
A. 丙可能是碳酸钠溶液 B. 丁可能是氢氧化钙溶液
C. 乙必须通过置换反应转化为铁 D. 甲和丁的反应一定是中和反应
21.下列四个实验中。“操作--图象--结论”对应关系正确的是( )
A. A B. B C. C D. D
22.兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象,下列说法不正确的是( )
A. 由实验可判断出铁、铜、锌的活动性顺序
B. 两支试管混合后,固体总质量一定增加
C. 滤液中的溶质一定有FeCl2、ZnCl2和CuCl2
D. 滤渣中一定有Cu,一定没有Fe和Zn
23.下列实验操作能达到实验目的是( )
A. A B. B C. C D. D
24.在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如表所示,下列说法错误的是( )
A. a可能是反应物也可能是生成物 B. x+y=20
C. x的取值范围是0≤x≤20 D. 反应生成c与d的质量比为2:1
25.既不溶于水,又不跟稀硫酸反应,但能跟硝酸银溶液反应的物质是 ( )
A. Fe B. Cu C. BaCl2 D. HCl
答案解析部分
一、单选题
1. C
解析:根据金属活动性顺序中排在前面的金属能与排在后面的金属的盐溶液发生反应,且两金属相差越多越先反应分析。
解答: 向一定质量的AgNO3和Cu(NO)2的混合溶液中不断加入铁粉, 铁先与硝酸银反应,然后再与硝酸铜反应;
A、 a点溶液为硝酸银部分反应的图像,向a点溶液中滴加稀盐酸,有白色沉淀产生,不符合题意;
B、 bd段是铁粉与Cu(NO)2溶液反应 ,不符合题意;
C、 d点为硝酸银和硝酸铜恰好完全反应的图像,溶液中的溶质是硝酸亚铁,不是硝酸铁,符合题意;
D、 e点为镁粉过量的图像,在e点时,固体 为银、铜、铁三种,不符合题意;
故答案为:C。
2. D
解析:
A、根据电解水时生成的氢气和氧气的质量关系分析;
B、根据双氧水放出氧气的质量与有无催化剂无关分析;
C、根据锌与硫酸反应生成的氢气和时间的之间的关系分析;
D、往稀盐酸和CuCl2混合液中滴入NaOH溶液,首先稀盐酸与NaOH溶液反应,当稀盐酸反应完,CuCl2再与NaOH溶液反应生成沉淀。
解答:
A、电解水时生成的氢气和氧气的质量比是1:8,故A错误;
B、双氧水放出氧气的质量与有无催化剂无关,生成的氧气的质量相等,故B错误;
C、锌与硫酸反应生成的氢气随时间的增加而增大,故C错误;
D、向含有盐酸和CuCl2的混合溶液中加入NaOH溶液,开始没有沉淀生成,因为如果生成氢氧化铜沉淀也会被盐酸溶解.当盐酸完全和氢氧化钠溶液反应后开始生成沉淀,当氯化铜完全和氢氧化钠溶液反应后不再生成沉淀,故D正确。
故选D。
3. D
【解析】解答:解:A、磷矿粉是灰白色的,硝酸钾是白色的晶体,用观察颜色的方法可以鉴别磷矿粉和硝酸钾,故选项实验方案合理;
B、某些植物的花瓣中含有能够遇酸碱会变色的物质,可检验溶液的酸碱性,故选项实验方案合理;
C、NH4NO3溶于水吸热,氢氧化钠溶于水放出大量的热,氯化钠溶于水温度几乎无变化,可以鉴别,故选项实验方案合理;
D、Cu和Ag与FeSO4溶液均不反应,说明了活动性铁>铜,铁>银,但无法确定银和铜的活动性强弱,故选项实验方案不合理.
故选:D.
分析:A、根据磷矿粉是灰白色的,硝酸钾是白色的晶体,进行分析判断;
B、根据某些植物的花瓣中含有能够遇酸碱会变色的物质分析判断;
C、根据三种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们;
D、根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断,通过分析方案所能得到的结论,确定是否能得出Fe、Cu和Ag三种金属的活动性顺序.
4. C
【解析】解答:A、Fe与CuSO4溶液反应置换出铜,说明了活动性铁>铜;Ag与CuSO4溶液不反应,说明了活动性铜>银;由此可得出三种金属活动性铁>铜>银;故该方案合理;
B、Fe与稀盐酸反应置换出氢气,说明了活动性铁>氢;Cu与稀盐酸不反应,说明了活动性氢>铜;Cu能与硝酸银溶液反应生成硝酸铜和银,说明了活动性铜>银;由此可得出三种金属活动性铁>铜>银;故该方案合理;
C、Cu、Ag均不能与硫酸亚铁溶液反应,说明了活动性铁>铜,铁>银,但无法确定铜和银的活动性强弱,故该方案不合理;
D、铜与FeSO4溶液不反应,说明了活动性铁>铜;Cu能与硝酸银溶液反应生成硝酸铜和银,说明了活动性铜>银;由此可得出三种金属活动性铁>铜>银;故该方案合理;
故选:C.
分析:根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“反应则活泼,不反应则不活泼”进行分析判断,通过分析方案所能得到的结论,确定是否能得出Ag、Fe、Cu三种金属的活动性顺序.
5. D
【解析】解答:假设等质量的四种金属的质量为m,与酸完全反应放出氢气质量为:
铝完全反应放出氢气质量= QUOTE
镁完全反应放出氢气质量= QUOTE
铁完全反应放出氢气质量= QUOTE
锌完全反应放出氢气质量= QUOTE
则关系图中四条线从上到下的顺序为:Al、Mg、Fe、Zn;
故选D.
分析:根据等质量的四种金属与酸完全反应放出氢气质量的大小,判断关系图中四条线与金属的对应关系.
6. B
【解析】解答:设锌和稀盐酸反应后增重为x,
Zn+2HCl═ZnCl2+H2↑,增重
65 2 65﹣2=63
13g x
QUOTE 6513g=63x 6513g=63x ,
x=12.6g,
因为铜不能和稀盐酸反应,因此要使天平再次保持平衡,需要在右边烧杯中加入铜片的质量为12.6g.
故选:B.
分析:锌和稀盐酸反应生成氯化锌和氢气,铜不能和稀盐酸反应;
根据锌的质量可以计算反应生成氢气的质量,进一步可以计算需要在右边烧杯中加入铜片的质量.
7. B
解析:本题是图像的判断题,解答时要通过题目要求分析涉及到的各物质之间量的关系,结合变化趋先做出判断,如随着横坐标物质量的变化纵坐标表示的物质的量的变化趋势,增加或降低等,再确定图形中的起点、终点、转折点是否符合题意。
解答:A、镁的化学性质比铁活泼, 0一t1时段,产生氢气的质量镁比铁大,说法正确;
B、 由图像可知,最终产生氢气质量镁和铁的相等,说明镁与铁质量不相等,因为等质量的镁和铁完全反应镁产生氢气比铁多,说法错误;
C、 等质量的镁和铁完全反应镁产生氢气比铁多,若产生等量氢气,则说明消耗的酸质量相等,而金属质量不相等,则反应结束后镁一定有剩余,说法正确;
D、最终产生等量氢气说明反应消耗盐酸的总质量一定相等 ,说法正确;
故答案为:B。
8. B
解析:根据氯酸钾分解时二氧化锰的催化作用分析,结合图像中各曲线的变化趋势及起点与转折点的判断方法解答。
解答:加二氧化 锰的氯酸钾反应快,即产生等量氧气,b所用时间少,但因氯酸钾质量少,所以最终产生氧气质量小于没有加二氧化锰的,即a大于b产生氧气,B符合题意;
故答案为:B。
9. A
解析::坐标曲线类试题,一般先要观察横纵坐标所表示的量,然后观察曲线的特点,包括起点、转折点、终点和变化趋势。
解答::A.起点位置不正确,再加入铁粉质量为“0”时,溶液中不可能有三种溶质,另外依据金属活动性顺序表可知,铁的活动性比银强比锌弱,铁能与硝酸银反应生成硝酸亚铁,不能与硝酸锌反应,故在加入足量铁时,硝酸银完全反应,溶质为硝酸锌和硝酸亚铁两种;故图像错误。
B.开始加盐酸时,盐酸不足完全反应时,氯化氢的质量相等,由化学方程式可知生成氢气的质量也相等,开始一段直线重合;加入的盐酸逐渐增多时,金属完全反应,由化学方程式可知,等质量的金属完全反应铁比锌生成的氢气多;当金属完全反应后,再加入盐酸,反应不再继续,氢气不再增多,图像是一段水平线;选项图像正确。
C.开始时硝酸钾的不饱和溶液一定量,加入硝酸钾晶体会逐渐溶解,溶液质量增加,达到饱和后不再溶解,溶液质量不再增加,选项图像正确;
D.开始时,溶液是稀盐酸,pH小于7,逐渐加入NaOH溶液(pH大于7),溶液pH逐渐增大,当恰好反应时溶液pH=7,当氢氧化钠过量时pH大于7,选项图像正确。
10. D
解析:(1)在发生置换反应时,加入金属总是先与活动性相差最大的金属先反应,然后按照活动性增大以此类推;
(2)首先将图像中的三段与反应过程对应起来,然后写出反应的化学方程式,利用反应物之间的数量关系完成解题。
解答:A.bc段(不含两端点)锌与硝酸铜反应,析出的金属是Cu,故A正确不合题意;
B.ab段锌与硝酸银反应,有生成的锌离子和剩余的银离子,还有没反应的铜离子和亚铁离子,共四种金属阳离子,故B正确不合题意;
C.锌和硝酸铜、硝酸亚铁的反应如下:
Zn+Cu(NO3)2=Zn(NO3)2+Cu;
65 64
Zn+Fe(NO3)2=Zn(NO3)2+Fe;
65 56
根据上面的化学方程式可知,消耗相同质量的锌,生成的铜多,因此BC段会略“陡”一些;但由于硝酸铜和硝酸亚铁的质量无法比较,故不一定会更长,该选项说法正确;
D.根据化学方程式可知,设析出固体质量相等都为m,参加反应的锌粉质量分别为 QUOTE m1=6564m m1=6564m , QUOTE m2=6556m m2=6556m , 则m1<m2 , 故D错误符合题意。
故选D。
11. B
【解析】解答:解:A、在金属活动性顺序表中,铜排在氢的后面,铜与稀硫酸不能反应.故不符合题意;
B、铝的活动性大于锌,但铝易于与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,使内部的铝不易被进一步氧化,与金属活动性强弱顺序无关,故选项正确;
C、铜的活动性大于银,因此铜可以与硝酸银溶液反应置换出银,故不符合题意;
D、锌粉、铁粉都能与盐酸反应,反应时活动性强的镁比活动性弱的锌铁反应剧烈,能用金属活动性强弱顺序加以解释,故不符合题意;
故选:B.
分析:根据金属活动性顺序表的应用分析:排在氢前面的金属可置换出酸中的氢元素,且金属的活动性越强,反应速度越快;排在前面的金属能把排在后面的金属从它们的盐溶液中置换出来.
12. D
解析:根据某溶液含有 Cu(NO3)2 和 AgNO3 , 现向其中加入一定量的锌粉,锌先与硝酸银反应,然后再与硝酸铜反应,且与硝酸银反应溶液质量减小,与硝酸铜反应溶液质量增加分析。
解答:A、 Cu 的活动性比 Ag 强,但都不能与盐酸反应,只用盐酸无法探究两者活动性强弱 ,不符合题意;
B、 当溶质种类为1种时,则为硝酸锌,则金属中一定含铜和银,可能含锌,不符合题意;
C、 c~d 间溶质种类为两种,则为硝酸铜和硝酸锌,溶液中金属离子为 Zn2+、Cu2+ ,不符合题意;
D、 从 m1 变化到 m2 时,溶液中硝酸铜的质量不变,但因锌与硝酸银反应时溶液质量减小,所以硝酸铜质量分数增加 ,符合题意;
故选D。
13. A
解析:本题是图像的判断题,解答时要通过题目要求分析涉及到的各物质之间量的关系,结合变化趋势先做出判断,如随着横坐标物质量的变化,纵坐标表示的物质的量的变化趋势,增加或降低等,再确定图形中的起点、终点、转折点是否符合题意。
解答:A、 在一定量AgNO3和Zn(NO)2的混合溶液中加入铁粉,铁不能与硝到锌反应,能和硝酸银反应,所以反应结束后溶液中溶质有硝酸锌和硝酸亚铁两种,错误;
B、横纵坐为盐酸的质量,等质量盐酸产生氢气质量相等,但最终铁消耗盐酸多,所以产生氢气多,正确;
C、常温下向硝酸银不饱和溶液中加入硝酸钾,硝酸钾继续溶解,溶质质量分数增大,直到达到饱和时不再发生改变,正确;
D、 向一定量的稀盐酸中加入过量的NaOH溶液,溶液pH由小于7到等于7,最后到大于7,与所加氢氧化钠溶液pH接近时几乎不再变化,正确;
故答案为:A。
14. D
解析:根据 向含CaCl2和HCl的废液中加碳酸钠溶液时,碳酸钠先与盐酸反应,然后再与氯化钙反应分析。
解答:A、 图1中b→c段表示生成沉淀过程,不符合题意;
B、 图1中b点为盐酸刚好完全反应时消耗碳酸钠溶液的质量,设碳酸钠溶液质量为 x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
10% x 2.2g
106:44=10%x:2.2g
x=53g,即b的值为53,不符合题意;
C、 图1中c点时,盐酸和氯化钙都恰好完全反应,溶液中的溶质只有氯化钠,不符合题意;
D、 图1中→a段反应过程为盐酸与碳酸钠的反应,溶液的pH变化情况可用图2中d→h段表示,符合题意;
故答案为:D。
15. B
解析:根据金属与盐的混合溶液混合时,按金属活动性顺序中强换弱进行反应,且活动性差距越大的金属越先反应分析。
解答:将铁粉加入到一定量的硝酸银、硝酸铜及硝酸锌的混合溶液中,铁先与硝酸银反应,若过量,再与硝酸铜反应,不能与硝酸锌反应,待充分反应后过滤,再在滤渣中加入稀盐酸,没有气体产生,说明没有铁剩余,则滤液中成分中一定有生成硝酸亚铁和不能参与反应的硝酸锌,若铁刚好与硝酸银反应,则无硝酸银,有硝酸铜,若铁少量,即硝酸银未完全反应,则还一定有硝酸银和硝酸铜。
故答案为:B。
16. C
解析:根据金属活动性顺序的应用分析,在金属活动性顺序表中,排在氢前的金属能与酸发生反应,排在前面的金属能与排在后面的金属的盐溶液反应。
解答: 铁粉加入含AgNO3和Zn(NO3)2两种溶质的溶液中,铁只能与硝酸银发生反应,反应结束后过滤,分别向滤液和滤渣中加入稀盐酸,均无明显现象 ,说明滤液中没有硝酸银,一定有硝酸锌和硝酸亚铁,滤渣中没有铁,只有银,A、B正确;C不正确;根据方程式可知,铁与硝酸银反应时,每56份质量的铁能置换出216份质量的银,溶液质量要减小,D正确;
故选C。
17. D
解析:根据AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,铜粉和锌粉都能与硝酸银反应,都不能和硝酸铝反应,且锌先与硝酸银反应,然后铜再反应分析。
解答: 在一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,铜粉和锌粉都能与硝酸银反应,都不能和硝酸铝反应,且锌先与硝酸银反应,然后铜再反应,得到溶液甲和固体乙,①溶液甲中一定含有Al(NO3)3和Zn(NO3)2 , 正确;②固体乙中一定含有Ag,可能含有Cu和Zn,正确; ③若溶液甲是蓝色,说明一定有硝酸铜剩余,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2 , 正确; ④向固体乙上滴加盐酸有气泡产生,说明固体乙中一定有锌,则溶液甲中一定没有能和锌反应的AgNO3和Cu(NO3)2 , 正确;
故答案为:D。
18. B
【解析】解答:A、根据金属活动顺序可以作为金属能否在溶液中发生置换反应的一种判断依据,位于氢前面的金属能置换出盐酸、稀硫酸中的氢,故A正确;
B、根据元素周期表,可以查出元素的元素符号、原子序数、相对原子质量等,但是不能查找元素原子核内中子的数目;故B错误;
C、利用“酸、碱和盐溶解性表”可判断物质的溶解性,因此,“酸、碱和盐溶解性表”是判断复分解反应能否发生的依据之一;故C正确;
D、溶解度曲线可以查出某物质在一定温度时的溶解度,所以根据溶解度曲线图能判断某物质在一定温度下的溶解度;故D正确.
故选B.
分析:A、根据金属活动顺序可以作为金属能否在溶液中发生置换反应的一种判断依据,进行解答;
B、根据元素周期表,可以查出元素的元素符号、原子序数、相对原子质量等,进行解答;
C、根据复分解反应发生的条件为有气体生成或有水或有沉淀产生进行解答;
D、根据某物质的溶解度曲线图,可判断该物质在一定温度下的溶解度,来解答本题.
19. C
【解析】解答:现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,甲能与盐溶液反应生成乙,说明甲的活动性比乙强;丙能与盐溶液反应生成甲,说明丙的活动性比甲强;丙能与盐溶液反应生成乙,说明丙的活动性比乙强;则三种金属活动性由强到弱的顺序是丙、甲、乙.
故选:C.
分析:在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此根据三种金属间的转化关系应,进而可确定三种金属活动性由强到弱的顺序.
20. A
【解析】
分析:首先根据所给的物质的性质结合反应间的转化关系,找到题中的题眼进行推断解题,硫酸会和其余的四种物质反应,可以知道丁就是硫酸,然后根据其他物质的性质进行验证推导。要发现题眼,要先了解它们之间的相互是否会反应,它们之间的反应关系如下:
解答:
A、根据上面可以看出,碳酸钠会和两种物质反应,而碳酸钠和氢氧化钙都会和两种物质反应,所以甲和丙要从碳酸钠和氢氧化钙中选,丙可能是碳酸钠溶液,故A正确;
B、根据上表可以看出,会与四种物质发生反应的只有硫酸,可知丁一定是硫酸,故B错;
C、只有氧化铁会转化成铁,但是不一定都是置换反应,比如一氧化碳还原氧化铁就不是置换反应,故C错;
D、中和反应必须是酸和碱反应生成盐和水,丁是硫酸,属于酸,但是甲可能是氢氧化钙,也可能是碳酸钠,所以不一定是中和反应,故D错。
故选A。
21. D
解析:根据所给图像中的变化规律及起点,结合各物质间的反应过程判断图像与结论是否一致分析。
解答:A、 分别向等质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸 ,通过反应速率可得出三种金属与硫酸反应的剧烈程度为 Mg>Zn >Fe,不符合题意;
B、 向饱和氢氧化钙溶液中加入氧化钙,氧化钙会吸收水份生成氢氧化钙,溶液中溶剂减少,溶质会析出,所以溶质质量减小,若向不饱和氢氧化钙溶液中加入氧化钙,氧化钙与水反应生成的氢氧化钙会溶解,溶质质量会增加,不符合题意;
C、向变质的氢氧化钠溶液中加稀盐酸,加入一定量稀盐酸后才开始产生气泡,说明氢氧化钠部分变质,不符合题意;
D、 向H2SO4、MgSO4混合溶液中滴加NaOH溶液 ,硫酸先与氢氧化钠反应,然后硫酸镁与氢氧化钠反应, pH为7时水平线段表示硫酸镁和氢氧化钠反应,符合题意;
故选D。
22. C
解析:根据铁能与氯化铜溶液反应,而不能与氯化锌反应,铁和锌都能与盐酸反应产生氢气分析。
解答:A、滤渣中加少量稀盐酸,无明显现象,说明滤渣中不含铁和锌,则证明铁的活动性小于锌,大于铜,不符合题意;
B、 两支试管混合后,铁与氯化铜反应,由方程式Fe+CuCl=FeCl+Cu可知,每56份质量的铁置换出64份质量的铜,固体总质量一定增加 ,不符合题意;
C、 滤液中的溶质一定有FeCl2、ZnCl2可能有CuCl2 ,符合题意;
D、 滤渣中一定有Cu,一定没有Fe和Zn ,不符合题意;
故选C。
23. A
解析:A、结合金属活动性顺序解答;
B、结合NaCl和HC溶液l遇无色酚酞试液的变色情况解答;
C、结合稀硫酸与铁金属及其金属氧化物反应的性质解答;
D、结合是否会生成新的杂质解答。
解答:A、铁丝浸入CuSO4溶液,能置换出铜,说明铁的金属活动性比铜强;铜丝浸入AgNO3溶液,能置换出银,说明铜的金属活动性比银强;则三种金属活动性由强到弱的顺序为铁>铜>银,说法正确;
B、盐酸显酸性,不能使无色酚酞试液变色,说法错误;
C、将铁制品长时间浸泡在足量的稀硫酸中,会损坏铁制品,说法错误;
D、硫酸铜能与过量的氢氧化钠溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,过滤后得到的滤渣是氢氧化铜,将滤渣溶于稀硫酸,氢氧化铜与硫酸反应生成硫酸铜和水;但滤液是硫酸钠和氢氧化钠(过量)的混合溶液,本实验操作不能达到实验目的,说法错误。
24. A
解析:根据密闭容器中物质质量总和相等,反应后质量增加为生成物,增加质量即为生成质量,参加反应的各物质质量总和与反应后生成的物质质量总和相等分析。
解答:A、反应后C质量增加,为生成物,且生成的质量为10克,反应后d质量增加,为生成物,且生成质量为5克,生成物20克,而b反应前只有5克,所以a一定是反应物,符合题意;
B、密闭容器内物质质量总和相等,所以x+y=30+5+10+15-20-20=20,不符合题意;
C、 x为反应物,其取值范围是0≤x≤20,不符合题意;
D、 反应生成c与d的质量比为10:5=2:1 ,不符合题意;
故答案为:A。
25. B
【解析】解答:根据条件,结合金属活动顺序表和酸 的化学性质,可以知道:铁可以与稀硫酸和硝酸银溶液反应,氯化钡溶于水且能有稀老师反应,氯化氢溶于水,只有铜符合条件,顾选B
分析;根据金属活动顺序表和酸的化学性质可以判断
A
B
C
D
操作
分别向等质量的镁粉、铁粉、锌粉中加入等浓度稀硫酸
一定温度下,向氢氧化钙溶液中加入氧化钙固体
向变质的氢氧化钠溶液中滴加稀盐酸
向H2SO4、MgSO4混合溶液中滴加NaOH溶液
图象
结论
三种金属与硫酸反应的剧烈程度: Mg>Fe>Zn
该氢氧化钙溶液已经饱和
氢氧化钠溶液已经全部变质
pH为7时水平线段表示硫酸镁和氢氧化钠反应
选项
实验目的
实验操作
A
比较Fe、Cu、Ag的金属活动性强弱
铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液
B
验证NaCl溶液中混有盐酸
取少量溶液,滴加无色酚酞试液
C
不损坏铁制品的前提下除去表面铁锈
将铁制品长时间浸泡在足量的稀硫酸中
D
分离硫酸钠和硫酸铜的混合溶液
加入过量的氢氧化钠溶液后过滤,并将滤渣溶于稀硫酸
物质
a
b
c
d
反应前的质量/g
30
5
10
15
反应后的质量/g
x
y
20
20
铁
氧化铁
硫酸
氢氧化钙
碳酸钠
铁
不会反应
不会反应
会反应
不会反应
不会反应
氧化铁
不会反应
不会反应
会反应
不会反应
不会反应
硫酸
会反应
会反应
不会反应
会反应
会反应
氢氧化钙
不会反应
不会反应
不会反应
不会反应
会反应
碳酸钠
不会反应
不会反应
不会反应
会反应
不会反应
2021年初中科学二轮复习专题17:受力分析 (含解析): 这是一份2021年初中科学二轮复习专题17:受力分析 (含解析),共13页。试卷主要包含了单选题,多选题,解答题等内容,欢迎下载使用。
2021年初中科学二轮复习专题12:质量与密度 (含解析): 这是一份2021年初中科学二轮复习专题12:质量与密度 (含解析),共15页。试卷主要包含了单选题,填空题,实验探究题,解答题等内容,欢迎下载使用。
2021年初中科学二轮复习专题29:空气 (含解析): 这是一份2021年初中科学二轮复习专题29:空气 (含解析),共17页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。












