





高中化学人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯多媒体教学ppt课件
展开1.掌握乙酸的酸性和酯化反应等化学性质,理解酯化反应的概念。2.了解羧酸的简单分类、主要性质、用途及甲酸的性质。
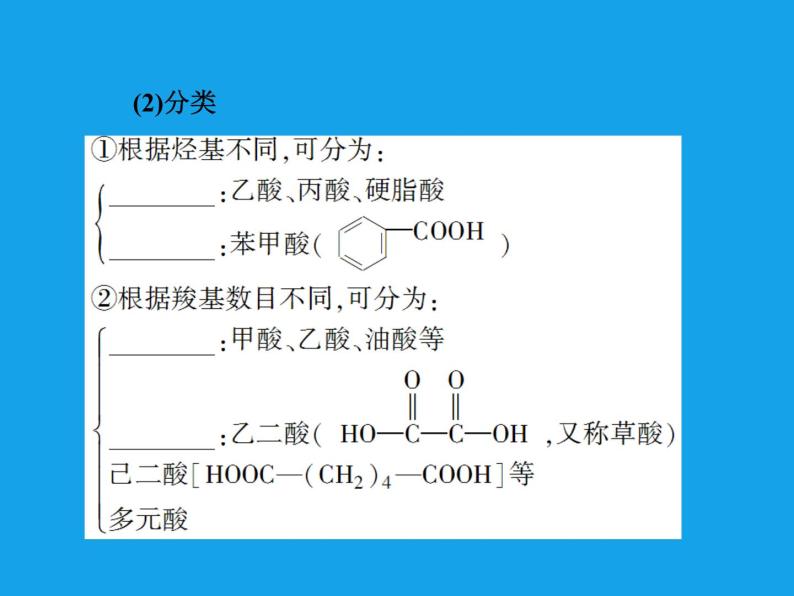
1.羧酸的概念与分类(1)概念在分子里________跟________直接相连接的有机化合物叫作羧酸。
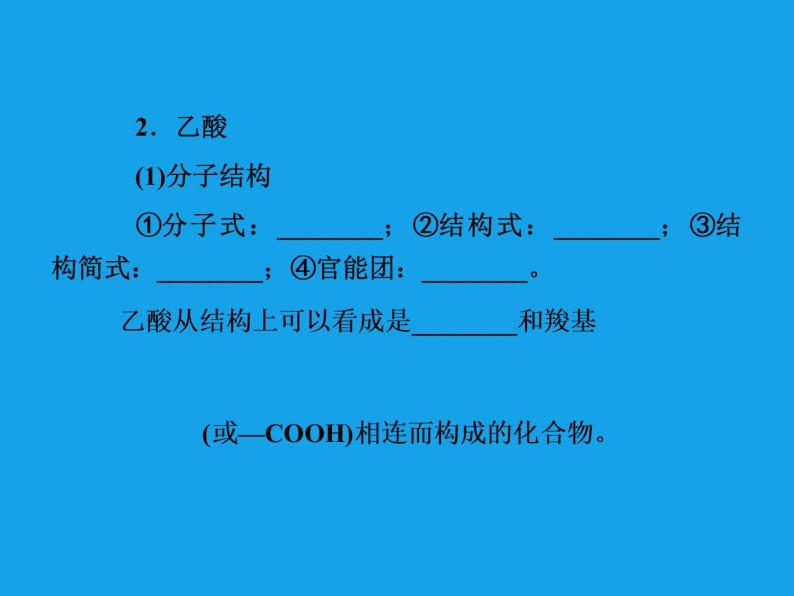
2.乙酸(1)分子结构①分子式:________;②结构式:________;③结构简式:________;④官能团:________。
(2)物理性质乙酸是一种有________气味的________色液体,沸点是117.9℃,熔点是16.6℃。当温度低于________时,乙酸就凝结成像冰一样的晶体,所以无水乙酸又称________。乙酸易溶于________和________。
(3)化学性质①酸性:乙酸在水溶液里能部分电离,产生氢离子。电离方程式为:____________________________。实验:向一盛有少量Na2CO3粉末的试管里,加入约3mL乙酸溶液。实验现象:_________________________________。实验结论:_________________________________。
化学方程式为:____________________,离子方程式为:________________________。乙酸尽管是弱酸,但具有酸的通性。
②酯化反应:概念:________和________作用生成________和________的反应叫酯化反应。乙酸与乙醇在浓H2SO4作用下发生酯化反应的化学方程式为:__________________________。酯化反应的脱水方式是:羧酸脱________而醇脱________,可用18O原子作示踪原子,证明脱水方式。
【答案】 1.(1)烃基 羧基 (2)脂肪酸,芳香酸;一元羧酸,二元羧酸2.(1)①C2H4O2 ② ③CH3COOH ④—COOH 甲基(2)强烈刺激性 无 熔点 冰醋酸 水 乙醇
1.羟基上的氢原子活泼性强弱有什么规律?提示:含氧酸、醇类、酚类化合物分子上均含有羟基,羟基上的氢原子活泼性与跟它相连的基团有关,按物质的类别来看,羟基上的氢原子活泼性强弱顺序为:强含氧酸>多元羧酸>一元羧酸>酚>水>醇。
2.如何理解羧基(—COOH)既能电离出H+显弱酸性,又能和醇发生取代反应?
注意:①羧酸是比H2CO3酸性强的酸,但不同的羧酸酸性也不相同。酸性关系:甲酸>苯甲酸>乙酸>丙酸。②羧酸的羧基中有羰基,此羰基不能发生一般的加成反应。③羧酸在空气或氧气中能燃烧。④酯化反应中的酸是指像乙酸之类的有机酸和像硝酸之类的无机含氧酸。
1.羧酸的定义羧酸是由烃基跟羧基直接相连构成的有机化合物。
2.羧酸的分类(1)根据分子里羧基的数目分类:
(2)根据分子里的烃基是否饱和分类:饱和羧酸:如CH3COOH、CH3CH2COOH、HOOC—CH2—COOH不饱和羧酸:如C6H5COOH、CH2CHCOOH
(3)根据分子里是否含有苯环分类:
3.羧酸的命名首先要选择包括羧基—COOH在内的最长碳链为主链,从离—COOH最近的一端开始编号,其他命名原则同醇类似。例如:3-甲基丁酸
4.羧酸的通式若烃CnHm可衍变为x元羧酸,则该羧酸的分子式为CnHm-2xO2x,如乙烷的分子式为C2H6,乙酸的分子式为C2H4O2;甲苯的分子式为C7H8,苯甲酸的分子式为C7H6O2。一元羧酸的通式为R—COOH。饱和一元脂肪酸的通式为CnH2nO2(n=1,2,3…)。
下列分子比例模型对应物质在水溶液中显酸性的是( )
【解析】 A为乙醛,B为苯酚,C为乙酸,D为乙醇,故显酸性的为B、C。【答案】 BC
下列说法正确的是( )
【解析】 A项名称为3-甲基丁酸,C项符合通式CnH2nO2的物质还有饱和一元羧酸酯。【答案】 BD
②乙酸与金属钠反应:2Na+2CH3COOH―→2Na++2CH3COO-+H2↑。③乙酸与碱(如NaOH)反应:CH3COOH+OH-―→CH3COO-+H2O。④乙酸与盐反应:2CH3COOH+CO32-―→2CH3COO-+H2O+CO2↑。
【例2】 某有机物的结构简式如图
【答案】 NaHCO3 NaOH或Na2CO3 Na
【解析】 本题中需理解的知识是酚羟基和羧基的性质。酚羟基和羧基都有酸性,都能与NaOH溶液反应,但酚羟基不与NaHCO3反应,而羧基能与NaHCO3反应,题给条件水杨酸与某物质反应得到C7H5O3Na,这种物质只能是NaHCO3,所发生的反应为
按下图进行实验,加热试管A中的乙酸、乙醇和浓硫酸的混合液,结果试管B中饱和碳酸钠溶液的液面上可看到有透明的油状液体,并可闻到香味。乙酸和乙醇在浓H2SO4存在和加热条件下,发生反应生成乙酸乙酯,其化学方程式如下:
①乙酸乙酯是酯类化合物的一种。乙酸乙酯密度约为0.9g/cm3,沸点77℃,易溶于乙醇。酸和醇起作用生成酯和水的反应叫做酯化反应。这里的酸可以是有机酸或像硝酸之类的无机含氧酸。②实验室制取乙酸乙酯时要注意:a.化学药品加入试管时,先加乙醇和乙酸,后加浓硫酸。b.加热要小心均匀地进行,以防乙酸、乙醇的大量挥发和液体剧烈沸腾。c.导气管末端不要浸入液体内,以防液体倒吸。
③实验室制取乙酸乙酯时要用饱和碳酸钠溶液吸收乙酸乙酯,主要优点是:随着乙酸乙酯蒸发出来的乙酸与碳酸钠反应生成盐溶于水,乙醇溶于碳酸钠溶液,有利于乙酸乙酯与乙酸、乙醇的分离。
【例3】 下列关于实验室制取乙酸乙酯的说法正确的是( )A.浓硫酸的作用是脱水剂B.导管口要伸入饱和Na2CO2溶液液面下,以确保产物完全吸收C.反应过程中要用水浴加热D.饱和Na2CO3溶液的作用是吸收挥发出来的乙醇和乙酸,并降低乙酸乙酯的溶解度
【解析】 浓硫酸的作用是催化剂、吸水剂;导管口不能伸入饱和Na2CO3溶液的液面下,防止倒吸;该反应可直接加热。故选D。【答案】 D
【答案】 A【点评】 酯化反应的断键规律:羧酸分子失去羟基,醇分子失去氢原子。
胆固醇是人体必须的生物活性物质,分子式为C27H46O,一种胆固醇酯是液晶材料,分子式为C34H50O2,生成这种胆固醇酯的羧酸是( )A.C6H13COOH B.C6H5COOHC.C7H15COOH D.C6H5CH2COOH
【解析】 胆固醇的分子式中只有一个氧原子,应是一元醇,而题给胆固醇酯只有两个氧原子,应为一元酯,据此可写出该酯化反应的通式(用M表示羧酸):C27H46O+M―→C34H50O2+H2O,再由质量守恒定律可求得该酸的分子式为C7H6O2。【答案】 B
(3)甲酸与新制氢氧化铜悬浊液之间是如何反应的?甲酸虽然分子组成简单,但分子内所含的官能团种类多,有羰基、羧基、羟基和醛基,如右图所示:
经过对甲酸分子结构的分析可知,甲酸除有一般羧酸的性质外,还有像醛一样的还原性。甲酸中的醛基被氧化后,使甲酸变为碳酸
化学选修5 有机化学基础第五章 进入合成高分子化合物的时代综合与测试复习课件ppt: 这是一份化学选修5 有机化学基础第五章 进入合成高分子化合物的时代综合与测试复习课件ppt,共32页。PPT课件主要包含了答案A等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第一节 油脂背景图课件ppt: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第一节 油脂背景图课件ppt,共54页。PPT课件主要包含了答案C等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第四章 生命中的基础有机化学物质综合与测试复习课件ppt: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第四章 生命中的基础有机化学物质综合与测试复习课件ppt,共19页。PPT课件主要包含了常见有机物的分离方法等内容,欢迎下载使用。













