
苏教版 (2019)必修 第一册专题1 物质的分类及计量第二单元 物质的化学计量练习题
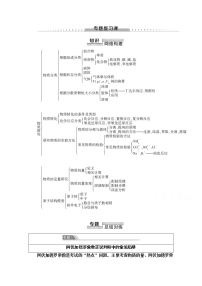
展开1.硫及其化合物的转化关系
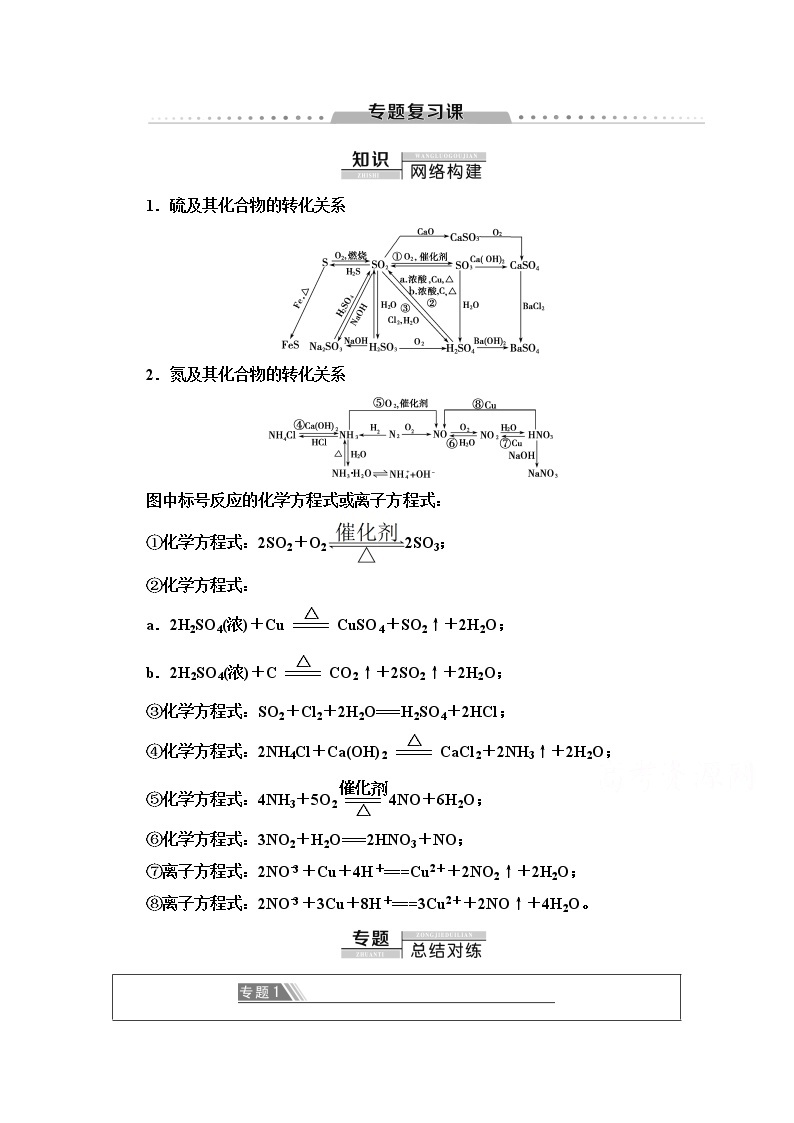
2.氮及其化合物的转化关系
图中标号反应的化学方程式或离子方程式:
①化学方程式:2SO2+O22SO3;
②化学方程式:
a.2H2SO4(浓)+Cueq \(=====,\s\up8(△))CuSO4+SO2↑+2H2O;
b.2H2SO4(浓)+Ceq \(=====,\s\up8(△))CO2↑+2SO2↑+2H2O;
③化学方程式:SO2+Cl2+2H2O===H2SO4+2HCl;
④化学方程式:2NH4Cl+Ca(OH)2eq \(=====,\s\up8(△))CaCl2+2NH3↑+2H2O;
⑤化学方程式:4NH3+5O2eq \(=====,\s\up8(催化剂),\s\d10(△))4NO+6H2O;
⑥化学方程式:3NO2+H2O===2HNO3+NO;
⑦离子方程式:2NOeq \\al(-,3)+Cu+4H+===Cu2++2NO2↑+2H2O;
⑧离子方程式:2NOeq \\al(-,3)+3Cu+8H+===3Cu2++2NO↑+4H2O。
非金属及其化合物是化学知识的重要组成部分:
主要考点有:
(1)碳、硅及其化合物;
(2)氯及其化合物;
(3)氧、硫及其化合物;
(4)氮及其化合物。
常见转化关系:①NH3eq \(――→,\s\up8(O2),\s\d10(催化剂))NOeq \(――→,\s\up8(O2))NO2eq \(――→,\s\up8(H2O))HNO3;
②H2S(S)eq \(――→,\s\up8(O2))SO2eq \(――→,\s\up8(O2),\s\d10(催化剂))SO3eq \(――→,\s\up8(H2O))H2SO4;
③CH4(C)eq \(――→,\s\up8(O2),\s\d10(不完全燃烧))COeq \(――→,\s\up8(O2))CO2eq \(――→,\s\up8(H2O))H2CO3;
④N2eq \(――→,\s\up8(O2))NOeq \(――→,\s\up8(O2))NO2eq \(――→,\s\up8(H2O))HNO3;
⑤SiO2eq \(――→,\s\up8(C))粗Sieq \(――→,\s\up8(Cl2))SiCl4eq \(――→,\s\up8(H2))Si。
1.如图锥形瓶内盛有气体X,胶头滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入锥形瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
A.X是NH3,Y是水
B.X是SO2,Y是NaOH浓溶液
C.X是CO2,Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
C [NH3、HCl都是极易溶于水的气体,SO2能够与NaOH溶液反应,造成锥形瓶内气体压强的急剧减小,气球a在大气压的作用下变大。CO2在水中的溶解度较小,在硫酸溶液中就更小,所以不会使气球a鼓起。]
2.A、B、C、D为中学常见物质且均含有同一种元素,相互转化关系如下(反应条件及其他物质已经略去):
Aeq \(――→,\s\up8(+O2))Beq \(――→,\s\up8(+O2))Ceq \(――→,\s\up8(+H2O))D
(1)若A、B、C、D均为化合物,而且它们的水溶液均能使湿润的蓝色石蕊试纸变红,则D的化学式为:________________________。
写出B→C的化学方程式:______________________________。
(2)若A能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红。则D的化学式为_________________________。
写出A→B的化学方程式:___________________________。
(3)若A为单质,组成元素的原子所含质子的数目小于18,D为强碱,写出C→D的化学方程式:___________________。
[解析] (1)A、B、C、D的水溶液均能使湿润的蓝色石蕊试纸变红,则这几种物质溶于水均显酸性,D为C与水反应的产物,故D为酸。通过一系列氧化而得的酸为H2SO4,则C为SO3。B为SO2,A为H2S。
(2)A能使湿润的红色石蕊试纸变蓝,则A为NH3;推断B为NO,C为NO2,D为HNO3。
(3)若A为单质,D为强碱,A通过两步氧化得C,则A为Na,B为Na2O,C为Na2O2,D为NaOH。
[答案] (1)H2SO4 2SO2+O22SO3
(2)HNO3 4NH3+5O2eq \(=====,\s\up8(催化剂),\s\d10(△))4NO+6H2O
(3)2Na2O2+2H2O===4NaOH+O2↑
1.硝酸的强氧化性的特殊表现
(1)不论浓硝酸还是稀硝酸,都具有强氧化性,且浓硝酸的氧化性比稀硝酸的氧化性强。
(2)在利用HNO3的酸性时,要注意考虑它的强氧化性。
如FeO与稀硝酸反应时的方程式应是3FeO+10HNO3(稀)===3Fe(NO3)3+NO↑+5H2O而不是FeO+2HNO3===Fe(NO3)2+H2O。
(3)硝酸与金属反应时,既表现强氧化性又表现强酸性,可由金属与硝酸反应的关系,求还原产物的化学式或物质的量。
(4)硝酸与铁反应时,由于存在反应Fe+2Fe3+===3Fe2+,当HNO3过量时,产物为Fe(NO3)3;当Fe过量时,产物为Fe(NO3)2;当Fe与HNO3恰好耗尽时,产物可能是Fe(NO3)3或Fe(NO3)2或Fe(NO3)3和Fe(NO3)2的混合物。
(5)浓硝酸与Cu反应时,若Cu过量,反应开始时浓硝酸的还原产物为NO2,但随着反应的进行,硝酸浓度变小,其还原产物将为NO,最终应得到NO2与NO的混合气体,可利用氧化还原过程中化合价升降总数相等的守恒规律求解有关Cu、HNO3和混合气体之间的量的关系。硝酸与其他金属(过量)反应的情况与此类似。
2.浓硫酸的特性
(1)吸水性:浓硫酸具有吸收现成的水(如气体中、液体中的水分子,以及固体中的结晶水等)的性能,原因是H2SO4分子与水分子可形成一系列稳定的水合物。因浓硫酸有吸水性,故不可将其暴露于空气中,防止其吸收空气中的水蒸气。
(2)脱水性:浓硫酸可将许多有机物(尤其是糖类,如:纤维素、蔗糖等)脱水。
(3)强氧化性:它的氧化作用是由H2SO4分子中+6价的硫元素产生的,其还原产物为SO2而不是H2,加热时,大多数金属(Au和Pt除外)可被浓硫酸氧化。一定量的浓硫酸与足量活泼金属(如Zn)发生反应时,开始发生反应:Zn+2H2SO4(浓)eq \(=====,\s\up8(△))ZnSO4+SO2↑+2H2O,当H2SO4的浓度降低后,发生反应:Zn+H2SO4(稀)===ZnSO4+H2↑。
3.下列关于浓硝酸和浓硫酸的叙述正确的是( )
A.都具有吸水性和强氧化性
B.分别露置在空气中,容器内溶质的物质的量浓度都降低
C.常温下能和铝很快反应,放出气体
D.分别露置在空气中,容器内溶质的质量都变小
B [浓硝酸无吸水性,A错误。二者露置于空气中,溶质的物质的量浓度都降低,浓硝酸是由于挥发性,浓硫酸则是吸收空气中的水,B正确、D错误。二者常温下都能使铝钝化,不会产生气体,C错误。]
4.盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2后,则可使铜顺利溶解。该反应的化学方程式为______________________________
____________________________________________________。
(2)在一定体积的10 ml/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 ml,则浓硫酸的实际体积________(填“大于”“等于”或“小于”)180 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为________________________。
(3)根据如图操作及现象推断酸X为________(填序号)。
a.浓盐酸 b.浓硫酸 c.浓硝酸
[解析] (1)根据题意可知,在盐酸存在的条件下,H2O2与铜发生氧化还原反应,H2O2作氧化剂,铜作还原剂。
(2)只有浓硫酸才能和Cu发生氧化还原反应,稀硫酸和Cu不反应,所以被还原的硫酸为0.9 ml时,浓硫酸的实际体积必须大于根据方程式计算的理论值。
(3)将酸X加入铁中,铁粉未见溶解;加水后溶解,说明酸是浓硫酸或浓硝酸;向反应后的溶液中滴加BaCl2溶液,产生白色沉淀,说明是浓硫酸。
[答案] (1)Cu+H2O2+2HCl===2H2O+CuCl2
(2)大于 3Cu+2NOeq \\al(-,3)+8H+===3Cu2++2NO↑+4H2O (3)b常见非金属及其化合物的性质和转化关系
硝酸、硫酸的性质及与金属的反应规律
高中化学苏教版选修4 化学反应原理第三单元 盐类的水解练习题: 这是一份高中化学苏教版选修4 化学反应原理第三单元 盐类的水解练习题,共6页。
高中第一单元 化学反应速率课后作业题: 这是一份高中第一单元 化学反应速率课后作业题,共6页。
苏教版专题一综合复习与测试课后测评: 这是一份苏教版专题一综合复习与测试课后测评,共6页。