






高中化学人教版 (2019)必修 第一册第一节 钠及其化合物备课ppt课件
展开石墨、Cu能导电,是因为含有能自由移动的电子而能够导电。那么,NaCl的水溶液、熔融的硝酸钾等能导电吗?为什么?
生活常识告诉我们,给电器设备通电时,湿手操作容易发生触电事故,这是为什么?
1.电解质:在水溶液中或熔融状态下能够导电的化合物。上述状态下不导电的化合物是非电解质。 例如:H2SO4、NaOH、KNO3等,都是电解质。酸、碱、盐、部分金属氧化物和水是电解质。酒精、苯、二氧化碳等是非电解质。
非电解质:在水溶液中和熔融状态下都不能导电
电解质:在水溶液中或熔融状态下能够导电
非金属氧化物、大部分有机物是非电解质。
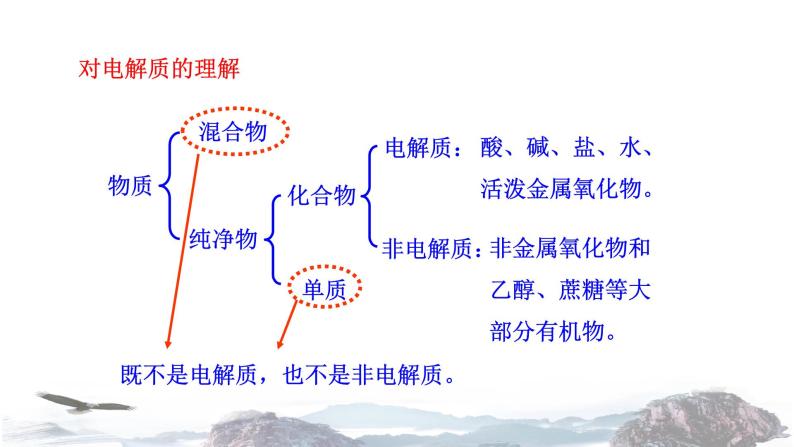
非金属氧化物和乙醇、蔗糖等大部分有机物。
酸、碱、盐、水、活泼金属氧化物。
(2)1 ml/L的NaCl溶液和1 ml/L的FeCl3溶液的导电能力相同吗?
(1)铁丝和盐酸能导电,所以二者是电解质,液态硫 酸不导电,所以硫酸是非电解质,对吗?并分析。
答案:(1)不对。因为电解质和非电解质都是化合物,而铁是单质,盐酸是混合物,故两者既不是电解质,也不是非电解质;硫酸溶液能导电,硫酸是电解质。
答案:(2)不同。因其自由离子浓度及所带电荷不同。
SO2属于化合物,溶于水也能导电,SO2属于电解质吗?
电解质是指在水溶液中或熔融状态下能自身电离而导电的化合物。SO2溶于水导电是因为生成H2SO3,电离产生自由移动的离子而导电,应该理解为H2SO3是电解质,SO2属于非电解质。
①单质、混合物既不是电解质,也不是非电解质。电解质、非电解质都是化合物。②电解质导电须有外界条件:水溶液或熔融状态。③电解质因本身离解成自由离子而导电。某些化合物,像SO2、CO2、NH3,它们的水溶液虽能导电,但它们不是电解质。④某些难溶于水的化合物。如BaSO4、AgCl等,由于它们的溶解度太小,难测其水溶液的导电性,但这些难溶于水的化合物和部分金属的氧化物,它们在熔融状态都是能够导电的,所以是电解质。⑤酸、碱、大多数盐、活泼金属的氧化物(Na2O 、Al2O3)都是电解质;除电解质外的化合物都是非电解质,如大多数有机物和非金属氧化物等。
⑴金属铜 ⑵碳棒 ⑶O2 ⑷H2SO4 ⑸液态HCl ⑹CH3COOH ⑺葡萄糖 ⑻固态NaCl ⑼CaCO3固体 ⑽CuSO4·5H2O ⑾熔融状态的KNO3 ⑿KOH水溶液 ⒀酒精水溶液 ⒁盐酸 ⒂CaO ⒃CO2 ⒄H2O ⒅NH3
能导电:电解质:非电解质:
1.下列物质哪些能导电?哪些是电解质?哪些是非电解质?
为什么NaCl、KNO3在水溶液里或熔融状态下能够导电?而固体不导电?
NaCl在水中的溶解和电离的示意图
物质导电条件:自由移动带电荷的粒子
电解质固体离子不能自由移动,所以不导电,而在水溶液中或熔融状态可以自由移动,故导电。
用化学符号表示电解质电离成自由移动离子的过程。如:NaCl == Na++Cl-
现在你知道电解质溶液能导电和非电解质不能导电的原因了吗?
(1)概念:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
(2)电离的表示——电离方程式
电解质和非电解质在水中电离的比较
2.下列电离方程式正确的是:
A、MgSO4=Mg+2 +SO4-2B、Ba(OH)2=Ba2++OH2-C、Al2(SO4)3=2Al3++3SO42-D、Ca(NO3)2=Ca2++NO3-
在溶液中,离子浓度越大,离子所带的电荷越多,溶液导电能力就越强。
NaCl ==== Na+ + Cl-
离子符号(代表水合离子)
◆如何正确书写电离方程式?
Al2(SO4)3==2Al3++3SO42-
(2)书写步骤:①阴阳离子部分拆开写,但原子团不能拆,例如NO3-、SO42-、OH-、NH4+、CO32-等不能拆。②构成物质的原子或原子团的个数在书写成离子时为化学计量数。
①式子左边书写化学式,表示电解质还未电离时的状态;右边书写离子符号,表示电解质电离产生的离子。
②离子所带的电荷数应等于元素或原子团的化合价数。
③电离方程式左右两边正负电荷之和相等。
下列电离方程式正确的是( )A.MgCl2==Mg2++Cl2-B.NaHCO3==Na++H++CO32-C.H2SO4==H 2++SO42-D.Ba(OH)2==Ba2++2OH-
【提示】NaHCO3 的第一步电离应该电离出Na+和HCO3- 。
1.写出下列酸的电离方程式: HCl 、HNO3、H2SO4
H2SO4==2H+ +SO42-
HCl == H+ +Cl-
HNO3== H+ +NO3-
▲酸:电离时生成的阳离子全部是H+的化合物。
1.写出下列碱的电离方程式: NaOH、KOH、Ba(OH)2
NaOH == Na+ + OH-
2.碱:电离时生成的阴离子全部是OH-的化合物。
Ba(OH)2 == Ba2+ + 2OH-
Ca(OH)2 == Ca2+ + 2OH-
写出下列盐的电离方程式: NaCl、KNO3、Fe2(SO4)3、NaHSO4
NaCl == Na+ + Cl-
▲盐:电离时能生成金属离子和酸根离子的化合物。
KNO3 == K+ + NO3-
Fe2(SO4)3 == 2Fe3+ + 3SO42-
NaHSO4==Na+ + H+ + SO42-
1.电解质:在水溶液里或熔融状态下能够导电的化合物。非电解质:在水溶液里和熔融状态下均不导电的化合物。
3.酸、碱、盐的实质。
1.下列物质中属于电解质的是( )A.铜 B.盐酸 C.稀硫酸 D.硝酸2.下列说法正确的是( )A.电解质都是易溶于水的物质B.氧化物都是电解质C.氢化物都不是电解质D.酸、碱、盐都是电解质
3.下列电离方程式正确的是( ) A.Na2CO3==Na+ + CO32- B.Ca(NO3)2==Ca2+ + NO32- C.KAl(SO4)2==K+ + Al3+ + 2SO42- D.H2SO4==2H+ + S6+ + 4O2-
4.根据电离方程式判断,下列物质中是酸的是( ) A.KOH == K+ + OH- B.HI == I- + H+ C.NaHSO4 == Na+ + H+ + SO42- D.Ba(OH)Cl == Ba2+ + OH- +Cl-
鲁科版 (2019)必修 第一册第2节 电解质的电离 离子反应课文课件ppt: 这是一份鲁科版 (2019)必修 第一册第2节 电解质的电离 离子反应课文课件ppt,共46页。PPT课件主要包含了知识网络,学业基础,不导电,水溶液,能够导电,溶于水,受热熔化,自由移动的离子,OH-,酸根离子等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 离子反应课文ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 离子反应课文ppt课件,共13页。PPT课件主要包含了2实验过程,灯泡不亮,无电流产生,KNO3固体都不导电,灯泡变亮,有电流产生,都能导电,氯化钠溶液导电,有自由移动的离子,电离方程式等内容,欢迎下载使用。
2020-2021学年第二节 离子反应优秀课件ppt: 这是一份2020-2021学年第二节 离子反应优秀课件ppt,共30页。PPT课件主要包含了熔融状态,水溶液状态,铜能导电,电解质,电解质与非电解质,非电解质,熔融状态下导电,④⑥⑧,①③④⑤⑨,①②④⑥⑧等内容,欢迎下载使用。













