
【化学】江苏省公道中学2018-2019学年高一上学期期末考试试卷
展开江苏省公道中学2018-2019学年高一上学期期末考试试卷
2019.01
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Fe-56 Ba-137
选择题(共40分)
选择题(本题包括20小题,每题2分,共40分。每小题只有一个选项符合题意)
1.2018年世界环境日中国主题是“美丽中国,我是行动者”。下列行为符合该主题的是( )
A.尽量乘坐公共交通工具 B.大量使用农药
C.大力开采化石燃料 D.推广使用一次性塑料餐具
2.对于2Na + 2H2O=2NaOH + H2↑,下列说法正确的是( )
A.Na+的结构示意图:
B.H2的摩尔质量:2 g·mol-1
C.H2O中O的化合价:-1
D.NaOH电离方程式:NaOH=Na+ + O2- + H+
3.可用于辐照治疗癌症,下列关于说法正确的是( )
A.核电荷数为138 B.核外电子数为226
C.中子数为50 D.与互为同位素
4.用一束光照射某液体,产生一条光亮的通路。该液体是( )
A.NaCl溶液 B.Fe(OH)3胶体 C.水 D.稀硫酸
5.硅酸钠(Na2SiO3)溶液在建筑上可用作防腐剂与粘合剂,硅酸钠属于( )
A.酸 B.碱 C.盐 D.氧化物
6.下列属于化学变化的是( )
A.碘升华 B.冰块粉碎
C.铜生锈 D.浓盐酸挥发
7.下列有关工业生产的叙述中正确的是( )
A.电解氯化钠溶液可得到金属钠
B.光照氯气和氢气的混合物生产盐酸
C.从铝土矿到铝单质过程中未涉及氧化还原反应
D.工业接触法制硫酸的主要设备有沸腾炉、接触室、吸收塔
8.下列各组离子在溶液中能大量共存的是( )
A.Mg2+、K+、OH- B.Ba2+、Na+、SO
C.K+、HCO、OH- D.K+、Cu2+、NO
9.下列有关物质的性质与用途具有对应关系的是( )
A.MgO具有高熔点,可用于制耐火材料
B.NaHCO3受热易分解,可用于治疗胃酸过多
C.金属铜具有金属光泽,可用作导电材料
D.浓硫酸具有脱水性,可用作干燥剂
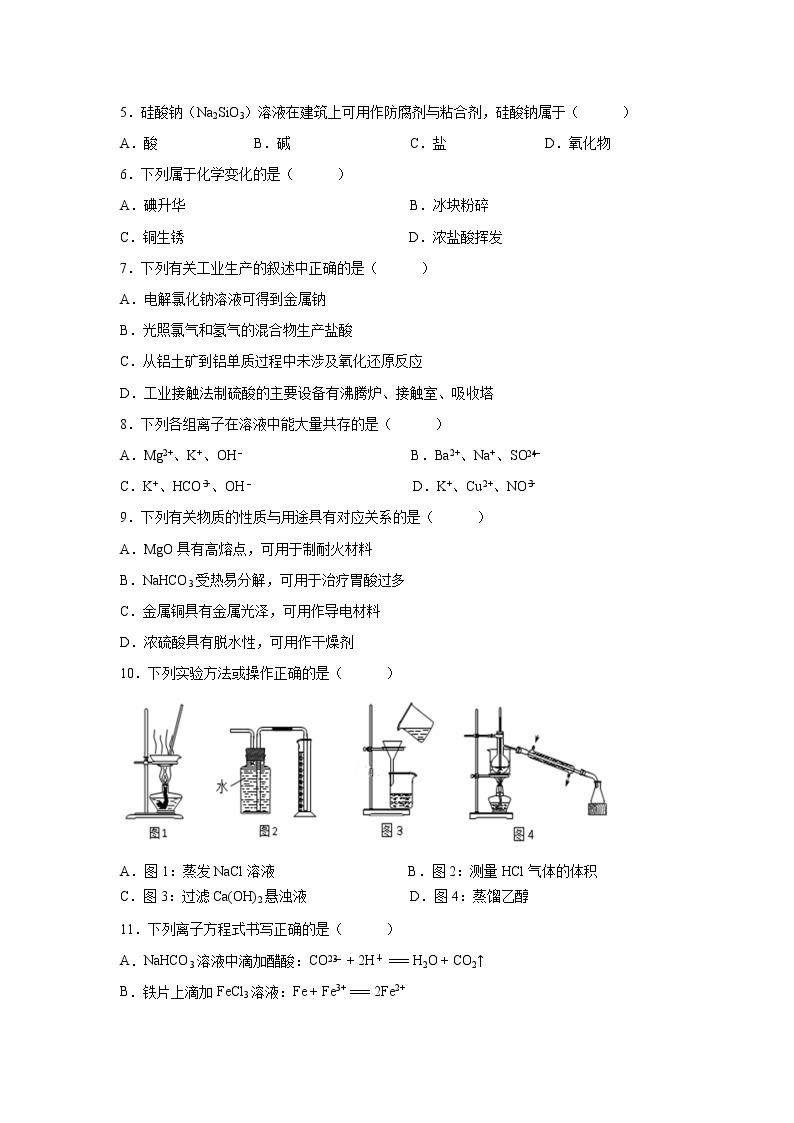
10.下列实验方法或操作正确的是( )
A.图1:蒸发NaCl溶液 B.图2:测量HCl气体的体积
C.图3:过滤Ca(OH)2悬浊液 D.图4:蒸馏乙醇
11.下列离子方程式书写正确的是( )
A.NaHCO3溶液中滴加醋酸:CO + 2H+=H2O + CO2↑
B.铁片上滴加FeCl3溶液:Fe + Fe3+=2Fe2+
C.AlCl3溶液中加入氨水:Al3+ + 3NH3•H2O=Al(OH)3↓+ 3NH
D.氯气通入NaOH溶液中:Cl2 + OH-=Cl- + ClO- + H2O
12.以下六项中需在容量瓶上标出的是( )
①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
A.①②④ B.②③⑤
C.①⑤⑥ D.①③⑤
13.含Na2SO4、MgSO4和NaNO3的1 L混合溶液,已知其中c(Mg2+)= 0.4 mol· L-1,c(SO)= 0.7 mol· L-1,c(NO)=0.2 mol·L-1,则此溶液中c(Na+)为( )
A.0.2 mol·L-1 B.0.4 mol·L-1
C.0.6 mol· L-1 D.0.8 mol· L-1
14.用无水Na2CO3配制250 mL 1.000 mol·L-1 Na2CO3溶液时,下列操作会使配制的溶液浓度偏大的是( )
A.称量时碳酸钠固体含有结晶水
B.移液时有液滴洒落瓶外
C.定容时俯视容量瓶刻度线
D.容量瓶没有干燥
15.分离提纯下列物质时选用的试剂或方法不正确的是( )
| 分离提纯 | 试剂 | 方法 |
A | 除去Cl2中的HCl | NaOH溶液 | 洗气 |
B | 提取溴水中的溴单质 | CCl4 | 萃取 |
C | 除去SiO2中的Fe2O3 | 稀盐酸 | 过滤 |
D | 除去H2O中的 Fe3+ | — | 蒸馏 |
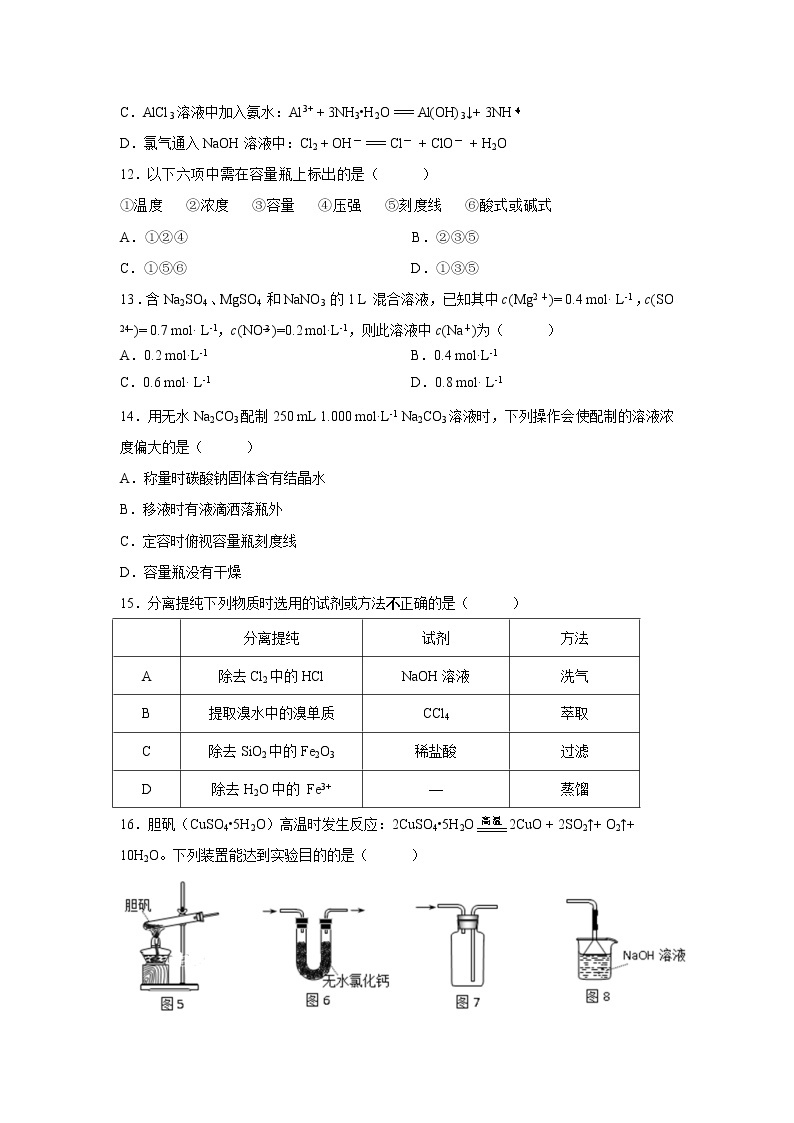
16.胆矾(CuSO4•5H2O)高温时发生反应:2CuSO4•5H2O2CuO + 2SO2↑+ O2↑+ 10H2O。下列装置能达到实验目的的是( )
A.图5装置可用于胆矾分解
B.图6装置可用于检验产物是否含H2O
C.图7装置可用于收集SO2
D.图8装置可用于吸收胆矾分解的SO2
17.在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.
B.
C.
D.
18.工业制备高铁酸钾的离子方程式为:2Fe(OH)3+3ClO-+4OH-2FeO+3Cl-+5H2O。关于该反应的说法正确的是( )
A.FeO中铁显+3价 B.ClO-发生还原反应
C.Fe(OH)3是氧化剂 D.ClO-失去电子
19.下列有关离子检验的操作及结论均正确的是( )
A.向无色溶液中先加适量盐酸酸化,再加AgNO3溶液,产生白色沉淀,则该溶液中一定含有Cl-
B.向无色溶液中加入BaCl2溶液有白色沉淀出现,再加盐酸,沉淀不消失,则该溶液中一定含有SO
C.向无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,则该溶液中一定含有CO
D.向某溶液中加入氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,则该溶液中一定含有NH
20.聚合硫酸铁[Fex(OH)y(SO4)z](铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL的溶液。
②准确量取25.00 mL溶液,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体6.99g。
③准确量取25.00mL溶液,加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥、灼烧至恒重,得到红棕色固体1.92g。
该聚合硫酸铁组成中x∶y∶z的值为( )
A.6∶8∶5 B.4∶2∶5 C.1∶1∶2 D.6∶3∶5
非选择题(共60分)
21.(8分)按要求进行计算,直接写出结果
(1)标准状况下,2.24 L CH4所含氢原子的物质的量为 ▲ mol。
(2)含0.2 mol氧原子的NO2的质量是 ▲ g。
(3)100 mL 0.5mol· L-1 H2SO4溶液中,H+的物质的量浓度为 ▲ mol· L-1。
(4)1mol碳在一定量氧气中反应,生成气体的质量为36 g。所得气体的物质的量为 ▲ mol。
22.(8分)有关物质的转化关系如下图所示。A、C、E是常见的金属单质,E为紫红色,反应①可用于焊接铁轨,B是赤铁矿的主要成分,F的溶液中加入KSCN溶液变红。(部分反应物和生成物省略)
请回答下列问题:
(1)D的化学式是 ▲ 。
(2)可选用 ▲ (填“字母”)实现反应C→F的转化。
a.稀盐酸 b.氯气/点燃 c.CuSO4溶液
(3)反应①的化学方程式为 ▲ 。
(4)反应②的离子方程式为 ▲ 。
23.(10分)转鼓指数是反映烧结矿的机械强度的物理性能指标,其值越大,机械强度越好。某炼钢厂的工业废渣中主要含有Al2O3、Fe2O3、SiO2,对该废渣进行处理来获取活性氧化铝,其流程如下:
(1)烧结时往往需要加入MgO以提高烧结产物的转鼓指数,右图是转鼓指数与MgO含量的关系曲线。根据此图可知,最适宜的MgO含量是 ▲ %。
(2)烧结产物主要有NaAlO2、Ca2SiO4、NaFeO2及气体X。气体X是 ▲ 。
(3)碱浸前需将烧结产物进行粉碎,其目的是 ▲ 。碱浸过程中,NaFeO2可与水反应生成NaOH和一种含铁的化合物,该含铁的化合物是 ▲ 。
(4)酸化时发生反应的离子方程式是 ▲ 。
24.(12分)某兴趣小组用如图所示装置进行实验,探究铁和浓硫酸反应的产物及性质。(夹持装置已略,气密性已检验)
实验开始前,先打开活塞K通一段时间N2。关闭活塞K后,向A中滴加一定量的浓硫酸,加热观察到A中铁片上有气泡产生。
请回答下列问题:
(1)仪器a的名称是 ▲ 。实验开始前,先通一段时间N2的目的是 ▲ 。
(2)加热一段时间后发现B装置中溶液褪色,说明有 ▲ (填化学式)生成。再取出A中反应后的溶液少许,加入KSCN溶液未出现血红色,浓硫酸与铁反应的化学方程式是 ▲ 。
(3)C装置中 ▲ (填“有”或“无”)沉淀生成。D中溶液紫色褪去,体现气体产物的 ▲ 性(填“氧化”、“还原”或“漂白性”)。
(4)E装置的作用是 ▲ 。(用离子方程式表示)
25.(12分)硫有多种化合物,如H2S、COS(羰基硫)、SO2等,它们对环境均有一定的影响。
(1)H2S经 K2CO3溶液吸收后,生成两种酸式盐。其中任意一种酸式盐的化学式是 ▲ 。
(2)COS(羰基硫)燃烧时有SO2生成,其原理为:2COS+3O22CO2+2SO2。若转移3.612×1024个电子,则参加反应COS(羰基硫)的物质的量是 ▲ mol。
(3)电厂排出的烟气中含有CO、SO2等。SO2能与H2S反应生成S和H2O,说明SO2具有 ▲ 性。CO在催化剂存在时可与SO2反应,转化为一种固体和一种无害气体。该反应的化学方程式是 ▲ 。
(4)石灰石作为脱硫剂,可有效吸收废气中的SO2,减少酸雨的产生。
①在煤炭中加入石灰石可减少燃烧时SO2的排放量,并生成CaSO4。该反应的化学方程式是 ▲ 。
②你认为减少酸雨产生的途径可采取的措施是 ▲ (填序号)。
a.避免直接用高硫煤作燃料 b.把工厂的烟囱造高
c.燃料脱硫 d.开发新能源
26.(10分)ClO2气体是一种优良的消毒剂,常用于自来水的消毒。
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2。
(1)工业上常将ClO2制备成NaClO2固体以便运输和贮存,流程如下:
①吸收器中,H2O2的作用是 ▲ 。(填“氧化剂”或“还原剂”)。
②在吸收器反应时应控制温度低于5℃的原因是: ▲ 。
③操作a: 55℃蒸发至有大量晶体析出、 ▲ 、用介于38℃~60℃的温水洗涤、低于60℃干燥,得到NaClO2固体。
(2)将ClO2溶于水得到溶液,为测定其浓度,进行以下实验操作:
步骤1:取待测ClO2溶液20.00mL于锥形瓶中;
步骤2:用稀H2SO4调节溶液pH <2.0,加入足量的KI晶体充分反应;
步骤3:加入几滴淀粉溶液,逐滴加入0.1 mol· L-1的Na2S2O3溶液,恰好完全反应时,消耗Na2S2O3溶液20.00mL;
已知:2ClO2+10KI+4H2SO4=2KCl+5I2+4K2SO4+4H2O,I2+2Na2S2O3=Na2S4O6+2NaI
试计算溶液中ClO2的物质的量浓度(写出计算过程)。
▲
【参考答案】
选择题(共40分)
选择题(本题包括20小题,每题2分,共40分。每小题只有一个选项符合题意)
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
A | B | D | B | C | C | D | D | A | A |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
C | D | D | C | A | D | C | B | D | B |
非选择题(共60分)
21.(8分)
(1)0.4 (2) 4.6 (3) 1 (4) 1
22.(8分)
(1)Al2O3 (2)b
(3)2Al+Fe2O32Fe + Al2O3 (4)Cu + 2Fe3+= Cu2+ + 2Fe2+
23.(10分)
(1)2.4 (2)CO2
(3)增大反应物接触面积,加快反应速率,提高烧结产物的浸出率 Fe(OH)3
(4)AlO + CO2+ 2H2O= Al(OH)3↓+HCO
24.(12分)
(1)分液漏斗 排除装置中的空气
(2)SO2 Fe + 2H2SO4(浓) FeSO4 + SO2↑+ 2H2O
(3)无 (1分) 还原(1分)
(4)SO2+ 2OH= SO + H2O
25.(12分)
(1)KHS或 KHCO3
(2)1
(3)氧化 SO2+ 2CO S + 2CO2
(4)① 2CaCO3 + 2SO2 + O2 2CaSO4 + 2CO2 ②acd(漏选1个得1分)
26.(10分)
(1)①还原剂 ②防止温度过高H2O2分解,或ClO2气体溶解度随温度升高而降低(答出一点即可)③趁热过滤
(2)n(I2)=n(Na2S2O3)=×0.1 mol· L-1×20.00×10-3L=1×10-3mol(1分)
n(ClO2)= n(I2) =×1×10-3mol =4×10-4mol(2分)
∴c(ClO2)= =0.02mol· L-1(1分) 其他合理解法也可得分








