

2018-2019学年甘肃省甘谷第一中学高二下学期期末考试化学试题 word版
展开甘谷一中2018—2019学年第二学期期末考试
高二化学试卷
相对原子质量:C:12 H:1 O:16 Cl: 35.5
一、选择题(每小题只有一个选项符合题意,每小题2分,共计44分)
1.下列说法不正确的是( )
A.油脂有油和脂肪之分,但都属于酯
B.糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应
C.葡萄糖既可以与银氨溶液反应,又可以与新制氢氧化铜悬浊液反应
D.天然油脂是混合物,没有固定的熔点和沸点
2. 下列表述正确的是
A. 羟基的电子式 B. 醛基的结构简式—COH
C. 1-丁烯的键线式 D. 聚丙烯的结构简式
3.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均可行的是( )
编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
A | 己烷(己烯) | 溴水 | 分液 |
B | 淀粉溶液(NaCl) | 水 | 过滤 |
C | 甲苯(乙酸) | NaOH溶液 | 分液 |
D | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
4.某有机物分子结构式如下图,下列说法正确的是( )
A.取少量该有机物,滴加酸性高锰酸钾溶液,微热,有气体产生
B.所有的碳原子不可能处在同一个平面上
C.所有的氧原子不可能同时处在苯环平面上
D.所有的氢原子有可能同时处在苯环平面上
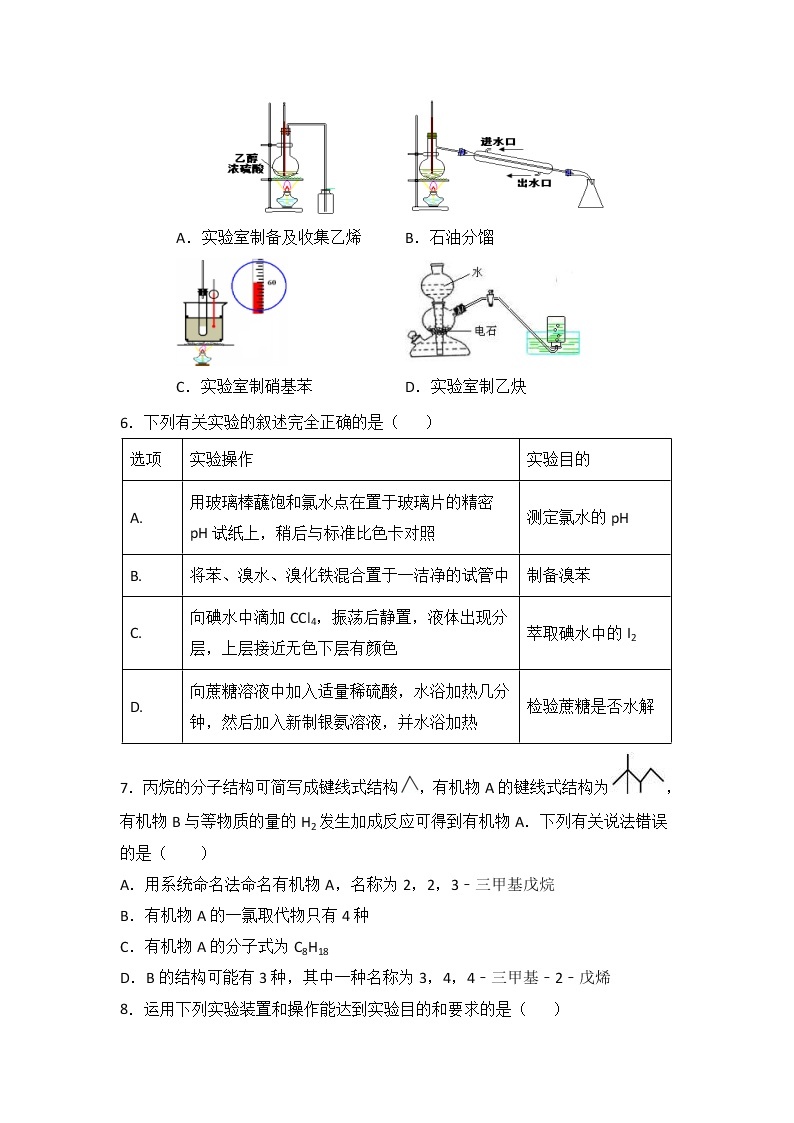
5.下列实验装置图正确的是( )
A.实验室制备及收集乙烯 | B.石油分馏 |
C.实验室制硝基苯 | D.实验室制乙炔 |
6.下列有关实验的叙述完全正确的是( )
选项 | 实验操作 | 实验目的 |
A. | 用玻璃棒蘸饱和氯水点在置于玻璃片的精密pH试纸上,稍后与标准比色卡对照 | 测定氯水的pH |
B. | 将苯、溴水、溴化铁混合置于一洁净的试管中 | 制备溴苯 |
C. | 向碘水中滴加CCl4,振荡后静置,液体出现分层,上层接近无色下层有颜色 | 萃取碘水中的I2 |
D. | 向蔗糖溶液中加入适量稀硫酸,水浴加热几分钟,然后加入新制银氨溶液,并水浴加热 | 检验蔗糖是否水解 |
7.丙烷的分子结构可简写成键线式结构,有机物A的键线式结构为,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
A.用系统命名法命名有机物A,名称为2,2,3﹣三甲基戊烷
B.有机物A的一氯取代物只有4种
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种名称为3,4,4﹣三甲基﹣2﹣戊烯
8.运用下列实验装置和操作能达到实验目的和要求的是( )
A.分离氯化铵和单质碘 B.除去淀粉胶体中混有的氯化钠
C.加热胆矾(CuSO4·5H2O)制取无水硫酸铜 D.除去SO2中的HCl
9.化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( )
A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1 mol化合物X最多能与2 mol NaOH反应
10.为了证明醋酸是弱电解质,某同学开展了题为“醋酸是弱电解质的实验探究”的探究活动。该同学设计了如下方案,其中错误的是( )
A.先配制0.10 mol/L CH3COOH溶液,再测溶液的pH,若pH大于1,则可证明醋酸为弱电解质
B.先配制0.01 mol/L和0.10 mol/L的CH3COOH,再分别用pH计测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸是弱电解质
C.取等体积、等pH的CH3COOH的溶液和盐酸分别与足量锌反应,测得反应过程中醋酸产生H2速率较慢且最终产生H2较多,则可证明醋酸为弱电解质
D.配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质
11.探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L−1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① | Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 | |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是( )
A.H2C2O4有酸性,Ca(OH)2+ H2C2O4=CaC2O4↓+2H2O
B.酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4=NaHC2O4+CO2↑+H2O
C.H2C2O4具有还原性,2+5+16H+=2Mn2++10CO2↑+ 8H2O
D.H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OHC2H5OOCCOOC2H5+2H2O
12.某有机物A由C、H、O三种元素组成,相对分子质量为90。将9.0gA完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,A能与NaHCO3溶液反应,且2分子A之间脱水可生成六元环化合物。有关A的说法正确的是( )
A.分子式是C3H8O3
B.0.1molA与足量Na反应产生2.24LH2 (标准状况)
C.A催化氧化的产物能发生银镜反应
D.A在一定条件下发生缩聚反应的产物是:
13.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.常温常压下,0.1mol C3H8所含有的共价键数目为1.1NA
B.1mol苯分子中,含有碳碳双键的数目为3NA
C.常温常压下,15g甲基(-CH3)所含的电子数为10NA
D.现有乙烯、丙烯的混合气体共14g,其原子数为3NA
14.DAP是电器和仪表部件中常用的一种合成高分子化合物,它的结构简式为:
则合成此高分子的单体可能是( )
①乙烯CH2=CH2 ②丙烯CH3CH=CH2 ③丙烯醇HOCH2CH=CH2
④ 邻苯二甲酸 ⑤邻苯二甲酸甲酯
A.①② B.③④ C.②④ D.③⑤
15.某芳香族化合物甲的分子式为C10H11ClO2,已知苯环上只有两个取代基,其中一个取代基为Cl,甲能与饱和碳酸氢钠溶液反应放出二氧化碳,则满足上述条件的有机物甲的同分异构体数目为
A.8种 B.12种 C.14种 D.15种
16.由醇X制备羧酸Z的合成路线如图所示,不正确的是( )
A.Y的结构有4种
B.X、Z能形成戊酸丁酯,戊酸丁酯最多有16种
C.与X互为同分异构体,且不能与金属钠反应的有机物有4种
D.与Z互为同分异构体,且能发生水解反应的有机物有9种
17.某有机物的结构为右图所示,这种有机物不可能具有的性质是 ( )
①可以燃烧 ②能使酸性KMnO4溶液褪色
③能跟NaOH溶液反应 ④能跟新制银氨溶液反应
⑤能发生加聚反应 ⑥能发生水解反应
A.只有⑥ B.①④ C.只有⑤ D.④⑥
18.奎宁酸和莽草酸是高等植物特有的脂环状有机酸常共存在一起,其结构简式如图所示。下列说法正确的是( )
A. 奎宁酸与莽草酸互为同分异构体
B. 两种酸含有的官能团完全相同
C. 两种酸均能发生加成反应、聚合反应和取代反应
D. 等物质的量的两物质分别与足量Na反应,同温同压下产生H2的体积比为5:4
19.分别燃烧等物质的量的下列各组物质,其中消耗氧气量相等的是
①C2H2与 CH3CHO ②C7H8与C6H12 ③C2H2与C6H6 ④HCOOCH3与CH3COOH,
A.①②③④ B.①④ C.①②④ D.②④
20.两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
①一定有乙烯;②一定有甲烷;③一定有丙烷;④一定无乙烷;⑤可能有乙烷;⑥可能有丙炔。
A.②③⑤ B.⑤⑥ C.①② D.②④⑥
21.烯烃或炔烃在酸性高锰酸钾溶液作用下,分子中的不饱和键完全断裂,此法可用于减短碳链或利用产物反推不饱和烃的结构等.已知烯烃与酸性 KMnO4溶液反应的氧化产物的对应关系为
烯烃被氧化的部位 | CH2═ | RCH═ | |
氧化产物 | CO2 | RCOOH |
现有某烯烃与酸性KMnO4溶液作用后得到的氧化产物有CO2、乙二酸(HOOC﹣COOH)和丙酮( ),则该烯烃结构简式可能是( )
A. B.
C.CH2=CH﹣CH=CHCH2CH3 D.
22.已知酸性: > H2CO3 > ,综合考虑反应物的转化率和原料成本等因素,将 转变为的最佳方法是( )
A.与稀H2SO4共热后,加入足量的NaOH溶液
B.与稀H2SO4共热后,加入足量的Na2CO3溶液
C.与足量的NaOH溶液共热后,再通入足量CO2
D.与足量的NaOH溶液共热后,再加入适量H2SO4
二、非选择题(共56分)
23.(9分)(1)有下列几种物质:
A:石墨和C60
B:35Cl和37Cl
C:CH3CH=CHCH3和(CH3)2C=CH2
D.
E.间二甲苯和异丙苯
请把合适字母填入以下横线里:
①属于同分异构体的是______________________
②属于同系物的是__________________________
③属于同种物质的是________________________
(2)下图是某药物中间体的结构示意图
试回答下列问题:
①观察上面的结构简式图1与立体模型图2,通过对比指出结构简式中的“Et”表示
_______________________(填名称),该药物中间体分子的化学式为___________,
②现有一种芳香化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如
上图所示,试写出该化合物的结构简式:_________________________________。
24.(12分)Ⅰ. 实验室制得气体中常含有杂质,影响其性质检验。
下图A为除杂装置,B为性质检验装置,完成下列表格:
序号 | 气体 | 反应原理 | A中试剂 |
① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | ______________ |
② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是_________________ | NaOH溶液 |
③ | 乙炔 | 电石与饱和食盐水反应 | _______________ |
Ⅱ. 为探究乙酸乙酯的水解情况,某同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
编号 | ① | ② | ③ |
实验操作 | |||
实验现象 | 酯层变薄 | 酯层消失 | 酯层基本不变 |
(1)试管①中反应的化学方程式是________________________;
(2)对比试管①和试管③的实验现象,稀H2SO4的作用是_________________;
(3)试用化学平衡移动原理解释试管②中酯层消失的原因_____________。
25.(14分)氯苯在染料医药工业中用于制造苯酚、硝基氯苯、苯胺、确基酚等有机中间体。实验室中制备氯苯的装置如下图所示(夹持仪器已略去)。
请回答下列问题:
(1)仪器a中盛有KMnO4晶体,仪器b中盛有浓盐酸.打开仪器b中的活塞,使浓盐酸缓缓滴下,可观察到仪器a内的现象是 ,用离子方程式表示产生该现象的原因: .
(2)仪器b外侧玻璃导管的作用是 .
(3)仪器d内盛有苯,FeCl3粉末固体,仪器a中生成的气体经过仪器e进入到仪器d中.
①仪器e的名称是 ,其盛装的试剂名称是 .
②仪器d中的反应进行过程中,保持温度在40~60℃,以减少副反应发生.仪器d的加热方式最好是 加热,其优点是 .
(4)仪器c的作用是 .
(5)该方法制备的氯苯中含有很多杂质,工业生产中,通过水洗除去FeCl3,HCl及部分Cl2,然后通过碱洗除去Cl2;碱洗后通过分液得到含氯苯的有机物混合物,混合物成分及沸点如表一:
表一
有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
沸点/℃ | 80 | 132.2 | 180.4 | 173.0 | 174.1 |
从该有机物混合物中提取氯苯时,采用蒸馏的方法,收集 ℃作用的馏分.
(6)实际工业生产中,苯的流失如表二:
表二:
流失项目 | 蒸气挥发 | 二氯苯 | 其他 | 合计 |
苯流失量(kg/I) | 28.8 | 14.5 | 56.7 | 100 |
某一次投产加入13t苯,则制得氯苯 t(保留一位小数).
26.(10分)聚合物F的合成路线图如下:
请据此回答:
(1)A中含氧官能团名称是_____,D的系统命名为_____。
(2)检验B中含氧官能团所用的试剂是____;A→B的反应类型是_____。
(3)C生成D的反应化学方程式为_______,E合成F的反应化学方程式为________。
(4)G物质与互为同系物,且G物质的相对分子质量比大14的,则符合下列条件的G的同分异构体有____种。
①分子中含有苯环,且苯环上有两个取代基
②遇氯化铁溶液变紫色
③能与溴水发生加成反应
27.(11分)A(C3H6)是基本有机化工原料,由A制备聚合物C和合成路线如图所示(部分条件略去)。
已知:
(1)(1)发生缩聚形成的高聚物的结构简式为__________;D-E的反应类型为__________。
(2)E-F的化学方程式为________________________________________。
(3)B的同分异构体中,与B具有相同官能团且能发生银镜反应,其中核磁共振氢谱上显示3组峰,且峰面积之比为6:1:1的是________________(写出结构简式)。
(4)等物质的量的分别与足量NaOH、Na2CO3、NaHCO3反应, 消耗NaOH、Na2CO3 、NaHCO3的物质的量之比为________________;检验的碳碳双键的方法是________________(写出对应试剂及现象)。
高二化学期末考试参考答案
1-5:BCCAC 6-10:CBBCC 11-15:CBDBD 16-20CADCD 21-22DC
23.(9分)
(1)①C ②E ③D(每空各1分)
(2)①乙基(2分) ②C9H12O3 (2分) ③ (2分)
24.(12分,每空2分)
Ⅰ. (1)水 (2)
(3)溶液
Ⅱ. (1)CH3COOCH2CH3+H2OCH3COOH+CH3CH2OH
(2)稀硫酸可以加速酯的水解(或稀硫酸是酯水解反应的催化剂)
(3)乙酸乙酯水解生成的乙酸与NaOH发生中和反应,乙酸浓度降低,使水解平衡向正反应方向移动,水解比较彻底。
25.(14分)(1) 2MnO4﹣+10Cl﹣+16H+=2Mn2++5Cl2↑+8H2O (2分).
(2) 使浓盐酸能顺利滴下(或答“平衡仪器a、b内的气压”) (2分) .
(3)① 洗气瓶 , 浓硫酸 .(2分)
② 水浴 ;受热均匀,易于控制温度 (2分)
(4) 冷凝、回流(2分)
(5)132.2 (2分)
(6) 16.9 (2分)
26.(10分)
(1)醛基 (1分) 1,2-丙二醇 (1分)
(2) NaHCO3溶液(或Na2CO3) (1分) 氧化反应 (1分)
(3)CH3CHBrCH2Br+2NaOHCH3CH(OH)CH2OH+2NaBr
(4)9
27. (11分)
(1) (2分) 取代反应 (1分)
(2) (2分)
(3) (2分)
(4) 1:1:1 (2分) 加入溴水,溴水褪色 (2分)








