


- 【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题01 硫及其化合物(考点专练)(8大题型).zip 试卷 0 次下载
- 【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题01 硫及其化合物(考点梳理+练习).zip 试卷 0 次下载
- 【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题02 氮及其化合物(考点梳理+练习).zip 试卷 0 次下载
- 【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题03 常见气体的实验室制取(考点专练)(6大题型).zip 试卷 0 次下载
- 【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题03 常见气体的实验室制取(考点梳理+练习).zip 试卷 0 次下载
【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题02 氮及其化合物(考点专练)(8大题型).zip
展开01 氮的固定
【例1】(23-24高一上·福建三明·月考)下列不属于氮的固定过程的是
A.工业合成氨
B.雷雨天气中,N2 与 O2 在闪电作用下转化为 NO
C.硝酸见光分解
D.豆科植物根瘤菌吸收氮
【答案】C
【解析】A.工业合成氨是氮气和氢气在适宜条件下合成氨,氮由游离态转化为化合态,属于氮的固定,A正确;
B.雷雨闪电时,氮气和氢气合成氨气,氮由游离态转化为化合态,属于氮的固定,B正确;
C.硝酸见光分解属于不同化合态的氮之间的转化,C错误;
D.根瘤菌把氮气转化为氨,氮由游离态转化为化合态,属于氮的固定,D正确;
故选C。
【变式1-1】(22-23高一下·江苏盐城·月考)下列变化属于氮的固定的是
A.工业上用氨气和硝酸合成硝酸铵B.氮气和氧气在放电条件下生成NO
C.氨气与氯气反应生成氮气D.氯化铵受热分解生成氨气和氯化氢
【答案】B
【解析】A.是含-3价N元素的NH3与含+5价N元素的HNO3反应,且反应前后化合价不变,A错误;
B.游离态的氮气与氧气反应生成+2价的NO,符合氮的固定, B正确;
C.含-3价N元素的NH3与氯气反应生成游离态的氮气,不符合氮的固定,C错误;
D.-3价的N元素在反应前后化合价不变, D错误。
故选B。
【变式1-2】(22-23高一下·四川南充·期中)氮是各种生物体生命活动不可缺少的重要元素,下列过程不属于氮的固定的是
A.在一定条件下由氨气和二氧化碳合成尿素B.雷雨闪电时,大气中产生了一氧化氮
C.豆科农作物的根瘤菌使空气中的氮转化为氨D.工业合成氨
【答案】A
【解析】A.氮得固定是将游离态得氮转化成化合态得氮,氨气和二氧化碳合成尿素不属于氮得固定,A错误;
B.雷雨闪电时,大气中产生了一氧化氮反应方程为,属于氮的固定,B正确;
C.豆科农作物的根瘤菌使空气中的氮转化为氨,将游离态的氮转化成了化合态的氮,属于氮的固定,C正确;
D.工业合成氨是将氢气与氮气在高温高压催化剂的条件下合成氨气,属于氮的固定,D正确;
故选A。
【变式1-3】(22-23高一下·广东云浮·月考)下列变化属于固氮的是
A.NO与O2反应生成NO2B.NH3催化氧化生成NO
C.N2和H2在一定条件下反应生成NH3D.由NH3制NH4HCO3和(NH4)2SO4
【答案】C
【解析】A.NO和O2反应生成NO2,是含氮化合物之间的相互转化,不符合氮的固定定义,故A不选;
B.NH3催化氧化为NO,是含氮化合物之间的相互转化,不符合氮的固定定义,故B不选;
C.N2与H2在一定条件下反应生成NH3,氮气是单质,是游离态的氮,转变为化合态NH3,符合氮的固定定义,故C选;
D.由NH3制NH4Cl、(NH4)2SO4等,是含氮化合物之间的相互转化,不符合氮的固定定义,故D不选;
故选:C。
02 氨气的性质
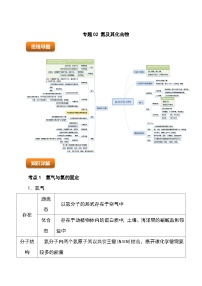
【例2】(23-24高一上·广东深圳·期末)某小组探究的催化氧化,实验装置图如下。③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后,④中产生白烟。下列分析不正确的是
A.③、④中现象说明③中的反应是
B.④中白烟的主要成分是
C.一段时间后⑤中可能变蓝
D.若用氨气进行尾气处理,每处理需消耗氨气
【答案】B
【分析】①中高锰酸钾受热制备氧气,装置②中氯化铵与氢氧化钙共热反应制备氨气,装置③中氨气在催化剂作用下与氧气发生催化氧化反应生成一氧化氮,装置④中反应生成的NO与过量的O2反应生成红棕色气体NO2,NO2与水蒸气反应生成硝酸,硝酸与氨气反应生成硝酸铵,会有白烟产生,装置⑤中氮的氧化物与氧气溶于水反应生成硝酸,硝酸与铜反应生成淡蓝色的硝酸铜溶液。
【解析】A.由分析可知,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟说明③中氨气在催化剂作用下与氧气发生催化氧化生成一氧化氮,反应方程式为:4NH3+5O24NO+6H2O,故A正确;
B.由分析可知,④中白烟的主要成分是硝酸铵,故B错误;
C.装置⑤中氮的氧化物与氧气溶于水反应生成硝酸,硝酸与铜反应生成淡蓝色的硝酸铜溶液,故C正确;
D.用氨气处理尾气NO2,发生的反应的方程式为:,NO2与NH3的化学计量数之比为6:8,则处理0.6mlNO2需消耗0.8ml氨气,故D正确;
故选B。
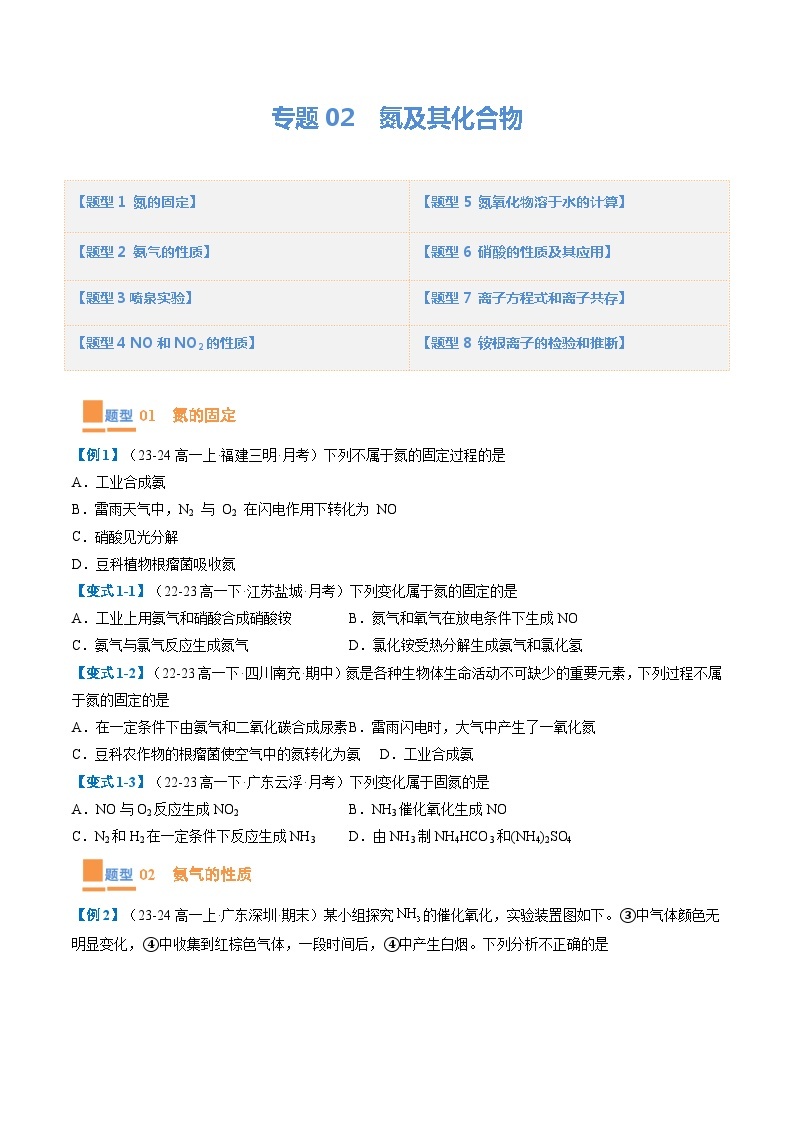
【变式2-1】(22-23高一下·河北衡水·期末)下列装置适用于实验室制氨气并验证氨气的性质,其中能达到实验目的的是
A.用装置甲制取氨气
B.用装置乙除去氨气中的水蒸气
C.丙的原理为
D.装置丁中,干燥烧瓶内盛有氨气,烧杯和胶头滴管内盛有水(含酚酞),挤压胶头滴管的胶头,会出现蓝色喷泉
【答案】C
【解析】A.NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl,气体进入收集装置的机会不多,故A错误;
B.浓硫酸和氨气反应,不能干燥氨气,故B错误;
C.浓氨水和浓盐酸都能挥发,氨气和氯化氢生成氯化铵,有白烟现象,反应方程式为:,故C正确;
D.氨气溶于水显碱性,打开止水夹后会看到红色喷泉,故D错误。
答案选C。
【变式2-2】(23-24高一上·广东东莞·期中)氨气可用来检验氯气是否泄漏,现象是产生大量白烟,反应的化学方程式为,下列有关该反应的叙述正确的是
A.常温常压下,氯气和氨气的密度之比为
B.被氧化与未被氧化的的分子数之比为3∶1
C.常温常压下,消耗的氨气和生成的氮气的体积之比为
D.产生时,消耗的质量为
【答案】C
【解析】A.常温常压下,气体的密度之比等于摩尔质量之比,故氯气和氨气的密度之比为,A错误;
B.根据化学方程式,若有8ml氨气分子,则2ml被氧化,被氧化与未被氧化的的分子数之比为1∶3,B错误;
C.常温常压下,气体体积之比等于物质的量之比,则消耗的氨气和生成的氮气的体积之比为,C正确;
D.没有说明温度和压强,无法进行计算,D错误;
故选C。
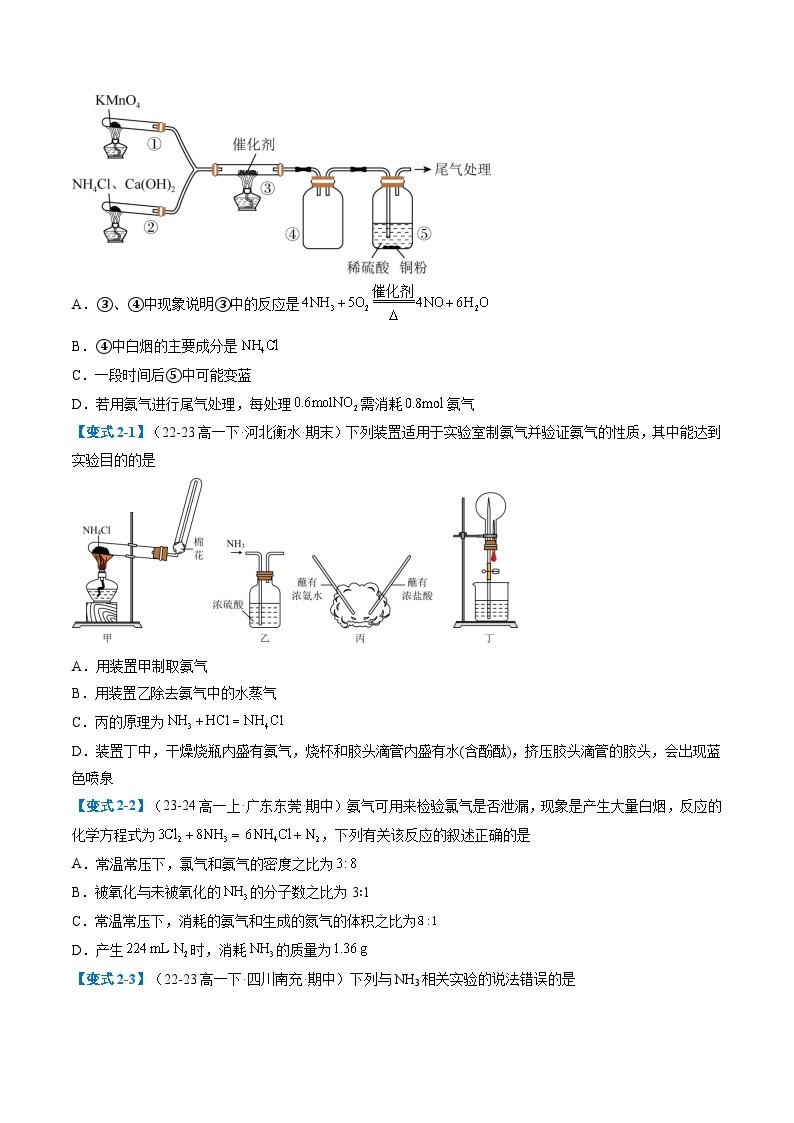
【变式2-3】(22-23高一下·四川南充·期中)下列与NH3相关实验的说法错误的是
A.甲图制备NH3可选用的药品为NH4Cl
B.乙图实验时,可观察到喷泉现象,体现NH3极易溶于水
C.丙图实验中,可观察到有大量白烟生成,说明NH3能与酸反应生成铵盐
D.丁图可用于NH3的尾气处理,且具有防倒吸作用
【答案】A
【解析】A.实验室制备可选用的药品为氢氧化钙与氯化铵的混合物,二者混合加热生成氯化钙、氨气和水,A错误;
B.氨气极易溶于水,可形成喷泉,氨气和水反应生成一水合氨,溶液显碱性,则乙图实验时,可观察到烧瓶中液体为红色,体现氨气是碱性气体,B正确;
C.丙图实验中,可观察到有大量白烟生成,是因为氨气和氯化氢反应生成了固体氯化铵,体现氨水的挥发性,C正确;
D.氨气极易溶于水,倒置的干燥管起防倒吸作用,即丁图可用于氨气的尾气处理,且具有防倒吸作用,D正确;
故选A。
03喷泉实验
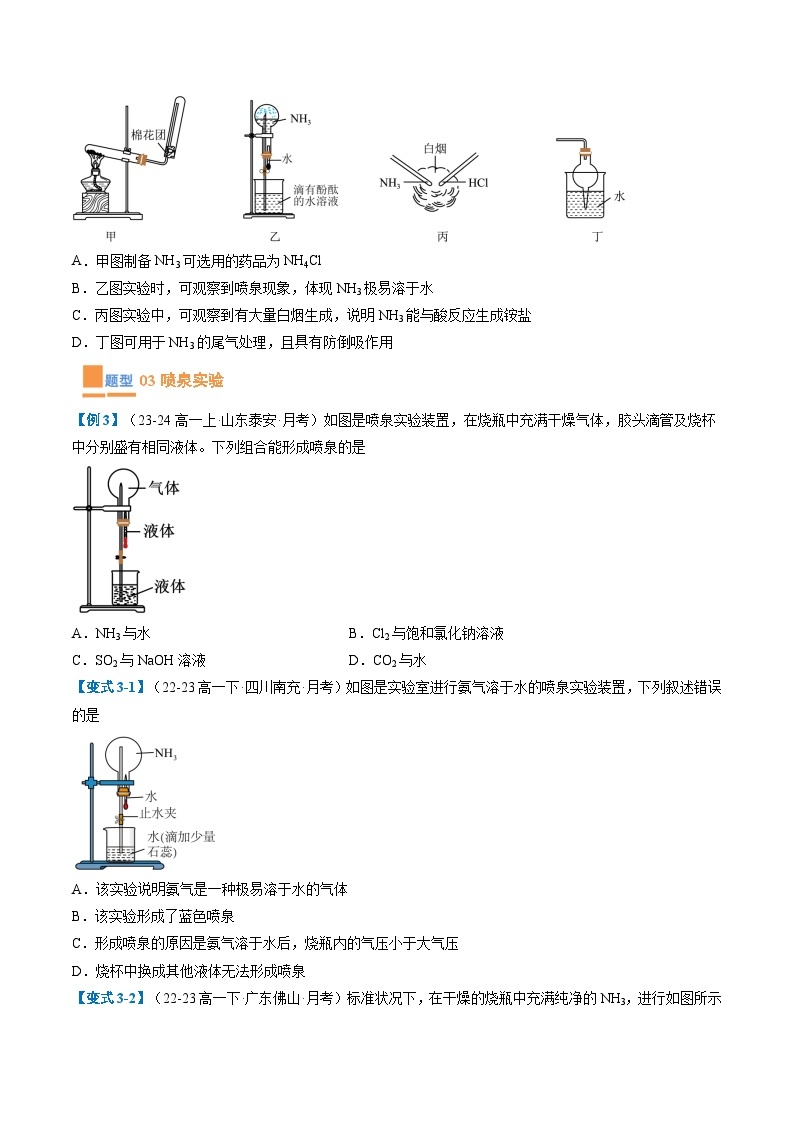
【例3】(23-24高一上·山东泰安·月考)如图是喷泉实验装置,在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有相同液体。下列组合能形成喷泉的是
A.NH3与水B.Cl2与饱和氯化钠溶液
C.SO2与NaOH溶液D.CO2与水
【答案】AC
【解析】A.氨气极易溶于水,因此可以形成喷泉,A项正确;
B.饱和食盐水不吸收氯气,因此无法形成喷泉,B项错误;
C.二氧化硫是酸性气体,易溶于碱液,因此可以形成喷泉,C项正确;
D.常温下二氧化碳与水1:1溶解,溶解度太低无法形成喷泉,D项错误;
答案选AC。
【变式3-1】(22-23高一下·四川南充·月考)如图是实验室进行氨气溶于水的喷泉实验装置,下列叙述错误的是
A.该实验说明氨气是一种极易溶于水的气体
B.该实验形成了蓝色喷泉
C.形成喷泉的原因是氨气溶于水后,烧瓶内的气压小于大气压
D.烧杯中换成其他液体无法形成喷泉
【答案】D
【解析】A.氨气在瓶中因为大量溶解于水,使得瓶内外压强差加大,所以产生喷泉,A正确;
B.氨气是一种碱性气体,溶于水形成一水合氨,是一种弱碱,与石蕊形成蓝色溶液,B正确;
C.因为水被压回瓶内,说明烧瓶内的气压小于大气压,C正确;
D.形成喷泉的原因是形成压强差,烧杯中换成盐酸也可以形成喷泉,D错误;
故答案为:D。
【变式3-2】(22-23高一下·广东佛山·月考)标准状况下,在干燥的烧瓶中充满纯净的NH3,进行如图所示的喷泉实验,下列说法错误的是
A.本实验之所以能够产生喷泉是因为氨气极易溶于水,导致烧瓶内外存在压强差
B.若烧瓶的氨气中混有少量空气,则喷泉实验后的水不能充满烧瓶
C.本实验若将NH3换成HCl,也能产生红色的喷泉
D.若烧瓶氨气中混有少量空气,实验结束后烧瓶中氨水物质的量浓度仍为ml/L
【答案】C
【解析】A.氨气极易溶于水,从而导致烧瓶内外存在压强差,使烧瓶内气压迅速小于大气压,所以形成喷泉,A正确;
B.若烧瓶的氨气中混有少量空气,由于空气中的氮气不溶于水,也不与水反应,则喷泉实验后的水不能充满烧瓶,B正确;
C.若将NH3换成HCl,HCl也极容易溶于水,由于HCl的水溶液显酸性,所以滴有酚酞的水形成的喷泉溶液显无色,C错误;
D.设烧瓶容积为VL,则烧瓶内氨气的物质的量为ml,由于氨水充满烧瓶,所以最终形成氨水的物质的量浓度c=,D正确;
故选C。
【变式3-3】(22-23高一下·山西大同·月考)喷泉是一种常见的现象,其产生的原因是存在压强差。图中有关胶头滴管及止水夹的操作均已略去。下列说法中正确的是
A.从产生喷泉的原理来分析,图1和图2都只能通过减小烧瓶内气体压强来形成喷泉
B.若图1的烧瓶盛装的是,胶头滴管及烧杯中均盛有溶液,不可能形成喷泉
C.常温下,在图2的锥形瓶中加入足量的铁粉与浓硝酸,能形成喷泉
D.在图3装置中,通过控制活塞的开关,可以选择性地使左、右烧瓶中形成喷泉
【答案】D
【解析】A.图2能通过增大下部锥形瓶内气体压强来形成喷泉,A错误;
B. 若图1的烧瓶盛装的是,胶头滴管及烧杯中均盛有溶液,二氧化碳被吸收,减小上部烧瓶内气体压强,能形成喷泉,B错误;
C.常温下,足量的铁粉与浓硝酸发生钝化,在图2的锥形瓶中气体压强几乎不变,不能形成喷泉,C错误;
D. 在图3装置中,如果关闭活塞c,打开活塞a、b,再挤压胶头滴管,有氨气的瓶内气压减小,HCl与氨气结合生成氯化铵,操作的基础上,打开活塞c,烧瓶内气体减少,外压大于内压,形成双喷泉,通过控制活塞的开关,可以选择性地使左、右烧瓶中形成喷泉,若关闭b打开c,则在左边烧瓶产生喷泉,若先打开活塞a,再挤压胶头滴管、再打开c,则在右边烧瓶产生喷泉,D正确;
答案选D。
04 NO和NO2的性质
【例4】(22-23高一下·河北衡水·月考)下列对NO和NO2的描述正确的是
A.NO2与水的反应中,NO2既是氧化剂又是还原剂
B.NO是无色气体,可用向上排空气法收集
C.NO2可由N2和O2直接化合得到
D.从元素化合价角度看,NO只有还原性
【答案】A
【解析】A.与水发生反应:,氮元素由+4价变为+5价和+2价,则既是氧化剂又是还原剂,A项正确;
B.NO易与反应生成,不能用排空气法收集,只能采用排水法收集NO,B项错误;
C.和在高温或放电条件下反应生成NO,不能直接得到,C项错误;
D.NO中氮元素显+2价,处于中间价态,则NO既有氧化性又有还原性,D项错误;
故选A。
【变式4-1】(23-24高一上·江苏连云港·月考)某化学研究小组设计利用硝酸工业尾气(只含NO、NO2)制备亚硝酸钠(NaNO2)的工艺流程如下。已知:。
下列说法错误的是
A.NO2为非电解质
B.用硝酸尾气制备的NaNO2中可能含有NaNO3
C.尾气中NO2的含量越高,NaNO2的纯度越高
D.标准状态下,aL的硝酸尾气用NaOH溶液完全吸收,至少消耗a/22.4mlNaOH
【答案】C
【解析】A.NO2在水溶液中不能因自身发生电离而导电,因此属于非电解质,A项正确;
B.根据已知反应方程式,若NO2过量,NO2和NaOH溶液反应生成NaNO3、NaNO2和,则NaNO2中可能含有NaNO3,B项正确;
C.根据B项分析,尾气中NO2的含量升高,会生成更多的NaNO3,NaNO2的纯度会降低,C项错误;
D.若标准状态下硝酸为气态,aL的硝酸尾气的物质的量为,则用NaOH溶液完全吸收,消耗NaOH,但标准状态下硝酸为液态,aL硝酸的物质的量大于,所以消耗NaOH的物质的量至少为,D项正确;
故选C。
【变式4-2】(22-23高一下·四川南充·期中)下列关于NO和NO2的说法正确的是
A.NO2是红棕色气体,易溶于水,属于酸性氧化物
B.NO2和O2以一定比例混合可以被水完全吸收转化成HNO3
C.NO可以采用向上排空气法进行收集
D.NO2可由N2和O2直接化合得到
【答案】B
【解析】A.NO2是红棕色气体,易溶于水,与水反应产生HNO3、NO,反应前后元素化合价发生变化,因此NO2不属于酸性氧化物,A错误;
B.二氧化氮和氧气可以完全反应4NO2 + O2 +2H2O=4HNO3,B正确;
C.NO易与空气中的氧气反应生成NO2,不可以采用向上排空气法进行收集,C错误;
D.N2和O2直接化合得到NO,NO与O2反应产生NO2,因此NO2不可由N2和O2直接化合得到,D错误;
故选B。
【变式4-3】(2023高一·海南·学业考试)打开充满NO的集气瓶,瓶口出现红棕色(2NO + O2 = 2NO2)。以下说法错误的是
A.NO是无色气体B.NO2是红棕色气体
C.可用排空气法收集NOD.该反应是氧化还原反应
【答案】C
【解析】A.NO是无色无味的气体,A不符合;
B.NO2是红棕色气体,有刺激性气味,B不符合;
C.NO遇到空气反应生成NO2,故不可用排空气法收集NO,C符合;
D.反应过程种由化合价变化,故是氧化还原反应,D不符合;
故答案为:C。
05 氮氧化物溶于水的计算
【例5】(23-24高一上·河北石家庄·调研)有一倒置于水槽且装满水的容器,向其中依次通入一定体积的NO2、NO和O2,充分反应后,若容器中仍充满溶液,则通入的NO2、NO和O2的体积比可能是
A.1∶1∶2B.4∶3∶2
C.4∶16∶13D.4∶3∶4
【答案】C
【分析】反应后容器中仍充满溶液,说明没有气体剩余,根据反应:4NO2+O2+2H2O=4HNO3、4NO+3O2+2H2O=4HNO3进行判断。
【解析】A.若NO2为1体积,NO为1体积,则消耗=1体积O2,故NO2、NO和O2的体积比为1∶1∶1,A项不符合题意;
B.若NO2为4体积,NO为3体积,则消耗体积O2,故NO2、NO和O2的体积比为4∶3∶,B项不符合题意;
C.若NO2为4体积,NO为16体积,则消耗=13体积O2,故NO2、NO和O2的体积比为4∶16∶13,C项符合题意;
D.若NO2为4体积,NO为3体积,则消耗=体积O2,故NO2、NO和O2的体积比为4∶3∶,D项不符合题意;
故选C。
【变式5-1】(22-23高一上·河南新乡·月考)将盛有NO2和N2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的一半,原混合气体中N2与NO2的体积比为
A.1:1B.1:2C.1:3D.3:1
【答案】C
【解析】设原混合气体中含有xmlN2,ymlNO2,盛有N2和NO2 的混合气体的试管倒立于水中发生反应3NO2+H2O=2HNO3+NO,则有,反应后试管内气体物质的量为ml,则有(x+y)=2,解得x:y=1:3,故答案选C。
【变式5-2】(22-23高一下·四川自贡·期末)同温同压下,向三支体积相同的试管中分别充入等体积的两种气体,它们是①NO和O2,②NO2和O2,③NO和NO2。并将三支试管均倒置于水槽中,充分反应后,试管中剩余气体体积分别为V1、V2、V3,则下列关系正确的是
A.V1>V3>V2B.V3>V2>V1C.V3>V1>V2D.V2>V1>V3
【答案】B
【解析】设每种气体各占L,①组合发生反应:4NO+3O2+2H2O=4HNO3,剩余气体的体积为:L -L=L;②组合发生反应:4NO2+O2+2H2O=4HNO3,剩余气体的体积为 L -L=L;③组合生反应:3NO2+H2O=2HNO3+NO,剩余气体的体为: L + = L;则V3>V2>V1,故选B。
【变式5-3】(22-23高一下·河北唐山·月考)如图所示,在注射器里吸入20mLNO,然后吸入5mL水。若再吸入6mLO2,夹住弹簧夹,直到内外大气压相同,观察整个过程。下列叙述正确的是
A.可观察到注射器内气体由无色变成红棕色,最后变成无色
B.可观察到注射器的活塞缓缓向右移动
C.最终剩余气体体积约为14mL
D.所得硝酸溶液的浓度约为
【答案】A
【解析】A.遇空气中氧气生成,为红棕色气体,溶于水生成,气体由红棕色变为无色,正确;
B.4NO+3O2+2H2O=4HNO3,该反应消耗掉全部的氧气和部分NO,注射器内气体被消耗,压强减小,活塞缓缓向左移动,B错误;
C.由可知完全反应,有剩余,剩余体积约为,C错误;
D.题干中并未说明气体所处状态,无法根据其体积计算其物质的量,故无法计算出生成硝酸的浓度,D错误;
故答案选A。
06 硝酸的性质及其应用
【例6】(23-24高一下·河北衡水·调研)下列关于浓硝酸和浓硫酸说法错误的是
A.常温下,可用铁制容器储存浓硫酸、浓硝酸
B.等量的铜分别溶于足量的浓硝酸、浓硫酸中,还原产物的物质的量相等
C.浓硝酸通常保存在棕色试剂瓶中
D.浓硫酸能与灼热的木炭反应,生成二氧化碳、二氧化硫和水
【答案】B
【解析】A. 常温下,铁遇浓硫酸、浓硝酸钝化,在铁表面生成致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应,则可用铁制容器储存浓硫酸、浓硝酸,A正确;
B. 铜与浓硝酸反应的还原产物为NO2,N元素化合价从+5价降低为+4价,与浓硫酸反应的还原产物为SO2,S元素的化合价从+6价降低为+4价,根据得失电子守恒可知,等量的铜分别溶于足量的浓硝酸、浓硫酸,生成NO2的物质的量更多,B错误;
C. 浓硝酸见光易分解,则通常保存在棕色试剂瓶中,C正确;
D. 浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫,发生反应,D正确;
故选B。
【变式6-1】(22-23高一下·陕西咸阳·月考)在铁和铜组成的合金中加入过量硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的溶液,生成沉淀,则下列表示X组成的选项中合理的是
A.B.
C.D.
【答案】A
【分析】在铁和铜组成的合金中加入过量硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的溶液,生成沉淀,则金属离子结合氢氧根离子的物质的量为,根据电荷守恒,铁和铜合金共失去0.6ml电子;
【解析】A.生成0.3mlNO2、0.1mlNO共转移电子的物质的量为0.3ml×1+0.1ml×3=0.6ml,故选A;
B.生成0.1mlNO2、0.3mlNO共转移电子的物质的量为0. ml×1+0.3ml×3=1ml,故不选B;
C.0.6mlNO共转移电子的物质的量为0.6ml×3=1.8ml,故不选C;
D.生成0.3mlNO共转移电子的物质的量为0.3ml×3=0.9ml,故不选D;
选A。
【变式6-2】(23-24高一上·江苏南通·月考)将 锌粉与一定量的浓硝酸反应,当锌粉完全反应时收集到 混合气体共 (标准状况下),则消耗的硝酸的物质的量是
A.1.0mlB.1.1mlC.1.4mlD.1.6ml
【答案】B
【解析】锌和浓硝酸反应生成NO2,而与稀硝酸反应时则生成NO,n(NO2)+n(NO)=11.2L÷22.4L/ml=0.5ml,即被还原的硝酸的物质的量为0.5ml,n(Zn)=19.5g÷65g/ml=0.3ml,则生成的n[Zn(NO3)2]=0.3ml,可知表现酸性的硝酸的物质的量为0.3ml×2=0.6ml,则参加反应的硝酸的物质的量为0.5ml+0.6ml=1.1ml。故选B。
【变式6-3】(22-23高一下·江苏无锡·期末)向含有0.01ml Cu,aml 、bml CuO的混合物中滴加的稀硝酸溶液至10mL时,固体恰好完全溶解,得到标准状况下224mL气体(纯净物)。下列说法正确的是
A.反应过程中转移0.01ml电子B.a:b=1:1
C.被还原的硝酸为0.06mlD.等量上述稀硝酸中最多能溶解0.84g Fe
【答案】B
【解析】A.得到的气体为 NO,中氮元素的化合价从+5价降低到+2价,每生成1ml NO,转移3ml电子,因此生成标准状况下224mLNO时,转移0.03ml电子,A项错误;
B.由Cu原子守恒有,则a:b=1:1,B项正确;
C.被还原的硝酸的物质的量等于生成NO的物质的量,为0.01ml,C项错误;
D.的稀硝酸,体积为10mL时,,最多溶解铁的量,即铁生成亚铁离子,反应方程为,所以最多溶解铁的质量,D项错误;
故选B。
07 离子方程式和离子共存
【例7】(23-24高一上·广东潮州·期中)下列各组离子在溶液中能大量共存的是
A.CO、NO、Mg2+、SO
B.H+、Fe3+、ClO-、SO
C.K+、Na+、MnO、SO
D.H+、NO、I-、Cl-
【答案】C
【解析】A.CO、Mg2+会反应产生MgCO3沉淀,不能大量共存,A错误;
B.H+、ClO-会反应产生弱酸HClO,不能大量共存,B错误;
C.选项离子之间不能发生任何反应,可以大量共存,C正确;
D.H+、NO、I-会发生氧化还原反应,而不能大量共存,D错误;
故合理选项是C。
【变式7-1】(23-24高一上·吉林长春·月考)下列离子方程式正确的是
A.Cl2通入冷的NaOH溶液:Cl2+2OH-=Cl-+ClO-+ H2O
B.用醋酸和淀粉KI溶液检验加碘盐中的IO:IO+5I-+6H+=3I2+3H2O
C.过量铁粉加入稀硝酸中:Fe+4H++NO=Fe3++NO↑+2H2O
D.NaHCO3溶液与少量的Ba(OH)2溶液混合:HCO+Ba2++OH-=BaCO3↓+H2O
【答案】A
【解析】A.氯气和NaOH溶液反应生成氯化钠、次氯酸钠和水,A正确;
B.醋酸是弱酸,不能拆开,反应为IO+5I-+6CH3COOH=3I2+3H2O+6CH3COO-,B错误;
C.过量的铁和稀硝酸生成硝酸亚铁和一氧化氮和水,反应为3Fe+8H++2NO=3Fe2++2NO↑+4H2O,C错误;
D.NaHCO3溶液与少量的Ba(OH)2溶液混合,应按少量的的电离比例书写离子方程式:2HCO+Ba2++2OH-=BaCO3↓+2H2O+ CO,D错误;
故选A。
【变式7-2】(23-24高一上·云南丽江·月考)表示下列反应的离子方程式正确的是
A.硝酸与铁屑反应:
B.碳酸钠溶液与氢氧化钡溶液反应:
C.溶液与稀反应:
D.用醋酸除去水垢:
【答案】C
【解析】A.硝酸与铁生成硝酸铁和NO,反应为,A错误;
B.碳酸钠溶液与氢氧化钡溶液均为强电解质溶液,反应为,B错误;
C.溶液与稀反应生成硫酸钠和水、二氧化碳,C正确;
D.碳酸钙不溶于水,醋酸为弱酸,两者均不能拆,反应为:,D错误;
故选C。
【变式7-3】(22-23高一上·江苏无锡·期中)某溶液中可能含有下列6种离子中的某几种:Cl-、、、、Na+、K+,为确认溶液组成进行如下实验:
(1)取200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。
(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出),由此可以得出关于原溶液组成的正确结论是
A.一定存在、、,可能存在Cl-、Na+、K+
B.一定存在、、、Cl-,一定不存在Na+、K+
C.c()=0.01ml/L,c()>c()
D.如果上述6种离子都存在,则c(Cl-)>c()
【答案】D
【分析】(1)取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成,说明白色沉淀为BaCO3和BaSO4,质量一共是4.3g,则溶液中含有、,向沉淀中加入过量的盐酸,有2.33g沉淀不溶,则硫酸钡的质量是2.33g,其物质的量是2.33g÷233g/ml=0.01ml,碳酸钡的质量是4.3g-2.33g=1.97g,其物质的量是1.97g÷197g/ml=0.01ml;(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体是氨气,物质的量是1.12L÷22.4L/ml=0.05ml,说明溶液中物质的量是0.05ml;根据溶液电中性可知,一定存在Cl-,不能确定是否存在Na+、K+,且氯离子的物质的量最少为0.05ml-0.01ml×2-0.01ml×2=0.01ml;
【解析】A.由分析可知,一定存在Cl-、、、,可能存在Na+、K+,A错误;
B.由分析可知,一定存在Cl-、、、,可能存在Na+、K+,B错误;
C.由分析可知,c()=0.05ml÷0.2L=0.25ml/L,c()=0.01ml÷0.2L=0.05ml/L,c()>c(),C错误;
D.Y如果上述6种离子都存在,则存在钠离子、钾离子中的一种,根据溶液电中性可知,氯离子大于0.01ml,故c(Cl-)>c(),D正确;
故选D。
08 铵根离子的检验和推断
【例8】(23-24高三上·浙江绍兴·月考)探究氮元素及其化合物的性质,下列方案设计、现象和结论都正确的是
【答案】C
【解析】A.氨气极易溶于水,滴加NaOH溶液反应后,由于没有加热,导致氨气没有逸出,则试纸不变蓝,不能确定原溶液中是否含有,A错误;
B.向硝酸亚铁溶液中加入酸性物质,H+与共同作用可将Fe2+氧化为Fe3+而使溶液变黄色,故此实验操作和现象不能证明是H2O2的氧化性强于Fe3+,B错误;
C.Mg和硝酸可以发生氧化还原反应:4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O,此时Mg完全溶解,未出现气泡,生成Mg(NO3)2和NH4NO3,C正确;
D.浓硝酸在热炭作用下受热分解也可以产生NO2,无法证明NO2是由浓硝酸与C反应产生的,D错误;
故选C。
【变式8-1】(23-24高一上·福建·期中)下列关于常见离子的检验方法和结论,其中正确的是
A.用铂丝蘸取待测液在无色的火焰上灼烧,若有黄色火焰产生,证明原溶液一定有钠元素,没有钾元素
B.取待测液加入浓NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝,证明原溶液一定有
C.取待测液加盐酸酸化的BaCl2溶液,产生白色沉淀,证明原溶液一定有SO
D.取待测液加入溶液,有白色沉淀生成,证明原溶液一定有
【答案】B
【解析】A.K元素的焰色反应必须透过蓝色钴玻璃观察,滤去黄光的干扰,原溶液中不一定没有K元素,A错误;
B.能使湿润的红色石蕊试纸变蓝的气体为氨气,加入浓NaOH溶液加热能生成氨气,说明原溶液中一定有,B正确;
C.待测液加盐酸酸化的BaCl2溶液,产生白色沉淀,该白色沉淀可能为氯化银,C错误;
D.加入溶液有白色沉淀生成,可能为硫酸银、碳酸银或氯化银等,应先加入硝酸酸化,D错误;
故选B。
【变式8-2】(23-24高一上·江西宜春·月考)某固体样品可能含有Fe3+、NH、Ag+、NO、Cl−中的若干种离子,为确定该样品的组成,将样品用蒸馏水配成100mL分散系A,进行了如下实验(假设气体全部逸出):
(提示:已知AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O,氯化银能溶于氨水,发生类似反应)下列说法正确的是
A.该样品中肯定含有NH4NO3、AgNO3B.溶液A中NO的物质的量浓度为0.5ml/L
C.溶液A可能含有Cl−D.固体中含NH物质的量 为0.2ml
【答案】C
【分析】100mL分散系A加入40mL 1ml/L的氢氧化钠溶液,恰好完全反应,生成448mL氨气和无色澄清溶液,氨气的物质的量是0.02ml,则原溶液一定含有,一定不含Fe3+;向无色澄清溶液中加入过量盐酸,生成1.435g白色沉淀,则白色沉淀一定是AgCl,物质的量是0.01ml,则无色澄清溶液中含有0.01ml ,原溶液含有0.04ml ,0.01ml Ag+,AgCl能溶于氨水,原溶液可能含Cl−、;
【解析】A.根据以上分析,该样品中可能含有NH4Cl、AgNO3,故A错误;
B.若溶液中含有Cl−,根据电荷守恒,溶液A中NO3-物质的量浓度小于0.5ml·L−1,故B错误
C.AgCl能溶于氨水,溶液A可能含Cl−,故C正确;
D.根据分析,原溶液含有0.04ml ,故D错误;
故选C。
【变式8-3】 (23-24高一上·福建莆田·期中)对于某无色溶液中可能存在离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有
B.加入氢氧化钠溶液后用湿润的红色石蕊试纸靠近试管口,不显蓝色,一定不含
C.加入足量稀HCl后再滴入AgNO3溶液,有白色沉淀生成,原溶液中含有Cl-
D.先滴加HCl溶液,再加BaCl2溶液,有白色沉淀生成,一定有
【答案】D
【解析】A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,生成的气体可能是二氧化硫或二氧化碳,该溶液中有可能是SO、HSO或HCO,不一定有, A错误;
B.NH3极易溶于水,检验是否存在时,需要氢氧化钠的浓溶液或加热,由于本实验中加入了氢氧化钠的稀溶液,可能生成的NH3溶于水生成了NH3·H2O,试管口湿润的红色石蕊试纸未变蓝,不能确定是否含,B错误;
C. 加入足量稀HCl后再滴入AgNO3溶液,必定使氯离子和银离子生成氯化银沉淀,有白色沉淀生成不能确定原溶液中含有Cl ,C错误;-
D. 先滴加HCl溶液,可排除Ag+、SO、等的干扰,再加BaCl2溶液,有白色沉淀生成,则沉淀为不溶于酸的硫酸钡,可证明原溶液一定有,D正确;
答案选D。
【题型1 氮的固定】
【题型5 氮氧化物溶于水的计算】
【题型2 氨气的性质】
【题型6 硝酸的性质及其应用】
【题型3喷泉实验】
【题型7 离子方程式和离子共存】
【题型4 NO和NO2的性质】
【题型8 铵根离子的检验和推断】
实验方案
现象
结论
A
取少量溶液,滴加溶液,将湿润的红色石蕊试纸置于试管口
试纸不变蓝
原溶液中不含
B
取少量溶液,滴入硫酸酸化的溶液
溶液变黄色
氧化性:比强
C
投入到一定浓度的硝酸中
完全溶解,未出现气泡
可能有和生成
D
向浓中插入红热的炭
产生红棕色气体
炭可与浓反应生成
【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题04 无机非金属材料(考点专练)(6大题型).zip: 这是一份【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题04 无机非金属材料(考点专练)(6大题型).zip,文件包含期中复习人教版2019必修第二册2023-2024学年高一下册化学专题04无机非金属材料考点专练原卷版docx、期中复习人教版2019必修第二册2023-2024学年高一下册化学专题04无机非金属材料考点专练解析版docx等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。
【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题02 氮及其化合物(考点梳理+练习).zip: 这是一份【期中复习】人教版2019必修第二册2023-2024学年高一下册化学 专题02 氮及其化合物(考点梳理+练习).zip,文件包含期中复习人教版2019必修第二册2023-2024学年高一下册化学专题02氮及其化合物考点梳理+练习原卷版docx、期中复习人教版2019必修第二册2023-2024学年高一下册化学专题02氮及其化合物考点梳理+练习解析版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。
【期中复习】2023-2024学年(人教版2019必修第二册)高一化学下册 专题02 氮及其化合物(考题预测)(8大题型).zip: 这是一份【期中复习】2023-2024学年(人教版2019必修第二册)高一化学下册 专题02 氮及其化合物(考题预测)(8大题型).zip,文件包含期中复习2023-2024学年人教版2019必修第二册高一化学下册专题02氮及其化合物考题预测8大题型原卷版docx、期中复习2023-2024学年人教版2019必修第二册高一化学下册专题02氮及其化合物考题预测8大题型解析版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。