
江苏省常州市2023_2024学年高二化学上学期10月阶段调研试题无答案
展开考试时间:75分钟页数:共6页满分:100
可能用到的相对原子质量:C-12 H-1 O-16 N-14
选择题:共14题,每小题3分,共42分
1.中国航天科技发展举世瞩目。2020年“嫦娥五号”成功携带月球样品返回地球,2021年“天问一号”着陆火星,它们都是由以液氢为燃料的“长征五号”火箭搭载升空的。下列有关说法错误的是()
A.氢气燃烧的产物不污染环境,有利于实现“碳中和”
B.低温液态储氢可以大大提高氢气的密度,降低储运成本
C.已知,则燃烧热
D.氢气的来源较多,包括水的电解、煤的气化、乙烷裂解和氯碱工业等
2.某化学反应的,,则此反应在下列哪种情况下可自发进行()
A.在任何温度下都能自发进行B.在任何温度下都不能自发进行
C.仅在高温下自发进行D.仅在低温下自发进行
3.对于反应:,下列有关说法不正确的是()
A.使用催化剂能缩短该反应到达平衡的时间
B.升高温度有利于提高的平衡转化率
C.提高的值可增大的转化率
D.增大体系的压强能提高的反应速率和转化率
4.下列变化不能用勒夏特别原理解释的是()
A.工业生产硫酸使用过量的氧气提高二氧化硫的转化率
B.、、HI平衡时的混合气体加压后颜色变深
C.溶液中加入少量固体KSCN后颜色变深
D.实验室用排饱和食盐水的方法收集氯气
5.对于反应:,下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是()
A.B.
C.D.
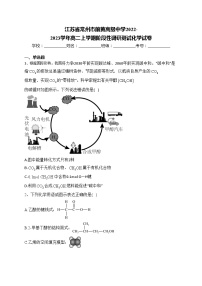
6.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现℃时(各物质均为气态),与水在铜催化剂上的反应机理和能量变化如图。
下列说法不正确的是()
A.反应
B.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
C.和的总能量大于和的总能量
D.反应Ⅱ的热化学方程式表示为
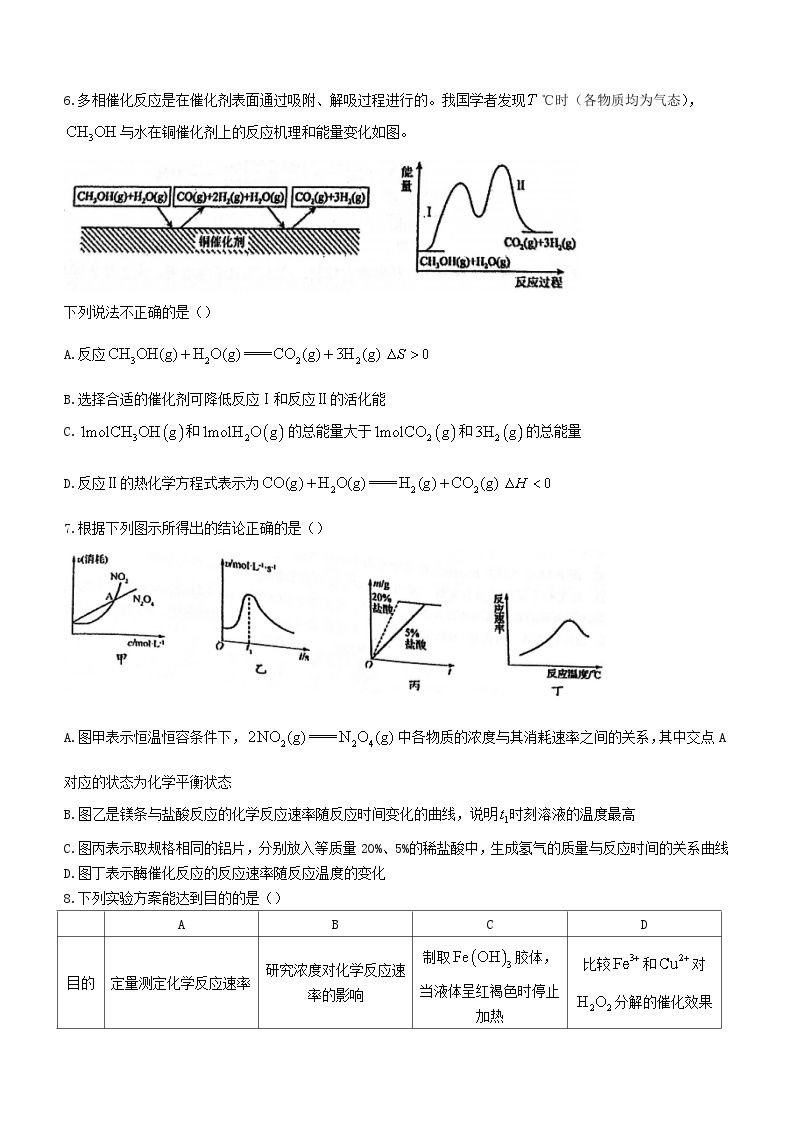
7.根据下列图示所得出的结论正确的是()
A.图甲表示恒温恒容条件下,中各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
B.图乙是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明时刻溶液的温度最高
C.图丙表示取规格相同的铝片,分别放入等质量20%、5%的稀盐酸中,生成氢气的质量与反应时间的关系曲线
D.图丁表示酶催化反应的反应速率随反应温度的变化
8.下列实验方案能达到目的的是()
9.对于反应,下列说法正确的是()
A.体积不变充入惰性气体,反应速率减慢
B.其他条件不变,降低温度,反应速率减慢
C.其他条件不变量,增大压强,活化分子百分数增大,化学反应速率加快
D.若增加或减少A物质的量,反应速率一定会发生明显的变化
10.常压下羟基化法精炼镍的原理为,下列判断正确的是()
A.增加Ni的用量,可加快该反应速率
B.该反应达到平衡时,
C.减压,平衡逆向移动,反应的平衡常数减小
D.选择合适的催化剂可提高CO转化率
11.溶液在不同温度下均可被过量氧化,当完全消耗即有析出,依据析出所需时间可以求得的反应速率。将浓度均为的溶液(含少量淀粉)10.00mL、(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是()
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中N、P两点对应的反应速率相等
C.图中M点对应的反应速率为
D.55℃时未观察到溶液变蓝,说明没有完全消耗
12.用如图所示的装置提纯难挥发的晶体,发生的反应为,将不纯的粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中,下列说法不正确的是()
A.温度:
B.在温度端得到纯净晶体
C.提纯过程中的量在不断减少
D.该反应的平衡常数与和的浓度乘积成正比
13.是种高毒性、高腐蚀性的气体污染物。最新研究表明,在多孔炭材料上搭载活性组分催化氧化脱硫效果明显优于传统的吸附法,其反应机理如图所示。下列有关说法错误的是()
A.活性炭的作用为吸附剂和作催化剂的载体
B.温度越高,多孔炭材料催化氧化脱硫的效果越好
C.增加水膜的酸性会降低反应的速率
D.该反应的总反应方程式为
14.近年来光催化处理船舶尾气技术被称为是一种“绿色友好”技术,以半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成羟基自由基(·OH),光生电子则与等反应在催化剂表面生成、等氧化物,这些氧化物作用于尾气中的、NO等污染物并将其氧化降解,原理见图。下列说法错误的是()
A.除、NO的总反应分别为、
B.催化剂可以改变氮氧化物、硫氧化物被氧化的速率
C.尾气中含有大量有害物质,但经过科学的处理可以转化为多种有实用价值的物质
D.含有氮氧化物、硫氧化物的尾气排放到大气中易形成酸雨,pH小于7的雨水为酸雨
非选择题:4小题,共58分
15.(15分)质子交换膜燃料电池广受关注。
(1)质子交换膜燃料电池中作为燃料的通常来自水煤气。
已知:
则________。
(2)燃料气(流速为;体积分数为:,,,)中的CO会使电极催化剂中毒,使用催化剂可使CO优先氧化而脱除。
①160℃、作催化剂时,CO优先氧化反应的化学方程式为________。
②燃烧草酸铈制得的化学方程式为________。
③在催化剂加入不同的酸(或),测得燃料气中CO优先氧化的转化率随温度变化如图1所示。
图1图2
加入________(填酸的化学式)的催化剂催化性能最好。
(3)图2为甲酸质子交换膜燃料电池的结构示意图。
该装置中________(填“a”或“b”)为电池的负极,负极的电极反应式为________。
16.(15分)工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0,通过电解生成沉淀。有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撤掉)浮渣层,即起到了浮选净化的作用。某科研小组用该原理处理污水,设计装置示意图如图所示。
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣,此时应向污水中加入适量的________。
A.B.C.D.NaOH
(2)电解池阳极实际发生了两个电极反应,其中一个反应生成一种无色气体,则阳极电极反应式分别是①________;②________;
(3)该燃料电池是以熔融碳酸盐为电解质,为燃料,空气为氧化剂,稀土金属材料作电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。
A物质的化学式是________。负极的电极反应式为________。
(4)已知燃料电池中有参加反应,则C电极理论上生成气体________L(标准状况)。
17.(13分)和均为重要的工业原料。已知:
Ⅰ.
Ⅱ.
请回答下列问题:
(1)若反应Ⅱ的逆反应的活化能表示为,则________220.9(填“>”“<”或“=”)。
(2)℃时,向10L恒容密闭容器中充入和,发生反应Ⅰ。5min达到平衡时测得的物质的量为0.2ml。
①0~5min内,用表示的反应速率________。
②的平衡转化率为________。
③下列措施,既能加快逆反应速率又能增大的平衡转化率的是________(填字母)。
A.缩小容器容积B.加入催化剂C.分离出部分D.增大浓度
④℃时,向10L恒容密闭容器中充入和一定量的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比的关系如图所示。
能表示平衡转化率的曲线为________(填“”或“”);点的坐标为________。
18.(15分)(1)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
相关反应的热化学方程式为:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
①总反应的热化学方程式为:________。
②在该过程中和________对总反应起到催化剂作用;使用了催化剂,总反应的________(填“增大”“减小”或“不变”)。
(2)和都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
①阴极上的反应式:________。
②若生成的乙烯和乙烷的体积比为,则消耗的和体积比为________。
(3)法可用于水体中有机污染物降解,其反应机理如图所示。
阴极发生两个不同的电极反应,其中之一产物为X。X微粒的化学式为________;
A
B
C
D
目的
定量测定化学反应速率
研究浓度对化学反应速率的影响
制取胶体,当液体呈红褐色时停止加热
比较和对分解的催化效果
实验方案
江苏省常州市2023_2024学年高二化学上学期期中试题pdf无答案: 这是一份江苏省常州市2023_2024学年高二化学上学期期中试题pdf无答案,共8页。
江苏省常州市联盟学校2023-2024学年高二下学期3月阶段调研考试化学试卷(Word版附答案): 这是一份江苏省常州市联盟学校2023-2024学年高二下学期3月阶段调研考试化学试卷(Word版附答案),文件包含常州市联盟学校20232024学年度第二学期学情调研高二化学试卷docx、常州市联盟学校20232024学年度第二学期学情调研答题卡docx、常州市联盟学校20232024学年度第二学期学情调研高二化学答案docx等3份试卷配套教学资源,其中试卷共13页, 欢迎下载使用。
江苏省无锡2023_2024高三化学上学期期中教学质量调研测试题无答案: 这是一份江苏省无锡2023_2024高三化学上学期期中教学质量调研测试题无答案,共8页。