




2022-2023学年江苏省响水中学高一3月学情分析化学试题
展开考生注意:
1.本试题分第I卷和第II卷,共8页;
2.满分100分,考试时间75分钟;
3.可能涉及的相对原子质量:H-1 C-12 Cu-64 Zn-65 O-16 N-14 Na-23
第I卷(共42分)
一、单选题(本大题共14小题,每小题3分,共42分)
1. 从古至今化学均与生活、生产密切相关,化学工业在各国的国民经济中占有重要地位,是许多国家的基础产业和支柱产业。下列有关说法错误的是
A. 大兴机场的隔震支座由橡胶和钢板相互叠加黏结而成,不属于新型无机材料
B. 敦煌莫高窟壁画中绿色颜料铜绿的主要成分是碳酸铜
C. 南孚干电池低汞化、无汞化,有利于减少废电池造成的土壤污染
D. 战国曾侯乙编钟属于青铜制品,青铜是一种合金
2. 在下列反应CO+H2O⇌CO2+H2中,加入C18O后,则18O存在于
A. 只存于CO和CO2中B. 存在于CO、H2O、CO2中
C. 只存在于CO中D. 存在于CO、H2O、CO2、H2中
3. 已知:H2 (g)+F2(g) =2HF(g) △H=- 270 kJ /ml,下列说法正确的是
A. 1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B. 1 ml 氢气与1 ml 氟气反应生成2ml 液态氟化氢放出的热量小于270kJ
C. 在相同条件下,2 ml 氟化氢气体的总能量大于1 ml 氢气与1 ml 氟气的总能量
D. 2 ml氟化氢气体分解成1ml的氢气积1ml的氟气吸收270kJ热量
4. “空气变面包,氨功不可没”。下列说法正确的是
A. NH3易液化,故液氨可作喷泉实验
B. 氨气是碱性气体,不能选择浓硫酸干燥,可用CaCl2干燥
C. 氨遇到浓盐酸、浓硫酸都会发生反应,产生白烟
D. 合成氨是人工固氮重要途径
5. N2和H2在催化剂表面合成氨的微观历程及能量变化的示意图如图所示,用、、分别表示N2、H2、NH3,下列说法正确的是
A. 使用催化剂时,合成氨反应放出的热量减少
B. 在该过程中,N原子和H原子形成的NH3是电解质
C. 在该过程中,N2、H2断键形成N原子和H原子
D. 合成氨反应中,反应物断键吸收的能量大于生成物形成新键释放的能量
6. 下列实验合理的是
A. 装置甲配制一定浓度的H2SO4溶液B. 装置乙制取少量NH3
C. 装置丙制取并收集NO2D. 装置丁收集SO2
7. 下列实验事实可用同一原理解释的是
A. 二氧化硫使溴水褪色和二氧化硫使品红溶液褪色
B. 久置的浓硫酸和浓硝酸浓度均变小
C. 常温下,可用铝制容器盛装浓硫酸和可用铁槽车装运浓硝酸
D. 分别加热盛有I2和NH4Cl的试管,管口处有固体凝结
8. 化学反应中,反应物用量、浓度或反应条件不同可能对生成物产生影响.下列反应的生成物不受上述因素影响的是( )
A 铜与硝酸反应B. 钠与氧气反应C. 氢气与氯气反应D. 氯化铝与氢氧化钠溶液反应
9. 为了防止钢铁零件生锈,常采用化学处理使钢铁零件表面生成的致密保护层——“发蓝”。化学处理过程中其中一步的反应为:,下列叙述不正确的是
A. 钢铁零件“发蓝”实质上是使铁表面钝化
B. 上述反应中,铁被氧化
C. 的氧化性大于的氧化性
D. 反应中转移电子,生成还原产物
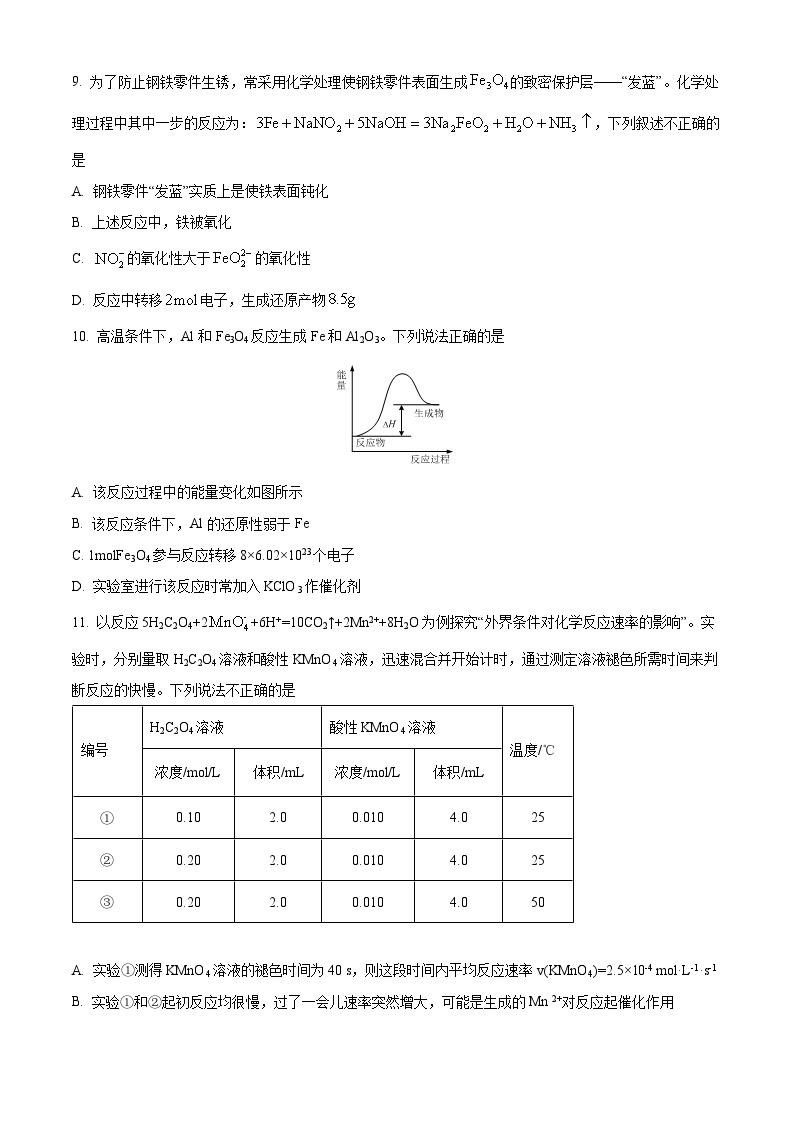
10. 高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是
A. 该反应过程中的能量变化如图所示
B. 该反应条件下,Al的还原性弱于Fe
C. 1mlFe3O4参与反应转移8×6.02×1023个电子
D. 实验室进行该反应时常加入KClO3作催化剂
11. 以反应5H2C2O4+2+6H+=10CO2↑+2Mn2++8H2O为例探究“外界条件对化学反应速率的影响”。实验时,分别量取H2C2O4溶液和酸性KMnO4溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。下列说法不正确的是
A. 实验①测得KMnO4溶液的褪色时间为40 s,则这段时间内平均反应速率v(KMnO4)=2.5×10-4 ml·L-1·s-1
B. 实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的Mn 2+对反应起催化作用
C. 实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影响
D. 实验①、②、③所加的H2C2O4溶液均要过量
12. 将一定质量的铜溶于100mL 11ml/L的浓硝酸中,待铜完全溶解后,生成0.4ml NO2和NO的混合气体,并测得溶液中H+的浓度为1ml/L。假设反应后溶液的体积仍为100mL,则金属铜的质量为
A. 6.4gB. 9.6gC. 12.8gD. 19.2 g
13. 某学生设计了一种家用消毒液发生器,装置如图如示。下列说法错误的是
A. 通电时发生氧化反应B. 通电时电子从阳极经食盐溶液流向阴极
C. 该消毒液的有效成分是NaClOD. 该装置的优点是随制随用
14. “碳呼吸电池”是一种新型化学电源,其工作原理如图。下列说法正确的是
A. 该装置能将电能转变为化学能
B. 正极的电极反应为:C2O42--2e-=2CO2
C. 每得到1 ml草酸铝,电路中转移3 ml电子
D. 利用该技术可捕捉大气中的CO2
第II卷(共58分)
二、填空题,共四大题,合计58分。
15. 按要求填空:
(1)常用作制冷剂的物质的电子式_______;
(2)氮气常用作保护气,但是氮气不能用作金属镁的保护气,其原因用化学方程式表示是_______;
(3)浓氨水可以检验输送氯气管道是否泄露,若泄露则会产生白烟,其原理用化学方程式表示为_______;
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是_______;
(5)汽车尾气(含有烃类、CO、SO2、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为_______;
(6)铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:
请用离子方程式表示以上工艺流程中第①步反应:_______;写出以上工艺流程中第③步反应的化学方程式:_______;若第①步加入的是盐酸,则发生反应的离子方程式为_______。
16. 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
I.将纯锌片和纯铜片按如图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)下列说法正确的是_______。
A. 甲、乙均为化学能转变为电能的装置
B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少
D. 甲、乙两烧杯中溶液的 pH 均增大
(2)在相同时间内,两烧杯中产生气泡的速度:甲_______乙(填“>”“<”或“=”)。
(3)请写出图中构成原电池的负极电极反应式: _______。
(4)当甲中溶液质量增重31.5 g时,电极上转移电子物质的量为_______。
II.新能源汽车的推广使用有利于环境保护,降低碳排放。实施低碳经济是今后经济生活的主流。回答下列问题:
(5)下列措施不利于有效减少二氧化碳的是_______(填字母)。
A. 植树造林,保护森林,保护植被
B. 加大对煤和石油的开采,并鼓励使用液化石油气
C. 大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
D. 推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
(6)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4的物质的量之比混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式: CO2+4H2_______+2H2O
(7) 用CO2合成燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下在体积为1 L的密闭容器中,充入2 ml CO2和6 ml H2,发生反应: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。
①能判断该反应已达化学平衡的标志是_______ (填字母)。
a.CO2百分含量保持不变
b.容器中混合气体的质量保持不变
c.容器中H2浓度与CO2浓度之比为3∶1
d.CO2的生成速率与CH3OH的生成速率相等
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示:
从反应开始到平衡,氢气的平均反应速率v(H2)= _______。
17. 除去工业尾气中的氮氧化合物(NxOy),常用氨催化吸收法,原理是NH3与NxOy反应生成无毒物质。某同学在实验室里采用以下装置和步骤模拟工业上NO的处理过程。
I.NH3的制取
(1)选择装置C制取氨气,检验生成氨气的方法为_______;
II.模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
(2)在上述括号中填入选用的装置编号______。
(3)装置A中反应的离子方程式为_______;
(4)装置D中液体可换成_______(填序号)。
A. H2OB. CCl4C. 饱和食盐水D. 浓硫酸
(5)装置E中NO参加反应的化学方程式为_______;
(6)从环保角度分析,该同学所设计的实验存在的明显缺陷是_______。
18. I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图:
(1)该反应的化学方程式为_______,从反应开始到10s时,Y的转化率为_______,如果想加快该反应速率,可采取的措施有_______。
II.把0.5ml X气体和0.6ml Y气体混合于2L的恒容密闭容器中,使它们发生如下反应:4X(g)+5Y(g)⇌nZ(g)+6W(g),2min末生成0.6ml W,若测知以Z的浓度变化表示的反应速率为0.05ml/(L·min),试计算:
(2)前2min内用X的浓度变化表示的平均反应速率为_______;
(3)2min末时Y的浓度为_______;
(4)2min末,恢复到反应前温度,体系内压强是反应前压强的_______倍。编号
H2C2O4溶液
酸性KMnO4溶液
温度/℃
浓度/ml/L
体积/mL
浓度/ml/L
体积/mL
①
0.10
2.0
0.010
4.0
25
②
0.20
2.0
0.010
4.0
25
③
0.20
2.0
0.010
4.0
50
2023-2024学年江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试(选修)化学试题: 这是一份2023-2024学年江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试(选修)化学试题,文件包含江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试选修化学试题原卷版docx、江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试选修化学试题解析版docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
2023-2024学年江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试(必修)化学试题: 这是一份2023-2024学年江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试(必修)化学试题,文件包含江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试必修化学试题原卷版docx、江苏省盐城市响水县清源高级中学高一下学期3月学情分析考试必修化学试题解析版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
2021-2022学年江苏省响水中学高二下学期第二次学情分析考试化学试题含解析: 这是一份2021-2022学年江苏省响水中学高二下学期第二次学情分析考试化学试题含解析,共24页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。












